
Рефераты по рекламе
Рефераты по физике
Рефераты по философии
Рефераты по финансам
Рефераты по химии
Рефераты по хозяйственному праву
Рефераты по цифровым устройствам
Рефераты по экологическому праву
Рефераты по экономико-математическому моделированию
Рефераты по экономической географии
Рефераты по экономической теории
Рефераты по этике
Рефераты по юриспруденции
Рефераты по языковедению
Рефераты по юридическим наукам
Рефераты по истории
Рефераты по компьютерным наукам
Рефераты по медицинским наукам
Рефераты по финансовым наукам
Рефераты по управленческим наукам
психология педагогика
Промышленность производство
Биология и химия
Языкознание филология
Издательское дело и полиграфия
Рефераты по краеведению и этнографии
Рефераты по религии и мифологии
Рефераты по медицине
Реферат: Ионообменная хроматография
Реферат: Ионообменная хроматография
Ионообменная хроматография
Основы метода
В ионообменной хроматографии разделение компонентов смеси достигается за счет обратимого взаимодействия ионизирующихся веществ с ионными группами сорбента. Сохранение электронейтральности сорбента обеспечивается наличием способных к ионному обмену противоионов, расположенных в непосредственной близости к поверхности. Ион введенного образца, взаимодействуя с фиксированным зарядом сорбента, обменивается с противоионом. Вещества, имеющие разное сродство к фиксированным зарядом, разделяются на анионитах или на катионитах. Аниониты имеют на поверхности положительно заряженные группы и сорбируют из подвижной фазы анионы. Катиониты соответственно содержат группы с отрицательным зарядом, взаимодействующие с катионами.
В качестве подвижной фазы используют водные растворы солей кислот, оснований и растворители типа жидкого аммиака, т.е. системы растворителей, имеющих высокое значение диэлектрической проницаемости и большую тенденцию ионизировать соединения. Обычно работают с буферными растворами, дозволяющими регулировать значение рН.
При хроматографическом разделении ионы анализируемого вещества конкурируют с ионами, содержащимися в элюенте, стремясь вступать во взаимодействие с противоположно заряженными группами сорбента. Отсюда следует, что ионообменную хроматографию можно применять для разделения любых соединений, которые могут быть каким-либо образом ионизированы. Можно провести анализ даже нейтральных молекул сахаров в виде их комплексов с борат-ионом.
Ионообменная хроматография незаменима при разделении вы-сокополярных веществ, которые без перевода в производные не могут быть проанализированы методом ГЖХ. К таким соединениям относятся аминокислоты, пептиды, сахара.
Ионообменную хроматографию широко применяют в медицине, биологии, биохимии, для контроля окружающей среды, при анализе содержания лекарств и их метаболитов в крови и моче, ядохимикатов в пищевом сырье, а также для разделения неорганических соединений, в том числе радиоизотопов, лантаноидов, актиноидов и др. Анализ биополимеров (белков, нуклеиновых кислот и др.), на который обычно затрачивали часы или дни, с помощью ионообменной хроматографии проводят за 20–40 мин с лучшим разделением. Применение ионообменной хроматографии в биологии позволило наблюдать за образцами непосредственно в биосредах, уменьшая возможность перегруппировки или изомеризации, что может привести к неправильной интерпретации конечного результата. Интересно использование данного метода для контроля изменений, происходящих с биологическими жидкостями. Применение пористых слабых анионообмеников на силикагелевой основе позволило разделить пептиды. Механизм ионного обмена можно представить в виде следующих уравнений: для анионного обмена
X- + R+Y- ↔ Y- + R+X-для катионного обмена
X+ + R-Y+ ↔ Y+ + R-X+
В первом случае ион образца X – конкурирует с ионом подвижной фазы Y – за ионные центры R+ ионообменника, а во втором в конкуренцию с ионами подвижной фазы Y+ за ионные центры R – вступают катионы образца Х+.
Естественно, что ионы образца, слабо взаимодействующие с ионообменником, при этой конкуренции будут слабо удерживаться на колонке и первыми вымываются с нее и, наоборот, более сильно удерживаемые ионы будут элюировать из колонки последними. Обычно возникают вторичные взаимодействия неионной природы за счет адсорбции или водородных связей образца с неионной частью матрицы или за счет ограниченной растворимости образца в подвижной фазе. Трудно выделить «классическую» ионообменную хроматографию в «чистом» виде, и поэтому некоторые хроматографисты исходят из эмпирических, а не теоретических закономерностей при ионообменной хроматографии.
Разделение конкретных веществ зависит в первую очередь от выбора наиболее подходящего сорбента и подвижной фазы. В качестве неподвижных фаз в ионообменной хроматографии применяют ионообменные смолы и силикагели с привитыми ионогенными группами.
Полистирольные ионообменные смолы для ВЭЖХ зернением 10 мкм и менее обладают селективностью и стабильностью, но сетчатая структура их, характеризующаяся расстоянием между узлами сетки 1,5 нм, что значительно меньше размера пор применяемого для адсорбционной хроматографии силикагеля (10 нм), замедляет массообмен и, следовательно, значительно снижает эффективность. Применяемые в ВЭЖХ ионообменные смолы представляют собой в основном сополимеры стирола и дивинилбензола. Обычно добавляют 8–12% последнего. Чем больше содержание ди-винилбензола, тем больше жесткость и прочность полимера, выше емкость и, как правило, селективность и тем меньше набухаемость.
Катиониты получают сульфированием матрицы. Протон, ионносвязанный с сульфо-группой, может перемещаться и даже уходить за пределы смолы в раствор. При этом чтобы молекула была в целом электронейтральной, место протона занимает положительно заряженный ион, который из раствора переходит в смолу. Например, при действии Na+Cl – на катионо-обменную смолу в Н+-форме происходит реакция обмена:
Смола – SO4-H+ + Na- → Смола – SO3-Na+ + H+
Если реакция протекает до конца, то смола находится в натриевой (ионной) форме.
Анионообменные смолы получают хлорированием матрицы и последующим алкили-рованием алифатическим амином.
Наиболее распространены аниониты, имеющие четвертичные аммонийные группы, полученные при алкилировании триметиламином.
В этих смолах подвижен анион хлора, который может замещаться другим анионом, например ОН- Катиониты обычно поставляются в Н+-форме или Nа+-форме, а аниониты в ОН--форме или Сl--форме. Таким образом указывается противоион ионо-обменника. Полученные материалы, содержащие сульфатные или триалкиламмонийные группы, являются сильными катионнообменниками и сильными анионообменниками и называются соответственно SCX и SAX. Слабые катионообменники и анионообменники получают на основе карбоксилата СOO- или амина NH+3 соответственно. Существуют также жидкие органические ионообменники – неомешивающиеся с водой жидкости, физически нанесенные на пористые или поверхностно-пористые материалы. Жидкие анионообменники – высокомолекулярные амины или их соли, а катионообменники–эфиры фосфорной или фосфиновых кислот.
Для улучшения условий разделения в ионообменной хроматографии иногда получают лигандные комплексы ионов, изменяя при этом их полярность
Fe3+ + 4Cl- ↔ FeCl4-и делят на анионообменном носителе анионы железа. Так как селективность смолы зависит от характера противоиона, часто необходимо изменить форму смолы. Противоионы связаны кулоновскими силами взаимного притяжения с ионообменными группами и экранируют их заряд. Это притяжение зависит от физической природы противоиона, размеров, формы, плотности электронных оболочек. Одни противоионы при равенстве концентраций могут вытеснять другие из связи с ионными группами ионообменника. Ниже приведены ряды противоионов в порядке убывающей активности и уменьшения сродства к ионообменной смоле.
Знать эти ряды полезно для выбора системы элюирования. Наиболее быстрый метод превращения анионита в форму, которая в ряду селективности стоит выше исходной, состоит в промывании ее четырехкратным объемом 1 М раствора соответствующей соли. Если для работы необходима форма слабее исходной, то ее сначала переводят в гидроксильную форму, промывая 20-кратным количествам 1 М раствора NaOH, а затем уже превращают в нужную форму. Катиониты переводят в требуемую форму промыванием 1 М раствором нитрата соответствующего металла.
При изменении ионной формы смолы или в присутствии органических растворителей, таких, как ацетонитрил, тетрагидрофуран, может изменяться и объем смолы. Если смола уменьшается в объеме, упаковка в колонке оседает и образуется мертвый объем наверху колонки. Это оседание сопровождается потерей эффективности. Если смола набухает и упаковка в колонке увеличивается, то возрастает сопротивление в колонке, значительно уменьшает скорость потока и может даже привести к разрушению
сорбента. Невысокая стабильность ионогенных материалов является одним из недостатков ионообменной хроматографии, причем анионообменники менее стабильны, чем катионообменники. Для увеличения срока службы колонок используют предколонки, а также регенерацию колонок сильным растворителем. Катиониты, например, регенерируют обрабатывая 1 М азотной кислотой и продолжительно промывая той подвижной фазой, которая будет использована.
Ионообменники характеризуются степенью набухания и емкостью. Степенью набухания называют объем упакованного в колонну обменника (в мл), приходящийся на 1 г его в сухом виде, и имеет размерность мл/г. Максимальное количество ионов, которое может связать ионообменник, определяет его емкость, которая совпадает с концентрацией ионогенных групп. Ёмкость выражается числам ммоль эквивалентов обмениваемого иона на 1 г сухого обменника (ммоль экв/г) или на 1 мл упакованного в колонну набухшего ионообменника (ммоль экв/мл) при значениях рН, соответствующих его полной ионизации. Для высокомолекулярных ионов или амфолитов, например белков, вводят понятие «эффективная» емкость, кoтоpaя зависит от размера молекулы амфолита, расстояния между ионогенными группами и степени доступности всего объема пористой матрицы обменника для этих молекул. Понятия емкости и эффективной емкости могут не совпадать. Иногда приходится снижать полезную емкость сорбента за счет изменения рН, увеличивая при этом его эффективную емкость. Катионообменные смолы имеют емкость около 4,4 ммоль экв/г, а анионообменные – 3,5–4 ммоль экв/г для гелеобразной структуры и 2,5 ммоль экв/г для пористой. Обменная емкость изменяется при изменении рН. При низких рН происходит нейтрализация катионита при добавлении протона:
R-+H+ ↔ R-H+,
а при высоких рН подобным образом при действии щелочи нейтрализуются аниониты:
R++OH- ↔ R+OH-.
Поскольку ионообменная емкость сильных катионитов падает до нуля при низких рН, они не могут быть использованы при рН<1. Сильные аниониты должны применяться при рН<11, слабые катиониты при рН>6, а слабые аниониты при рН<8. Из рисунка видно, что сильные ионообменники могут быть использованы в более широком диапазоне рН, чем слабые. Этим объясняется широкое применение сильных ионитов, на которых может быть разделено большее количество веществ разных классов одновременно, особенно если используется градиентное изменение рН. Сильно удерживаемые вещества, нестойкие при крайних зна чениях рН, могут разделяться на слабых ионитах. Еще раз подчеркнем, что сильные иониты полностью ионизированы в диапазоне рН=2–11. Слабые иониты полностью ионизированы в ограниченной области рН, и их ионизацией можно управлять, меняя рН элюента в пределах диапазона рабочих значений рН.
Таким образом, к категории слабых могут быть отнесены ионообменники, значительно отличающиеся друг от друга. Для них характерно не толыко сужение рабочего диапазона рН, но и уменьшение прочности сорбции вещества внутри этого диапазона. Слабым ионообменникам, в частности анионитам с замещающими группами диэтиламиноэтила (ДЕАЕ), отдают предпочтение в тех случаях, когда необходимо элюирование в мягких условиях, например, при разделении белков и пептидов.
Наибольший интерес в качестве сорбентов для ионообменной хроматографии представляет химически модифицированный силикагель, получаемый прививкой к силикагелю ионогенных групп.
Таблица 1. Характеристика модифицированных силикагелей и ионообменных смол
| Характеристика | Силикагель | Смола (сополимеры полистирола с дивинилбензолом) |
| Типичный диаметр частицы в мкм | 5–10 | 7–10 |
| Типичная ионообменная емкость, в мэкв/г | 0,5–2 | 3–5 |
| Стойкость к деформации давлением | Очень хорошая | От удовлетворительной до плохой (в зависимости от степени сшивки) |
| Форма | Сферическая или неправильная | Сферическая |
| Перепад давления на колонке | Высокий | Очень высокий |
| Эффективность | Высокая | Низкая |
| Метод набивки | Суспензионный | Суспензионный |
| Диапозон рН | 2–7,5 | 0–12 (анионообменные) 0–14 (катионообменные) |
| Скорость регенерирования | Умеренная | Медленная |
Применение этих материалов значительно увеличивает стабильность работы колонок, в которых не происходит изменения эффективности. Однако сильнокислые или сильноосновные среды (2>рН>7,5) могут воздействовать на силикагель, выводя из строя колонку. Привитые к силикагелю ионообменники могут быть нестабильны при действии органических растворителей, концентрированных буферных растворов, высоких температур. Ионообменные силикагели зернением 10 или 5 мм не набухают, не сжимаются, как смолы, и отличаются от них большИМ размером и доступностью внутренних пор как для ионов образца, так и для противоионов. Благодаря этому быстрее устанавливается массоперенос даже без повышения температуры и значительно возрастает эффективность сорбента.
Не существует слабых катионитов на основе силикагеля, так как при рН<8 материал не ионизирован, а при рН>8 разрушается подложка наполнительного материала. Сравнительные характеристики модифицированных силикагелей и ионообменных смол, применяемых в ионообменной хроматографии, даны в табл. 1.
Выбор подвижной фазы и условий разделения
Подвижная фаза в ионообменной хроматографии должна обеспечивать растворимость различных солей и создание буферного раствора, необходимых для ионного обмена, контроль степени удерживания образца за счет использования растворителя нужной силы, получения необходимой селективности разделения.
Ионообменное, разделение обычно выполняют при применении водных растворов солей, которым придаются буферные свойства. Иногда добавляют в подвижную фазу небольшое количество смешивающихся с водой органических растворителей – метанола, этанола, ацетонитрила, тетрагидрофурана. Сила и селективность растворителя зависят от типа и концентрации буферных ионов и других солей, от значения рН и от вида и концентрации добавленных органических растворителей.
Удерживание в ионообменной хроматографии зависит от двух процессов: распределения образца между водной подвижной фазой и органической неподвижной и образования ионных пар (т.е. анионного или катионного обмена), причем последний процесс доминирует.
Распределение вещества между фазами зависит от силы электростатического взаимодействия заряженных ионизированных групп вещества с заряженными группами ионообменника. Некоторые гидрофобные соединения или вещества, способные образовывать водородные связи, могут взаимодействовать с материалом матрицы неспецифически.
Степень удерживания образца снижается с увеличением ионной силы подвижной фазы и увеличивается с увеличением ионообменной емкости сорбента. Ионная сила подвижной фазы возрастает при возрастании концентрации буфера и сохранении неизменным рН или при добавлении соли. Важна также концентрация буферных растворов, так как в растворе наблюдается конкуренция между ионами образца и буфера. Уменьшение концентрации буферного раствора увеличивает сродство смолы к образцу, что приводит к увеличению времени удерживания. Концентрация буферного раствора колеблется от 0,001 до 6 моль/л, причем верхняя граница определяется растворимостью соли, используемой в качестве буфера, а нижняя – самой буферной силой, так как в слабом буферном растворе нельзя контролировать уровень рН. Сильных буферных растворов также следует избегать, так как возможно выпадение осадка и забивание колонок. Сила растворителя зависит от типа противоиона, причем степень удерживания образца увеличивается в ряду, обратном ряду активности ионов, приведенному выше.
При анализе рН раствора выбирают таким образом, чтобы молекула образца была полностью ионизирована, обычно для кислот рН≅рКα+1,5, а для оснований рН≅рКα+1,5. Изменение рН подвижной фазы влияет на удерживание образца. Оно с повышением рН увеличивается при анионообменном разделении и уменьшается при катионообменном, т.е. происходит уменьшение силы растворителя при анионном и увеличение при катион-ном обмене. Особенно сильно влияет изменение рН раствора, происходящее вблизи значений рКα образца.
В ионообменной хроматографии применяют следующие буферные растворы: ацетатный, фосфатный, цитратный, формиатный, аммиачный, боратный. Селективность разделения в ионообменной хроматографии зависит от концентрации и вида буферных ионов и органических растворителей, а также от рН среды. Ионообменное разделение проходит в пределах температур от комнатной до 60 °С. Чем выше температура, тем меньше вязкость подвижной фазы и тем эффективнее разделение. Однако при высокой температуре стабильность колонки или образца может быть нарушена. Многие ионо-обменники выдерживают температуру до 60 °С, а некоторые полимерные катионообмен-ники – даже до 80 °С. Биохимические пробы принято разделять при низких температурах, часто при 4 °С, хотя в современной ВЭЖХ при быстрых разделениях вероятность разрушения образца при 20–30 °С резко снижается. Повышение температуры может привести к снижению k' для всех компонентов образца, а снижение ионной силы подвижной фазы может привести к обратному явлению.
Вводимые количества образца не должны превышать 5% суммарной ионообменной емкости. Так, для соединений с молекулярной массой 200–500 предполагается введение около 50 мг пробы на 1 г полимерного сорбента. Желательно, чтобы вводимый объем образца не превышал 1/3 объема первого интересующего пика.
В подвижную фазу добавляют иногда органические растворители (метанол, этанол, ацетонитрил, диоксан), действие которых аналогично добавлению растворителей в обращенно-фазной хроматографии: при увеличении их количества степень удерживания образца снижается, и этот эффект более силен для менее полярных растворителей. Добавлением органических растворителей можно добиться также изменения селективности системы. Таким образом, снижают время удерживания в ионообменной хроматографии следующие факторы: 1) повышение температуры; 2) повышение концентрации буферного раствора; 3) снижение степени ионизации вещества за счет изменения рН.
Ионная хроматография
Особым видом ионообменной хроматографии, применяемым для анализа органических и неорганических ионов, не поглощающих в УФ-области, является ионная хроматография. В этом методе ионообменное разделение ионов сочетают с кондукто-метрическим определением их. Поскольку высокочувствительное кондуктометрическое определение возможно только при невысокой фоновой электропроводности потока жидкости, поступающей в детектор, фоновый электролит подвижной фазы предварительно удаляют пропусканием его через ионообменные смолы.
Предложены два основных метода ионной хроматографии.
1. Двухколоночная ионная хроматография, основанная на компенсации (подавлении) электролита, содержащегося в элюенте для разделения смеси ионов на колонке с помощью второй ионообменной колонки, расположенной между детектором и раздели тельной колонкой. Этот метод и был ранее назван ионной хроматографией.
Вещества разделяются на катионообменной колонке 4 по ионообменному механизму, попадают в десорбционную колонку 5 со смолой в ОН-форме, где происходит нейтрализация подвижной фазы и удаление электролита из элюента. Анализируемые вещества выходят из колонки 5 в деионизиванной воде и попадают в кондуктометрическую кювету 6. Сигнал с кондуктометра 7 поступает на самописец 8 или интегратор. На аналогичной установке анализируют анионы. Так как десорбционную колонку приходится часто регенерировать, отношение объемов, пропущенных через колонку 5, к объемам, допущенным через колонку 4, должно быть меньше или равно 1O. Предложений схемы разделения для ионной хроматографии и варианты заполнения разделительной и десорбирующей колонок.
2. Другим вариантом ионной хроматографии является одноколоночная ионная хроматография, основанная на использовании электролита с невысокой электропроводностью. В этом случае компенсационная колонка отсутствует.
Метод подробно не рассматривается нами, так как имеется ряд неплохих обзоров по ионной хроматографии [17, 18].
Ионнные хроматографы от простых до полностью автоматических выпускают фирмы «Даонекс корпорейшн», «Бекман» (США) и др. В СССР ионные хроматографы серийно выпускаются Джержинским ОКБА. Методом ион-хроматографии определяют неокрашенные анионы и катионы, находящиеся в образце в виде примесей, и микроколичества вредных веществ в воде, воздухе и биологических жидкостях.
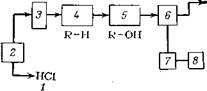
Рис. 1. Схема установки для анализа катионов методом ионной хроматографии: 1 – емкость с элюентом; 2 – насос: 3 – ввод пробы; 4 – разделительная колонка; 5 – десорбирующая колонка; 6 – кондуктометрическая кювета; 7 – кондуктометрический детектор; 8 – самописец
Практические рекомендации
Ионообменная хроматография в экспериментальном отношении – один из самых трудных видов ВЭЖХ, так как имеется много параметров, которые необходимо учитывать и контролировать.
Если анализ необходимо вести при рН ниже 2 или выше 7,5, то должна быть применена соответствующая анионная или катионная смола, а в остальных случаях – силикатель с привитой ионообменной смолой.
Для анализа молекул с молекулярной массой до 2000 применяют ионообменники с химически привитой фазой к силикагелю с размером частиц 5–10 мкм, а при препаративном разделении можно применять полимерные пористые сорбенты типа даррум ДА-Х8. При разделении крупных молекул с молекулярной массой 2000 применяют слабоосновный ионит, привитый на крупнопористый силикагель.
Скорость элюента обычно устанавливают 1 мл/мин, температуру 50 °С или комнатную, если контроль температуры неудобен, а рН подбирают так, чтобы компоненты были ионизированы.
Так как в ионообменной хроматографии изотермы не параллельны, необходимо найти оптимальную для каждого частотного разделения температуру, изменяя ее с инкрементом 10 °С. Обычно придерживаются середины найденного интервала оптимальных температур, контролируя ее с точностью 1 °С.
Для создания определенного рН и поддержания на необходимом уровне готовят соответствующий буферный раствор. Если это возможно, то буферный раствор подбирают таким образом, чтобы его функциональная группа была похожа на функциональную группу образца. Так, ацетатный буферный раствор приемлем для анализа карбоновых кислот, фосфатный – для люирования нуклеотидов. Большое значение имеет чистота буферного раствора, так как он не должен детектироваться выбранным детектором, что особенно важно при работе в режиме градиентного элюирования. Чистота буферного раствора зависит от фирм-производителей, и даже разные партии одной фирмы могут различаться по составу. Каждая новая партия буферного раствора тестируется двумя холостыми хроматографическими опытами перед использованием. Второй опыт показывает, существуют ли вещества, отложившиеся в колонке в процессе регенерации или в течение последних стадий предыдущего градиента. Хотя большинство разделений проводят в водных буферных растворах, иногда добавляют органический растворитель (метанол, этанол) в количестве 3–10% для повышения селективности и улучшения растворимости образца. При этом концентрация растворителя не должна быть велика, чтобы не выдать осаждения буферной соли, о чем будет свидетельствовать появление течи в системе и увеличение сопротивления в колонке.
При работе в градиентном режиме желательно, чтобы к концу разделения ионная сила буферного раствора повышалась. Начинают работать с концентрации буферного раствора 0,1 M, так как оптимизация разделения при работе с низкими концентрациями (0,001 М) отнимает много времени. Если при этих условиях вещества не удается удовлетворительно разделить, то дальнейшее улучшение разделения происходит за счет снижения концентрации буферного раствора, изменения рН или температуры шаговым методом, приводящих к повышению значений k' и увеличению времени удерживания.
Часто в буферный раствор для регулирования силы подвижной фазы добавляют нейтральные соли. Особой популярностью пользуется нитрат натрия, поскольку он не вызывает коррозии аппаратуры. Галогенид-ионы оказывают вредное влияние на нержавеющую сталь, и поэтому их лучше не применять.
Сравнивая сорбенты, предназначенные для ионообменной хроматографии, с сорбентами, применяемыми в других вариантах ВЭЖХ, можно отметить ряд недостатков у первых.
Применяемые в ионообменной хроматографии сорбенты менее эффективны и стабильны, а также менее воспроизводимы, Улучшить эффективность разделения ионогенных соединений можно, повысив температуру до 60 °С, изменив рН, добавив органический растворитель или перейдя от ионообменной хроматографии к работе в режиме ион-парной хроматографии или обращенно-фазной хроматографии с использованием метода подавления ионов.
Повышения стабильности достигают за счет очистки образца, уменьшения температуры и рН, снижения количества органических растворителей. Для рутинного анализа и лучшей воспроизводимости желательно использовать колонки, набитые в лаборатории.
Литература
1. Krstulovic A.M., Brown P.R. Reversed-Phase Liquid Chromatography; Theory, Practice and Biomedical Applications. J. Wiley. N.Y., 1982. 296 p.
2. Hamaji M., Seki Г./J. Chromatogr., Biomed. Appl., 1979, v. 163, p. 329 – 336.
3. Фритц Дж., Гьерзе Д.Г., Поланд К. Ионная хроматография: Пер. с англ. / Под ред. В.Г. Березкина. М., Мир, 1984. 224 с.
4. Шпигун О.А., Золотое Ю.Л. / Зав. лаб., 1982, т. 48, №9, с. 4.
5. Small Я./Anal. Chem., 1983, v. 55, p. 235A.
6. Беленький Б.Г., Виленчик Л. 3. Хроматография полимеров. М., Химия, 1978. 344 с.
7. Van W., Kirkland J., Bly D. Modern Size-Exclusion Liquid Chromatography. N.Y., J. Wiley, 1979. 476 p.
8. Нефедов П.П., Лавренко П.Н. Транспортные методы в аналитической химии полимеров. Л., Химия, 1979. 232 с.
9. Тенников М.Б. и dp. / Высокомол. соед., 1977, т. А19, №3, с. 657 – 660.
10. Mori S., Suzuki T./Anal. Chem, 1980, v. 52, No. 11, p. 1625–1629.
© 2009 База Рефератов