
Рефераты по рекламе
Рефераты по физике
Рефераты по философии
Рефераты по финансам
Рефераты по химии
Рефераты по хозяйственному праву
Рефераты по цифровым устройствам
Рефераты по экологическому праву
Рефераты по экономико-математическому моделированию
Рефераты по экономической географии
Рефераты по экономической теории
Рефераты по этике
Рефераты по юриспруденции
Рефераты по языковедению
Рефераты по юридическим наукам
Рефераты по истории
Рефераты по компьютерным наукам
Рефераты по медицинским наукам
Рефераты по финансовым наукам
Рефераты по управленческим наукам
психология педагогика
Промышленность производство
Биология и химия
Языкознание филология
Издательское дело и полиграфия
Рефераты по краеведению и этнографии
Рефераты по религии и мифологии
Рефераты по медицине
Дипломная работа: Исследование твердых электролитов
Дипломная работа: Исследование твердых электролитов
Введение
Ионика твердого тела как
область науки, лежащая на пересечении физики и химии твердого тела, электроники
и электрохимии, кристаллографии и неорганической химии, материаловедения и
энергетики получила широкое признание в последние 10-15 лет. В советском союзе
начало исследованиям твердых электролитов было положено в 60-е годы в Институте
электрохимии УрО РАН, Екатеринбург (школа акад. СВ. Карпачева; профессора В.Н.
Чеботин, М.В. Перфильев и С.Ф. Пальгуев), СПбГУ (проф. А.Н. Мурин), МГУ (работы
акад. Ю.Д. Третьякова), Институте новых химических проблем, Черноголовка (проф.
Е.А. Укше, д-р хим. наук Н.Г. Букун), Институте электрохимии, Москва (канд.
техн. наук B.C. Боровков, д-р хим. наук Ю.Я. Гуревич). В последние годы в связи
с открытием большого числа новых материалов с высокой ионной проводимостью,
созданием макетов полностью твердотельных топливных элементов, новыми
теоретическими подходами к изучению явлений аномально быстрого ионного переноса
в конденсированных средах и использованием новых мощных экспериментальных
методик - в мире отмечается все более возрастающий интерес к суперионным
проводникам и устройствам на их основе. Электролиты твёрдые, вещества, в
которых электропроводность осуществляется движением ионов одного знака - катионами
или анионами. Ионы передвигаются по свободным позициям в структуре в-ва,
разделенным невысокими потенц. барьерами (0,1-0,5 эВ). Количество позиций, которые
могут занимать ионы проводимости, намного больше кол-ва самих ионов. Кроме
того, эти позиции могут различаться по степени заселенности ионами. Например, в
элементарной ячейке![]() -Agl на 42 позиции приходятся 2 иона Ag+, причем 12 тетраэдрит,
позиций являются предпочтительными. Таким. образом, подрешетка ионов
проводимости разупорядочена, в то время как остальные ионы твердых электролитов
образуют жесткий каркас, и их перенос возможен по обычным механизмом
образования точечных дефектов (вакансий и междоузельных ионов). Ионная
составляющая
-Agl на 42 позиции приходятся 2 иона Ag+, причем 12 тетраэдрит,
позиций являются предпочтительными. Таким. образом, подрешетка ионов
проводимости разупорядочена, в то время как остальные ионы твердых электролитов
образуют жесткий каркас, и их перенос возможен по обычным механизмом
образования точечных дефектов (вакансий и междоузельных ионов). Ионная
составляющая![]() общей проводимости твердых электролитов, как правило, на 5-6 порядков больше
электронной, т. е. числа переноса ионов проводимости практически равны 1. Коэф.
диффузии Di этих ионов сравнимы с таковыми для конц. водных р-ров и
соответствуют величинам порядка 10-5 - 10-6 см/с. твердые электролиты относят к
суперионным проводникам и часто называют супериониками. Однако суперионик -
более общее понятие, относящееся к высокопроводящим соединениям как с ионной
проводимостью (электролиты твёрдые), так и со смешанной ионно-электронной
проводимостью. В электрохимических системах суперионики со смешанной
проводимостью выполняют роль электродов. Температурная зависимость ионной
проводимости электролиты твёрдые
общей проводимости твердых электролитов, как правило, на 5-6 порядков больше
электронной, т. е. числа переноса ионов проводимости практически равны 1. Коэф.
диффузии Di этих ионов сравнимы с таковыми для конц. водных р-ров и
соответствуют величинам порядка 10-5 - 10-6 см/с. твердые электролиты относят к
суперионным проводникам и часто называют супериониками. Однако суперионик -
более общее понятие, относящееся к высокопроводящим соединениям как с ионной
проводимостью (электролиты твёрдые), так и со смешанной ионно-электронной
проводимостью. В электрохимических системах суперионики со смешанной
проводимостью выполняют роль электродов. Температурная зависимость ионной
проводимости электролиты твёрдые![]() описывается ур-нием:
описывается ур-нием:
![]()
где А - константа, Т -
абс. т-ра, Еа - энергия активации, k -константа Больцмана. Значение![]() и Еа для наиб, известных
электролиты твёрдые приведены в таблице. Электролиты твёрдые подразделяются на
электролиты с собственным структурным разупорядочением в одной из подрешеток и
с примесным. К первым относятся в-ва, структура к-рых либо уже имеет пути
проводимости для ионов определенного типа, как, напр., Na-
и Еа для наиб, известных
электролиты твёрдые приведены в таблице. Электролиты твёрдые подразделяются на
электролиты с собственным структурным разупорядочением в одной из подрешеток и
с примесным. К первым относятся в-ва, структура к-рых либо уже имеет пути
проводимости для ионов определенного типа, как, напр., Na-![]() -глинозем (полиалюминат
натрия Na1+xAl11O17), либо приобретает их вследствие фазового перехода, как,
напр., Agl (
-глинозем (полиалюминат
натрия Na1+xAl11O17), либо приобретает их вследствие фазового перехода, как,
напр., Agl (![]() -переход при 420 К). Пути проводимости могут иметь вид каналов [напр., в
(C5H5NH)Ag5I6], щелей (напр., в Na-
-переход при 420 К). Пути проводимости могут иметь вид каналов [напр., в
(C5H5NH)Ag5I6], щелей (напр., в Na-![]() -глиноземе) или трехмерных сеток
(напр., в
-глиноземе) или трехмерных сеток
(напр., в![]() -Agl). К электролиты твёрдые с примесным разупорядочением относятся твердые
р-ры замещения, образующиеся в ионных кристаллах при легировании их ионами с
валентностью, отличной от валентности основного иона. Возникающий при этом
дефицит (или избыток) заряда компенсируется образованием дефектов
противоположного знака. Так, в оксидах Zr, Hf, Се и Th, легир. оксидами двух- и
трехвалентных металлов (Са, Y, Sc и др.), компенсация заряда примеси
осуществляется кислородными вакансиями. Флюорит CaF2 и изоморфный ему SrF2
образуют твердые р-ры замещения с фторидами трехвалентных РЗЭ, обладающих
высокой подвижностью ионов F-. Последние легко обмениваются на ионы
О2-. Характерное свойство твердых электролитов - способность к
замещению одних ионов проводимости на другие. Например, при выдерживании Na-
-Agl). К электролиты твёрдые с примесным разупорядочением относятся твердые
р-ры замещения, образующиеся в ионных кристаллах при легировании их ионами с
валентностью, отличной от валентности основного иона. Возникающий при этом
дефицит (или избыток) заряда компенсируется образованием дефектов
противоположного знака. Так, в оксидах Zr, Hf, Се и Th, легир. оксидами двух- и
трехвалентных металлов (Са, Y, Sc и др.), компенсация заряда примеси
осуществляется кислородными вакансиями. Флюорит CaF2 и изоморфный ему SrF2
образуют твердые р-ры замещения с фторидами трехвалентных РЗЭ, обладающих
высокой подвижностью ионов F-. Последние легко обмениваются на ионы
О2-. Характерное свойство твердых электролитов - способность к
замещению одних ионов проводимости на другие. Например, при выдерживании Na-![]() -глинозема в
расплаве AgNO3 ионы Na+ полностью замещены ионами Ag+.
Если же Ag-b-глинозем поместить в р-р к-ты, то можно получить
-глинозема в
расплаве AgNO3 ионы Na+ полностью замещены ионами Ag+.
Если же Ag-b-глинозем поместить в р-р к-ты, то можно получить![]() глинозем с высокой
проводимостью по протонам - ионам Н+.
глинозем с высокой
проводимостью по протонам - ионам Н+.
Характеристика поликристалических твердых электролитов
| Электролит | Подвижный ион |
|
Ea,эВ |
|
|
Ag+ | 337 (423 K) | 0,101a |
| RbAg4I5 | Ag+ | 28 | 0,104 |
| Ag6WO4I4 | Ag+ | 4,2 | 0,248 |
| (C5H5NH)Ag5I6 | Ag+ | 21 (323 K) | 0,198б |
| Cs2Ag3Br3I2 | Ag+ | 0,1 | 0,38 |
| Cu4RbCl3I2 | Cu+ | 47 | 0,115 |
| Na2O x 10Al2O3e | Na+ | 3,3 | 0,140 |
| Na2O x 10Al2O3 | Na+ | 0,5 | 0,148 |
| Na3Zr2Si2Р012 | Na+ | 14 (573 K) | 0,246д |
| Nа3Sс2(РO4)3 | Na+ | 19 (573 K) | 0,144в |
| Na5DySi4O12 | Na+ | 0,50 | 0,208 |
| CsHSO4 | H+ | 1,8 (435 K) | 0,33ж |
| HUO2PO2 x 4H2O3 | H+ | 0,32 | 0,32 |
| H3PW12O40 x 19H2O3 | H+ | 1,20 | 0,432 |
| Cs3PW12O40 x 10H2O3 | H+ | 1,6 | 0,223 |
| Sb2O5 x 5,43H2O3 | H+ | 0,75 | 0,16 |
| 0,75Li4GeO4 x 0,25Li3PO4 | Li+ | 9,1 (573 K) | 0,42 |
| Sr0,8La0,2F2,2 | F- | 0,11 (573 K) | 0,196 |
| 0,91ZrO2 x 0,09Sc2O3 |
O2- |
30 (1273 K) | 0,43 |
| (Bi2O3)0,8(SrO)0,2 |
O2- |
0,6 (773 K) | 0,8 |
Протоно-проводящие
электролиты твёрдые - в осн. кристаллогидраты твердых орг. и неорг. к-т и их
солей, в к-рых перенос Н осуществляется либо по сетке водородных связей молекул
Н2О (механизм туннельного перехода), либо перемещением иона
гидроксония Н3О+ (прыжковый механизм), либо по молекулам, адсорбир.
на межзеренных границах поликристаллич. материала. Исключение составляют
безводные гидросульфаты и гидроселенаты щелочных металлов (напр., CsHSO4
и CsHSeO4), к-рые приобретают высокую ионную проводимость при т-рах
выше структурного фазового перехода, когда число возможных мест локализации
протонов оказывается вдвое больше числа самих протонов. Обладают протонной
проводимостью и мн. полимерные структуры. Большинство Ag+-проводящих
электролиты твёрдые получают либо выращиванием монокристаллов (![]() -Agl, RbAg4I5), либо
твердофазным синтезом (RbAg4I5, (C5H5NH)Ag5I6 и др.). Для изготовления Li+-,
Na+- и О2- -проводящих электролиты твёрдые используют технологию произ-ва
керамики. Существуют полимерные электролиты твёрдые, к-рые обладают
пластичностью, из них можно изготавливать тонкие пленки толщиной 0,5-250 мкм.
По электропроводности они сравнимы с жидкими и твердыми электролитами (
-Agl, RbAg4I5), либо
твердофазным синтезом (RbAg4I5, (C5H5NH)Ag5I6 и др.). Для изготовления Li+-,
Na+- и О2- -проводящих электролиты твёрдые используют технологию произ-ва
керамики. Существуют полимерные электролиты твёрдые, к-рые обладают
пластичностью, из них можно изготавливать тонкие пленки толщиной 0,5-250 мкм.
По электропроводности они сравнимы с жидкими и твердыми электролитами (![]() 1-10-3 См/м).
Полимерные электролиты твёрдые - как правило, аморфные комплексы полимер-соль
или полимер-к-та на. Получают их из полиэтиленоксида (ПЭО) и др. сходных по
строению полимеров. Ион проводимости определяется природой второго компонента.
При этом ион мигрирует вдоль полимерной цепи благодаря сегментальным движениям
полимерной матрицы. Температурная зависимость проводимости комплексов удовлетворяет
ур-нию, основанному на теории свободного объема:
1-10-3 См/м).
Полимерные электролиты твёрдые - как правило, аморфные комплексы полимер-соль
или полимер-к-та на. Получают их из полиэтиленоксида (ПЭО) и др. сходных по
строению полимеров. Ион проводимости определяется природой второго компонента.
При этом ион мигрирует вдоль полимерной цепи благодаря сегментальным движениям
полимерной матрицы. Температурная зависимость проводимости комплексов удовлетворяет
ур-нию, основанному на теории свободного объема:
![]()
где Т0 - идеальная т-ра стеклования полимера, Т - т-ра системы, В - константа.
В системе ПЭО-Н3РО4
образуется комплекс (ПЭО) Н3РО4 с n =1,33, обладающий
протонной проводимостью ок. 10-3 См/м (298 К). В комплексе ПЭО-NH4НSО4
анионы практически неподвижны и протон переносится катионами![]() (
(![]() 2 x 10-2 См/м). В комплексах
ПЭО-LiС1О4 ток переносится как ионами Li+, так и
2 x 10-2 См/м). В комплексах
ПЭО-LiС1О4 ток переносится как ионами Li+, так и![]() на подвижность к-рых оказывает
влияние неполная диссоциация соли и образование ионных кластеров
на подвижность к-рых оказывает
влияние неполная диссоциация соли и образование ионных кластеров![]() и
и![]() Аморфные структуры со св-вами
электролиты твёрдые существуют и среди неорг. соединений. Это - стекла,
представляющие собой трехмерные сетки, не имеющие строгой периодичности, но
сохраняющие ближний порядок в расположении ионов. Такие структуры типа
Аморфные структуры со св-вами
электролиты твёрдые существуют и среди неорг. соединений. Это - стекла,
представляющие собой трехмерные сетки, не имеющие строгой периодичности, но
сохраняющие ближний порядок в расположении ионов. Такие структуры типа![]() -RbAg4I5
обнаружены в смешанных галогенидных системах AgX-CsX и AgX-CuX-CsX (X = С1, Вr,
I). Используют электролиты твёрдые в химических источниках тока, ионисторах,
хим. сенсорах, в качестве ионселективных мембран, при термодинамич.
исследованиях и др.
-RbAg4I5
обнаружены в смешанных галогенидных системах AgX-CsX и AgX-CuX-CsX (X = С1, Вr,
I). Используют электролиты твёрдые в химических источниках тока, ионисторах,
хим. сенсорах, в качестве ионселективных мембран, при термодинамич.
исследованиях и др.
1. Общие сведения
В последние годы все большее внимание привлекают новые твердотельные ионопроводящие материалы (проводники второго рода) с высокой ионной проводимостью: их называют суперионными проводниками (СИП) или твердыми электролитами (ТЭЛ) (в англоязычной научной литературе — superionic conductors, solid electrolytes или fast ion conductors). Как известно, при нормальных условиях ионный перенос в обычных твердых телах — как кристаллических, так и аморфных — не очень значителен и при комнатной температуре проводимость, σ не превышает 10-10-10-12 Ом-1*см-1 [1].
Поскольку ионная проводимость имеет термоактиваиионный характер, то по мере увеличения температуры величина σ растет, однако даже в окрестности точки плавления она редко превышает 10-3Ом-1*см-1 (здесь не рассматриваются эффекты "предплавления" твердых тел, см., например, [2]). Однако аномально высокая ионная проводимость ТЭЛ наблюдается при температурах, существенно более низких, чем температура их плавления. На рис. 1.1 показана проводимость некоторых СИП в сравнении с обычными ионными кристаллами и жидкими электролитами.
Электропроводность "хороших" ТЭЛ составляет 10-1Ом-1*см-1 (при комнатной температуре!), что по порядку величины близко к проводимости расплавов и концентрированных растворов жидких электролитов. Таким образом, речь идет о материалах, сочетающих свойства жидкостей (проводимость, характерная для расплава или раствора, ионная термоЭДС) и твердых тел (механическая жесткость кристаллов).
Первые упоминания о высокой проводимости ионных кристаллов относятся, по-видимому, к началу XIX в., когда в 1833 г. Фарадей [3] отметил аномально высокую электропроводность сульфида серебра, сравнимую со значениями, σ для металлов. Через год, при исследовании фторида свинца, он обнаружил резкое изменение электропроводности кристалла при 450°С [4]; в настоящее время этот эффект известен как фарадеев (размытый) фазовый переход в кристаллах со структурой флюорита.
Первым оксидным ТЭЛ можно считать керамику состава (масс.%) 85ZrO2-l 5Y203, которую Нернст в 1899 г. использовал в качестве материала для ламп накаливания [5]. В 1914 г. при исследовании йодистого серебра Тубандт и Лоренц [6] обнаружили фазовый переход (при 147°С), в результате которого электропроводность скачком меняется более чем на три порядка, достигая величины 1*10-1*Ом*см-1 с последующим слабым ее повышением вплоть до плавления кристалла. Далее проводимость Agl даже слегка уменьшается (примерно на 7%). Следует отметить работы Каммера и Уэбера (1967 г.) [7,8], которые сообщили об электролитических свойствах глинозема и использовании этого материала в серно-натриевом аккумуляторе. В то же время Брэдли и Грин (и независимо от них) Оуэне и Агью [9,10] синтезировали новый серебропроводящий электролит RbAg4I5,проводимость которого при комнатной температуре долгое время была рекордно высокой (0,35 Ом-1* см-1). В настоящее время известно большое количество ТЭЛ, в которых проводимость обеспечивается самыми различными катионами — одно-, двух- и трехзарядными (Ag+, Cu+, Lн+, Na+, К+, Rb+ Тl+, Cs+, Ca2+, Zn2+, Mg2+, Pb2+,Al3+ Sc3+, Ce3+, Eu3+), а также анионами (F-, Сl-, Вr-, О2-, S2-).
Существуют материалы, где носителями зарядов служат одновременно ионы двух сортов, например, Ag2+ и Hg2+ в Ag2HgI4 или сокатионная проводимость в твердых растворах (N,К)-β-Аl2Оз; возможно, ионы трех сортов (К+, Rb+, Сs+) являются подвижными в системах [0,75(l-x)Rb0.7,К0.3FеО2]0,25ТiО2 [11].
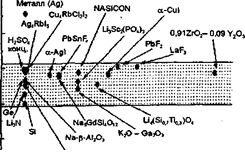
Рис. 1. Электропроводность наиболее интересных ионных проводников в сравнении с жидкими электролитами, полупроводниками, металлами и диэлектриками.
1.1 Основные положения теории дефектов в ионных кристаллах
Сложившиеся к началу XX столетия представления о твердых, телах как о кристаллических решетках, составленных из регулярно повторяющихся структурных единиц, не позволяли объяснить явления переноса вещества и электрического заряда в этих материалах.
Понятие о термических, точечных дефектах впервые было предложено в 1926 г. К.Ч Френкелем при рассмотрении механизма электропроводности ионных кристаллов [12]. При этом предполагалась, что в результате тепловых флуктуации часть катионов покидает свои нормальные места, переходя в междоузлия, образуя равное количество вакансий и "междоузельных катионов данного сорта. Такой тип дефектов впоследствии назвали "дефекты по Френкелю". Галогениды серебра AgCl и АgВr, нитраты щелочных металлов являются примером систем с преобладанием дефектов по Френкелю. Фториды щелочноземельных элементов (ЩЗЭ) обладают антифренкелевскими дефектами, т.е. в них при тепловом равновесии существуют равные количества вакансий анионов фтора и междоузельных анионов фтора. В 1935 г. В. Шоттки показал, что в ионных кристаллах может реализоваться такой предельный случай, когда равное число катионов и анионов уходит из нормальных мест в решетке на поверхность кристалла, создавая катионные и анионные вакансии и сохраняя при этом условие электронейтральности объема кристалла в целом [13]. Преобладающий тип дефектов по Шоттки имеют щелочногалоидные кристаллы.
Теоретически возможно существование антишоттковских дефектов равное количество катионов и анионов в междоузельных положениях, однако они пока не обнаружены ни в одной реальной кристаллической структуре.
Анализ большого числа стехиометрических ионных кристаллов позволяет сделать вывод, что наиболее распространенным типом разупорядоченности являются дефекты по Шоттки. Существование неконтролируемых примесных ионов или примеси (область малых концентраций), специально введенной в кристаллические объекты при легировании их в процессе выращивания, является также распространенным типом точечных дефектов.
Точечные дефекты термодинамически обратимы, поскольку их концентрация в твердом теле зависит от температуры и давления. Эти дефекты зачастую могут легко двигаться в кристалле посредством скачков атомов или ионов в междоузлиях либо в результате миграции вакансий, что эквивалентно смещению структурных элементов в направлении, обратному тому, в котором диффундируют дефекты. Очевидно, что явление переноса вещества тесно связано с существованием дефектов.
Теория точечных дефектов одна из наиболее важных частей современной физической химии и физики твердого тела. Наличие точечных дефектов во многом определяет физико-химические свойства твердого тела, такие, как электропроводность ионных кристаллов, их оптические и полупроводниковые свойства, каталитическую активность, реакционную способность твердых тел и т.д.
Теория дефектов дает возможность количественно интерпретировать все физико-химические явления, связанные с существованием точечных дефектов в кристаллических твердых телах. Здесь рассмотрим лишь главные принципиальные концепции теории дефектов, которые, прежде всего, связаны с процессами переноса вещества в твердых телах. Основные положения теории дефектов были разработаны Френкелем, Иостом, Вагнером, Шоттки [12-15]. Затем эта теория была развита Хауффе, Вервеем и Лидьярдом, давшим возможность объяснить эффект влияния примесей на характер и степень разупорядоченности ионных кристаллических решеток [1, 16]. В 60-е годы значительный вклад в теорию точечных дефектов был сделан Крегером и Винком [17]. Впоследствии были обнаружены существенные ограничения в области применения термодинамической теории, так как стало известно, что структура дефектов в кристаллах с большой степенью отклонения от стехиометрии либо при повышенных концентрациях второй компоненты в смешанных кристаллах, как правило, более сложная, чем та, которая предполагается классической теорией точечных дефектов.
Однако необходимо подчеркнуть, что в большинстве случаев концентрация точечных дефектов даже при очень высоких температурах не превышает предельного значения. Это имеет место в случае галидов, сульфидов, оксидов металлов основных групп периодической системы, а также применимо к значительному количеству оксидов переходных металлов. Потому теория точечных дефектов является важной и постоянно развивающейся основой интерпретации экспериментальных результатов при изучении многих физнко-химических свойств твердых тел. В первом приближении можно ограничиться случаем невзаимодействующих дефектов, а затем учесть дальнодействуюшее кулоновское взаимодействие.
1.2 Основные положения физики и химии суперионных материалов
1.2.1 Структурные особенности
С известной степенью условности к СИП относятся соединения с проводимостью выше 10-3 Ом-1см-1 и (что не менее важно) низкими энергиями активации, Ea < 0,4 эВ. Такие высокие значения электропроводности обусловлены во многом особенностями атомного строения рассматриваемых материалов, а точнее, особым (зачастую уникальным) характером разупорядочення одной или нескольких подрешеток кристалла (ионных подсистем).
Развитые ранее классические представления о природе и механизмах ионной проводимости не могут объяснить столь высокие значения проводимости или коэффициента диффузии, реализуемые в ТЭЛ. Действительно, из уравнения (10) следует, что для обеспечения высокой проводимости желательно участие максимально возможного числа ионов (высокая концентрация носителей я) с наибольшей подвижностью и. Это означает, что коваленткые связи в кристалле должны быть слабыми. Качественное рассмотрение данной проблемы позволяет сформулировать дополнительные условия существования суперионной проводимости, основанные на структурных особенностях материала [20,21]:
Энергетически эквивалентных кристаллографических позиций (в элементарной ячейке) для размещения потенциально подвижных ионов должно быть больше, чем самих ионов.
Энергия разупорядочення ионов по позициям и энергия, затрачиваемая на движение, должны быть малыми. Энергетические барьеры между соседними позициями должны быть небольшими (в cравнении с кТ), что в случае выполнения первого условия приведет к статистическому распределению мобильных ионов по "разрешенным" решеточным позициям.
Необходимо существование связной сетки "каналов" для движения ионов, в противном случае быстрым будет лишь "локальное" движение частиц (в пределах одной или нескольких элементарных ячеек).
Все ТЭЛ можно разделить на несколько типов в соответствии с величиной ионной проводимости и особенностями кристаллического строения. К настоящему времени обнаружено и изучено значительное (см. гл. IV) количество кристаллов с собственным структурным разупорядочением, причем число их непрерывно возрастает. Наиболее ярким представителем ТЭЛ со структурным разупорядочением является соединение, RbAg4I5 проводимость которого, осуществляемая разупорядоченными катионами Ag+, при комнатной температуре составляет 0,35 0м-1*см-1 (для сравнения заметим, что эта величина более чем на 16 порядков превышает ионную проводимость поваренной соли при той же температуре).
Другой тип суперионных материалов представляют вещества, высокая ионная проводимость которых обусловлена большой концентрацией гетеровалентных примесных ионов, активирующих разупорядочение структуры. Например, если в решетку CaF2 вводится дополнительно LaF3, то ионы La3+ встраиваются в подрешетку Са+2. Однако ввиду различия зарядов Са+2 и La*3 в таком смешанном кристалле (твердом растворе) для того, чтобы компенсировать избыточный заряд ионов лантана, возникает избыток анионов фтора, что и приводит к разупорядочению фторной порешетки. Если удается создать материалы с большим отклонением от стехиометрии (сильно нестехиометрические гетеровалентные твердые растворы), т.е. с высокой концентрацией избыточных ионов F-, то в них будет наблюдаться значительная ионная проводимость. Так, электропроводность нестехиометрической фазы Sr1-xLaxF2+x при х = 0,3 на 6 порядков превышает σ чистой матрицы SrF2 [23], а в тисонитоподобных кристаллах LaF3 — гетеровалентные изоморфные замещения приводят также к увеличению σ на 3-4 порядка [24]. Описанные выше системы называются примесными твердыми электролитами или твердыми электролитами с примесной разупорядоченностью. Примерами примесных ТЭЛ могут служить также твердые растворы вида МО2-МОx, где М = Zr, Hf, Ce; М' = У, Са. Их ионная проводимость, осуществляемая анионами кислорода, составляет 1-10 Ом-1*см-1 при 1000-1500°С.. Среди натрий проводящих материалов укажу твердые растворы Na1+xZr2P3-xSixO12 (NASICON) с проводимостью порядка 1*10-1Ом-1*см-1 при 300 С.
Формально считается, что ионная проводимость обусловлена подвижностью катионов, образующих клатраты в спиралях макромолекул ПЭО либо ППО, и каналами проводимости являются такие спирали. Однако результаты, полученные методами рентгеновского анализа на монокристаллах (ПЭО)4—KSCN, показали отсутствие катионов K+ и анионов внутри спирали ПЭО [28]. В настоящее время принято считать, что подобные комплексы полимеров состоят из трех фаз: кристаллической фазы ПЭО—МХ, кристаллической фазы самого ПЭО и аморфной фазы ПЭО с внедренной солью МХ. Такая композитная аморфная фаза ведет себя как раствор при температурах выше температуры стеклования Tg и обычно ответственна за ионную проводимость
Полимерные ТЭЛ имеют существенные преимущества перед другими ТЭЛ в практическом плане в связи с легкостью получения тонких пленок.
2. Особенности получение материалов
2.1 Физико-химические принципы - основа систематического подхода к созданию суперионных материалов
Одной из важнейших задач ионики твердого тела является создание новых СИП и материалов со смешанным (ионно-электронным) характером проводимости. Потребность в них постоянно растет, и ее нельзя удовлетворить, ограничиваясь лишь полуэмпирическими подходами и классическими методами синтеза. Число различных материалов в ионике твердого тела столь многообразно, что решение этой сложной проблемы возможно лишь в том случае, если исследователи будут опираться на закономерности, вытекающие из общности физико-химической природы разнородных процессов и материалов.
Основные, наиболее важные фундаментальные физико-химические пршщшты, имеющие большое значение при создании суперионных материалов и играющие определяющую роль в целом для развития неорганического материаловедения, сформулированы в работах Ю.Д. Третьякова [29,30]:
1) периодичности свойств неорганических соединений элементов;
2) химического, термодинамического и структурного подобия;
3) непрерывности, соответствия и совместимости компонентов равновесной системы;
4) ограничения числа независимых параметров состояния в равновесной системе;
5) структурного разупорядочения и непостоянства состава, химического, структурного и фазового усложнения системы;
6) химической, гранулометрической и фазовой однородности;
7) неравноценности объемных и поверхностных свойств;
8) метастабильного многообразия физико-химических систем;
9) одинакового эффекта, производимого различными физико-химическими воздействиями.
Частично проиллюстрируем применимость выше перечисленных принципов на примере синтеза наиболее перспективных СИП.
Принцип периодичности хорошо прослеживается на примере керамических ТЭЛ с высокой катионной и анионной проводимостью. В первом случае СИП являются соединения металлов первой группы (Li, Na, К, Rb, Сs, Сu, Ag), а во втором — соединениями наиболее активных неметаллов (F, С1, Вr, I, О,S).
Принципы химического, термодинамического и структурного подобия также широко использовались при создании новых СИП. Так, например, по аналогии с хорошо известным серебропроводящим твердым электролитом RbAg4I5; была сделана попытка получить RbCu4I5 [31]. Но соединение RbCu4I5 не могло быть синтезировано из-за того, что ионный радиус Си+ меньше ионного радиуса Ag+. Для того чтобы получить соответствующую медьсодержащую комплексную соль, потребовалась замена иода на химически подобный хлор (с меньшим ионным радиусом в случае Сl-, чем у I-) В результате был синтезирован наиболее высокопроводящий СИП, имеющий ту же кристаллическую структуру, что и Rb4Cu16I7Cl13
Принцип химического усложнения (легирование или модифицирование исходной матрицы) наиболее часто используется при создании новых СИП с заданными электрофизическими свойствами. При образовании твердых растворов изовалентного или гетеровалентно-го замещения примесные компоненты изменяют концентрацию точечных дефектов и дефектов более сложной природы, влияя тем самым на стурно-чувствительные характеристики [34]. Так, например, электропроводность фторида бария BaF3 увеличивается в 109 раз при легировании его фторидом калия.
Принцип фазового усложнения является основой для создания нового класса композиционных СИП. В большинстве двухфазных композиционных твердоэлектролитных систем проводимость увеличивается в 104-1000 раз [35-40]. Для Lil- Аl203 было найдено, что σ увеличивается в 50 раз при добавлении в Lil оксида алюминия с размером частиц меньше 1 мкм [41], для системы Agl - А1203 наблюдался рост σ при комнатной температуре более чем в 2000 раз [42].
Принцип химической, гранулометрической и фазовой однородности чрезвычайно важен при синтезе СИП с воспроизводимыми физико-химическими свойствами, особенно тех, которые используются в микроминиатюрных твердотельных электрохимических устройствах. При этом необходимо помнить об имеющемся пределе миниатюризации твердофазных систем, поскольку при любой температуре, отличной от абсолютного нуля, химически сложная система неоднородна на микроуровне вне зависимости от того, является ли она равновесной или неравновесной (появление микрогетерогенности в нестехиометрнческих соединениях). Известно также, что в открытых неравновесных системах, постоянно обменивающихся веществом и энергией с окружающей средой, возможно спонтанное образование и развитие сложных упорядоченных структур в результате так называемой диссипативной самоорганизации [43, 44]. Для современного материаловедения представляет также большое значение консервативная самоорганизация, связанная с формированием упорядоченных структур в равновесных или близких к ним условиях супромолекулярные структуры или дендримеры [43].
Необходимые свойства твердофазных материалов могут быть получены в результате различных физических или химических воздействий на исходную матрицу. Хорошо известно, что высокая кислородионная проводимость может быть реализована в кубической модификации Zr02 [45]. Чистая двуокись циркония (Тпл = 2700С) имеет моноклинную структуру при комнатной температуре и тетрагональную при Т ~ 1500°С. Введение в Zr02 10+20% СаО приводит к образованию кубических флюоритоподобных твердых растворов Zr1-xCax-02-x, стабильных вплоть до температуры плавления. Стабилизированная кубическая двуокись циркония может быть получена также при введении в Zr02 других оксидов Y, Mg и некоторых оксидов редкоземельных элементов (РЗЭ). Нейтронное облучение также может привести к переходу тетрагональной модификации Zr02 в кубическую.
Необходимый эффект регулируемого изменения функциональных свойств ТЭЛ может быть получен в результате и других нетрадиционных физико-химических воздействий: взрывных волн, давления, лазерного облучения, вибрации, электрофореза, радиационного облучения.
Принцип неравноценности объемных и поверхностных свойств особенно широко используется при создании керамических наноструктурированных ТЭЛ, в которых очень важна межкристаллитная поверхность — ее протяженность и состав [46,47], а также в традиционных методах получения тонкопленочных материалов и методе химической сборки (атомная послойная эпитаксия) [48].
Один из фундаментальных принципов метастабильного многообразия физико-химических систем создается в современном дизайне перспективных СИП методами "soft chemistry" или "chimie douce" [49]. "Мягкая химия" определяется набором "умеренных" химических операций, позволяющих получить, в частности, новые метастабильные соединения, которые не могут быть реализованы из термодинамически стабильных полиморфных соединении путем структурных преобразований между "материнско-дочерними" фазами. В наборе приемов "мягкой химии" могут быть использованы такие процессы, как интеркаляция и деиитеркаляция, ионный обмен, дегидратация, дегидроксилирование, гидролиз, окисление и восстановление (включая электрохимическое), обработка газовыми смесями и т д.
Система перечисленных выше принципов в настоящее время далека от завершения, но ее использование, тем не менее, дает возможность создать общую методологическую основу контролируемого синтеза твердофазных веществ и материалов с уникальными электрофизическими характеристиками.
2.2 Применение препаративных методов в ионике твердого тела
Соединения ТЭЛ можно получать в различном виде, например порошков, керамики, поликристаллических таблеток, трубок и ампул, пленок различной толщины и, наконец, монокристаллов разных размера и качества. Это определяется как научными целями и практическими задачами, стоящими перед исследователем, так и экспериментальными возможностями, имеющимися, а распоряжении ученых.
Ниже рассмотрим экспериментальные подходы к реализации различных методов получения таких материалов.
Препаративные методы в ионике твердого тела приобретают все более фундаментальное значение, и любые новые разработки в этой области весьма актуальны. В последнее время помимо традиционного твердотельного метода синтеза ТЭЛ применяются современные методы синтеза, использующие золь-гель технологию, криотехнологию, синтез под давлением (ударные волны), ионное наслаивание, химическую сборку и методы синтеза, позволяющие получать наноструктурированные и дисперсные ТЭЛ.
2.2.1 Твердофазный синтез твердых электролитов
Наиболее распространенным методом синтеза ТЭЛ (как и других твердофазных материалов) является твердофазный. Сведения о твердофазных реакциях, используемых в частности и для получения как солевых, так и оксидных ТЭЛ, обобщены в ряде монографий и обзоров [1-10]. В них рассмотрены основы термодинамики и кинетики твердофазных реакций, большое внимание уделено механизмам важнейших твердофазных реакций и проблеме активирования твердых фаз. В силу того, что научные интересы авторов в большей степени связаны с исследованием СИП с преимущественной проводимостью по анионам, основные примеры применения твердофазных методов синтеза будут касаться фтор - и серапроводящихТЭЛ.
Существенным условием при синтезе ТЭЛ на основе фторидов элементов П., III., IV групп периодической системы является предотвращение реакции пирогидролиза, приводящей к образованию оксифторидных фаз. Известно, например, что наличие примеси кислорода во фторидах РЗЭ влияет на температуры полиморфных превращений и плавления [И], в случае же фторидов щелочноземельных металлов (ЩЗМ) приводит к уменьшению параметров кристаллической решетки и понижению плотности, а также значительно сказывается на электрофизических свойствах [12].
Существуют активный и пассивный способы предотвращения реакции пирогидролиза неорганических фторидов [13]. В случае активного способа в качестве фторирующей атмосферы обычно используются фтористый водород, элементарный фтор или продукты пирогидролиза тефлона
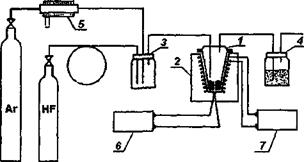
Рис. 2.1. Схема установки для гвдрофторнрования исходных фторидов и продуктов синтеза. 1- платиновый сосуд. 2 — печь; 3 — смеситель газов; 4 —поглотитель; 5 — кислородный насос с датчиком; 6 — контроль температуры; 7—терморегулятор.
2.2.2 Синтезы под высоким давлением
Синтезы под высоким давлением представляют большой интерес, поскольку многие вещества, получаемые в этих условиях, устойчивы или метастабильны при атмосферном давлении и температурах, значительно превышающих комнатную температуру [37, 38]. Для проведения синтезов под высоким статическим давлением применяется различная аппаратура: аппарат Бриджмена, цилиндрическая матрица с поршнем, аппараты типа "белт", тетраэдрический аппарат и другие различные установки для гидротермального синтеза. В типичном синтезе соединения, получаемого при высоком статическом давлении с последующей температурной закалкой, помешенный в капсулу образец доводят до соответствующего давления (до нескольких десятков сотен килобар) и затем повышают температуру. После выдерживания при заданной температуре (обычно несколько минут) образец, находящийся под давлением, подвергают закалке путем понижения температуры со скоростью около 400 градус. После этого снимают давление, которое играет двоякую роль в данном методе синтеза: во-первых, благоприятствует протеканию твердофазной реакции, обеспечивая тесный контакт между частицами реагирующих твердофазных компонент, и, во-вторых, препятствует разложению нестабильных фаз или возгонке летучих соединений.
Упоминавшиеся выше соединения были получены под действием статического давления. Однако возможен синтез ТЭЛ под действием ударного сжатия или ударных волн при использовании взрывчатых веществ, так как в этом случае можно достигнуть давлений на 1-2 порядка величины выше тех значений, которые могут быть реализованы в обычных статических установках высокого давления. Длительность воздействия ударных волн измеряется несколькими микросекундами. Величины развиваемого давления и температуры зависят от геометрии опыта, плотности сжимаемого вещества и скорости распространения в нем ударной волны. При их варьировании ударное давление может изменяться от 10 тысяч до миллионов атмосфер, а температура может меняться от нескольких сотен до десятков тысяч градусов. Первый синтез неорганического соединения при ударном сжатии был осуществлен при получении феррита цинка из смеси соответствующих окислов [43].
Большой интерес представляет синтез смешанных дигалогенидов олова. Обычные методы синтеза, такие, как действие интергалогена ХУ (где X и У — галогены) на металл, совместная кристаллизация из раствора или сплавление SnX2 и SnУ2, привели к образованию смешанных галогенидов SnС10.5Вr1, ClI и SnBrI [44]. Никакое изменение условий синтеза не позволило получить котунитоподобное соединение SnС1Вг. Оно было синтезировано лишь при ударном сжатии смеси хлорида и бромида олова (П). Этими же авторами был получен монобромид меди при ударном сжатии при изучении системы СuВr2 + Си [45], что является примером синтеза соединений с понижением валентности солеобразующего атома. При этом обнаружено, что плотность и диэлектрическая проницаемость у ударно-синтезированного СuВr оказались больше, чем у стандартного образца: р. = 5,26 против 5,06 г/см3 и έ= 17,8 против 10,0. Фазовый переход из структуры сфалерита к вюрциту происходит при Т = 375С вместо 395°С. Параметр кристаллической ячейки у "сжатого" вещества 0,5643 км оказался меньше, чем у стандартного 0,5690 нм. Методом динамического сжатия были получены также твердые растворы КС1 — КВr [46], RbС1 — СsС1 [47], NН4I — CsI [48] и NH4Br —CsBr [49]. В работе [50] был выполнен синтез сложных оксидов на основе ZnО2 под действием ударного сжатия (22 ГПа) и изучена кинетика твердофазных реакций с участием двуокиси циркония.
В последние годы большое внимание уделяется методу механохимических (трибохи-мическнх) реакций, позволяющему получать при комнатных либо умеренных температурах новые метастабильные состояния многих твердофазных материалов, для которых характерны полиморфные превращения [51]. Так, например, данный метод был применен для синтеза тернарных галидов АВ2Х4 (где А = Мg Мn, Zn; В = Li, Na; X = С1, Вr) [52].
2.2.3 Золь-гель технология
Золь-гель технология становится одной из наиболее ведущих для синтеза материалов ионики твердого тела [53-58]. С ее помощью можно получить новые виды тонкой керамики, пленки, оксидные стекла, неоргано-органические композиты, нанокомпозиты с уникальными электрофизическими свойствами. Она включает целый комплекс химических и физико-химических процессов, каждый из которых может существенно влиять на свойства конечных продуктов. Общими признаками процессов приготовления неорганических материалов в золь-гель технологии являются гомогенизация исходных составляющих в виде раствора, их перевод в золь и затем в гель при сохранении гомогенности с последующей сушкой. Стадия золь-гель перехода приводит к формированию неорганической структурной сетки и протекает в жидкости (обычно коллоидном растворе) при низкой температуре. Возникающее твердое тело представляет при этом двух- или многофазный гель [53,59].
Золь-гель технология может быть разделена на две группы различных способов получения "химического геля" (гидролиз и поликонденсация алкоксидов) и "физического геля" (гелирование неорганических золей). Основное различие заключается в исходном сырье: в первом случае — алкоксиды элементов, во втором — неорганические соли. В обоих случаях технология начинается с приготовления растворов, а затем идут операции гидролиза и поликонденсации. Достаточно устойчивый золь требуется готовить только в технологии получения "физического геля", в то время как в случае алкоксидов такая цель не ставится, хотя в какой-то момент образование частиц нанометровых размеров весьма вероятно. В указанных выше двух подходах различаются и свойства геля: образование "физического геля" — процесс, как правило, обратимый, а "химический гель" не поддается последующей пептизации [57].
Как известно, золь-гель технология позволяет получать большое число различных оксидных материалов [53, 54]. В этом случае алкоксиды металлов и неметаллов (общая формула M(OR), где М Si, Al, Ti, V, Cr, Mo, W, Zr и т.д.; R — алкильная группа, в частности СНз, C2H5, С3Н7; n — степень окисления элемента М) подвергаются гидролизу и поликонденсации в растворе при комнатной температуре. Алкоксиды многих элементов являются жидкостями (к примеру, тетраэтоксиксилан Si(OC2H5)4), растворяются в спирте и других органических растворителях. При добавлении воды в спиртовой раствор алкоксида происходит его гидролиз. Это приводит к образованию гидроксилированных М—ОН-групп:
M(OR)n + Н20 - [M(OR)n-1(OH)] + ROH
и мономеров гидроксидов, которые выступают в качестве активных центров в реакции поликонденсации, протекающей, по всей видимости, по механизму алкоксилирования:
М—ОН + М—ОХ - " М—О—М + ХОН (X - Н либо R).
![]()
Реакции гидролиза и поликонденсации алкоксидов, как правило, протекают одновременно, что и приводит к формированию димеров и затем более сложных структур. Трехмерная сетка геля строится из очень мелких частиц размером 3-4 им (частицы золя), формируемых из димеров и их ассоциатов [60]. Структура и состав продукта зависят в большей мере от природы атома М и условий протекания процесса (регулирование соотношения Н20 к М—СЖ в реакционной системе и величины рН) [60-62].
Следует заметить, что "золь-гель химия" алкоксидов переходных металлов более сложна, так как атомы переходных металлов имеют не только высокую электрофильность, но и проявляют несколько координационных состояний [63]. Гели могут быть получены также из неорганических солей, но водная химия их осложнена процессами комплексообразования и гидролиза [57]. Сравнение двух вариантов золь-гель технологии показывает, что алкоголят-ный метод обеспечивает более высокую однородность состава материалов на всех стадиях процесса, вплоть до получения конечного продукта. Смешение идет на молекулярном уровне, что чрезвычайно важно при получении смешанных оксидов или других соединений, содержащих два или более металла либо металлы и неметаллы. Этот факт особенно важен при синтезе ТЭЛ на основе гетеровапентных твердых растворов. Синтез же аналогичных материалов другим методом (технология "физического геля" из неорганических солей) становится более сложной задачей, так как для получения золей смешанных оксидов в каждом случае требуется разработка специальных методик. К тому же объединение золей разного состава часто приводит к гетерокоагуляции и другим эффектам, затрудняющим процесс гелирования.
При образовании геля первичные частицы формируют пространственную сетку, в которой иммобилизована жидкая фаза. Механизм гелеобразования достаточно сложный. В ряде работ с позиции фрактальной геометрии обсуждается возможность реализации процесса кластер — кластер диффузионноограниченной агрегации [53, 64].
Гели склонны к упорядочению уже в процессе их старения (рис. 11.2.2). При старении наблюдается продолжение процесса поликонденсации (пока сохраняются группы М—ОН), проявляется синерезис, вызывающий самопроизвольную усадку гель-сфер, выделяется часть жидкости из пор и наступает огрубление пространственной сетки геля за счет процессов растворения и переосаждения вещества, составляющих первичные частицы разных размеров [53]. Результаты старения проявляются существенно на стадии сушки гель-сфер — очень важной операции золь-гель технологии. Сушка сопровождается значительной усадкой, повышением плотности упаковки первичных частиц и понижением удельной поверхности материала. В производстве керамики по золь-гель технологии используются специальные химические агенты, контролирующие высушивание [65]. К ним можно отнести, например, формамид (NH2СНО) и щавелевую кислоту (Н2С2О4). В первом случае получают крупнопористый ксерогель, во втором мелкопористый.
2.2.4 Синтез дисперсных твердых электролитов
Увеличение проводимости ионной соли Lil в результате гетерогенного легирования оксидом алюминия наблюдалось впервые в 1973 г. Лиангом [73]. Это обстоятельство инициировало интенсивные исследования в ионике новых композиционных ТЭЛ и развитие методов их синтеза.
Наиболее распространенным методом синтеза композитов является керамическая технология: компоненты тщательно перемешивают и прогревают смесь при достаточно высокой температуре (как правило, выше температуры плавления ионной соли) в условиях, при которых не происходят, разложение ионной соли и рекристаллизация дисперсной добавки. Этим методом были созданы композиты Lil—А1203 [73-75], AgCl—Al2O3 [76, 77], AgI А120з [78], CuCl—А12Оз [79], KCl—А1203 [80], AgBr—А120з [81], LiBrxH20—А1203 [82], Т1С1-А1203 [83], CaF2—А12Оз [84], SrCI2—AI2O3 [85].Данный метод получил широкое распространение при синтезе и других композитов: Li2S04—А1203 (СеОг, Yb203, У203,Zn202, BaTiOs), RbNO3—А1203, NaCl—AL2O3, KCl—А1203, RbCI—AL2O3, CsCl—А1203 [86], PbCl2— А120з [87]. В ряде работ композиты получали методом осаждения ионной соли на поверхности гетерогенной добавки. Гетерогенный компонент помешали в раствор ионной соли, а затем проводили испарение растворителя. Этот метод применяли для синтеза композитов на основе кристаллогидратов галогенидов лития [80-90]. В работах Дадни [91, 92] композиты создавали пропиткой пористой мембраны, изготовленной из А1203, расплавом хлорида серебра. Подобный метод был использован при синтезе композитов на основе цеолитов [93]. Адаме с сотрудниками [94] получали композиты методом кристаллизации ионной соли из стеклообразной матрицы. При синтезе композитов на основе нитратов щелочных металлов Li(Na,K,Rb,Cs)N03—А1203 применялась механическая обработка смеси исходных веществ в высоконапряженных планетарных мельницах с ускорением шаров 60-90 g [86]. В этом случае были созданы наиболее высокопроводящие композиционные ТЭЛ. Методом ИК-спектроскопии было показано, что при использовании в данном случае механической обработки в мельницах нитраты не разлагались.
Представляет интерес синтез нанокомпозитов LiX—А1203 (X = F-, Сl, Вr, I, Р043, SO42) методом разложения прекурсоров — двойных солей общей формулы LinX-2nAl(OH)*3mH20. Соли были синтезированы из водных растворов по методике, описанной в работах [95, 96]. Композиты образуются при термическом разложении указанных солей при 400.°С в течение 2 ч. Дегидратация соли описывается уравнением LinX-2nAl(OH)*3mH20 -LinX + nА1203 + mH20 и приводит к образованию двухфазного композита, содержащего при X = F-, Сl, Вr и I 50 мол.% А12Оз, при X = S042~ 33,3 мол.% А1203 и при X = Р043 25 мол.% А120з.
Нагаи и Нишино [97, 98] использовали технику электрохимического осаждения соответствующих ТЭЛ в пористых матрицах А120з при синтезе композитов AgI—AgCl—AI2O3. Указанные галогениды серебра осаждались из растворов в микропорах мембраны из А1203. Использование встречной диффузии реагентов AgNO2, с одной стороны, и Nal — с другой. (для синтеза композита Agi—А120з), либо смеси NaCl и Nal (для синтеза композита Agi— AgCl—А1203) позволяет регулировать микроструктуру ТЭЛ в порах. На рис. II 2.3 показан возможный механизм образования осадков ТЭЛ на основе хлорида и иодида серебра в порах AI2O3. Анализ полученного композиционного ТЭЛ показал, что AgC! кристаллизуется в структурном типе поваренной соли, а иодид серебра — в модификации. Композит AgCl— Agi—А1203 имеет более высокие значения ионной проводимости по сравнению с соответствующими величинами для AgCl—А1203 и Agi—А1203 Метод соосаждения с использованием компонент ZrOCI28H20, YCI3 и А1С13 применялся при получении композитов из стабилизированной двуокиси циркония и оксида алюминия [99,100]
2.3 Выращивание монокристаллов суперионных проводников
Выбор методов выращивания монокристаллов СИП зависит от физических и химических характеристик кристаллизуемого вещества. Оптимальные условия получения кристаллов определяются, исходя из фазового состава исходного вещества и его вида (порошок, слиток и т.п.), типа кристаллшапионной атмосферы, вида контейнера, скорости выращивания, характера начальных стадий кристаллизации (спонтанное зарождение или кристаллизация на затравку) и многих других параметров. Методы кристаллизации можно условно разделить на несколько основных групп [1,2]:
выращивание кристаллов в твердой фазе, из растворов, в том числе и раствор-расплавные методики, из растворов и расплавов при повышенных давлениях, из расплавов, из газовой фазы.
Ниже будут рассмотрены основные методы получения монокристаллов, используемые три выращивании суперионных материалов [3].
2.3.1 Выращивание кристаллов в твердой фазе
Для получения новых материалов часто используется метод твердофазных реакций [4]. При отжиге веществ после завершения процесса синтеза происходят процессы рекристаллизации, при которых в материале образуются новые зерна со способными к перемещениям границами. После продолжительной выдержки при температурах несколько ниже точки плавления часть кристаллитов существенно увеличивается в размерах. Описанным выше способом были получены, например, монокристаллы типа NASICON (Na1+xZr2P3-xSixO12 2<x<2.4): отжиг при 1245.°С в течение 4 месяцев приводил к росту кристаллитов размером до 100-300 мкм [5].
2.3.2 Выращивание кристаллов из растворов
Кристаллизация из растворов позволяет получать кристаллы соединения, химический состав которого может отличаться от химического состава исходной жидкой фазы. В зависимости от температуры процесса и химической природы растворителя различают кристаллизацию из низкотемпературных растворов и рост из солевых расплавов (раствор-расгшавные методы). Сразу отметим, что при росте из раствора процессы идут при температурах, значительно меньших температуры плавления, поэтому получаемые кристаллы менее дефектны, чем выращенные из расплава.
Ниже рассмотрим основные методы выращивания кристаллов на примерах получения различных СИП.
При росте кристаллов необходимо создать пересыщение. Это состояние может быть реализовано различными путями, например, локальной добавкой к растворителю таких компонентов, которые понижают растворимость кристаллического вещества, изменением температуры, смешением различных растворов и т.д.
Способы кристаллизации за счет изменения температуры
Пересыщение достигается путем непрерывного изменения (повышения или понижения) температуры во всем объеме кристаллизатора.
Этот способ был использован для получения кристаллов RbAgI; из раствора AgI и Rbl в иоди-стоводородиой кислоте [6]. При правильно подобранных соотношениях компонентов (концентрация катионов Rb* лежит в пределах 17,5—18,5 масс,% от общей концентрации катионов) и добавлении Н3РО4 в раствор (для нейтрализации свободного молекулярного иода) удается получить [6] монокристаллы высокого качества. Кристаллы размером до 1 см с четким октаэдрическим габитусом были выращены в режиме ступенчатого понижения температуры с периодичностью 1° каждые 12 ч.
Рассмотрим способы создания пересыщения с использованием зон с различными температурами' в одной из зон происходит растворение вещества, в другой — рост кристалла.
Для получения кристаллов PyrAg,I6 и Pyr5Ag1gI23 (где Руr= (C5HSNH)+— пиридин-ион) [7] использовали аппаратуру, показанную на рис. II.3.1.
Ростовой кристаллизатор состоял из двух камер, в которых содержался насыщенный раствор AgI и Руr! в 57%-ной иодистоводородной кислоте при разных температурах. Сосуды сообщаются между собой через горизонтальные трубки. В результате циркуляции насыщенный раствор, поступающий из камеры с более низкой температурой Т0, становится пересыщенным в камере с температурой Т1, что и обеспечивает необходимое для роста кристаллов пересыщение. Кристаллы спонтанно росли на стенках сосуда; за несколько недель кристаллы вырастали до 5 мм в длину и 1 мм в поперечнике.
Кристаллизация при постоянной температуре
Пересыщение раствора может достигаться при постоянной температуре за счет испарения раствора, отбора растворителя или разбавления исходного раствора В [8, 9] монокристаллы RbAgI2 были получены кристаллизацией из раствора в ацетоне AgI и Rbl взятых в соотношении от 1 1,3 до I 3,28, при температурах выше 57°С.Поскольку в интервале температур от 57°С до температуры кипения растворимость кристаллов характеризуется отрицательным температурным коэффициентом, то процесс роста можно вести двумя способами за счет увеличения температуры или благодаря созданию пересыщения отбором растворителя В первом случае из-за малого диапазона изменения температуры (Т < 3°С) возникают трудности при выращивании больших кристаллов, поэтому процесс роста кристаллов осуществлялся за счет отбора конденсата в кри-оаллизаторе, показанном на рис II 3 2 В кристаллизатор помещали затравочный кристалл и добивались такой степени пересыщения, при которой скорость роста i раней составляла 0,2-0,3 мм/сут Для получения качественных кристаллов точность поддержания температуры должна быть не менее 0 1°, чтобы не происходил захват маточного раствораВыращивание кристаллов AgI из водных растворов основывается на особенностях системы Agl—Kl (или HI)—Н2О Йодистое серебро хорошо растворяется в водных растворах KI или HI. его Раствсримость быстро растет по мере увеличения концентрации растворителя [9]
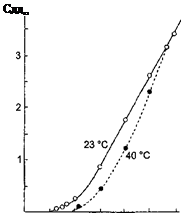
Рис 3.3.1 Кривые растворимости AgI в концентрированном растворе Кl
Разбавление достигалось несколькими способами:
а) добавлением воды, медленно поступающей сверху через стеклянную трубку в ростовую камеру, содержащую насыщенный при комнатной температуре раствор Agi в KI [9,10];
б) поступлением воды из паровой фазы, образующейся при испарении Н;0 в соседнем сосуде [11], в) принудительной подачей воды снизу в ростовую камеру через специальные мембраны [12] Указанные методики позволили получить монокристаллические образцы |3-фазы Agi размерами до 20 мм в длину и несколько миллиметров в поперечнике.
2.3.3 Раствор-расплавные методики
При кристаллизации из растворов в расплавах особое значение имеет знание фазовой диаграммы участвующих компонентов, поскольку в этом случае можно установить параметры кристаллизации, прежде всего температурный режим. Так как система расплавленных солей одновременно может содержать нейтральные молекулы, простые и комплексные ионы, то при понижении температуры в системе возможно образование эвтектик, твердых растворов или соединений.
Если в качестве растворителя используются расплавы, то растворитель и растворяемое вещество в расплавленном состоянии должны обладать полной смесимостью, но не должны образовывать твердый раствор. Наиболее пригоден растворитель, дающий с растворяемым веществом эвтектику с высоким содержанием растворителя.
Для осуществления процесса кристаллизации в расплавах солей в качестве растворителя лучше выбирать расплавы, удовлетворяющие следующим требованиям: 1) растворитель легкодоступное химически чистое вещество; 2) растворяемое вещество имеет большой положительный температурный коэффициент растворимости; 3) растворимость вещества конгруэнтна, т.е. внутри системы не протекают химические реакции; 4) низкая упругость пара при рабочих температурах; 5) небольшая вязкость расплава; 6) невысокая агрессивность относительно материала тигля; 7) легкая растворимость растворителя в воде.
Уменьшить влияние примесей удается использованием растворителей, имеющих общие атомы с выращиваемым соединением. Для выращивания кристаллов с целью понижения рабочей температуры роста необходимо, чтобы точка плавления растворителя была как можно ниже точки плавления растворяемого вещества. В качестве растворителя применяют и смесь солей, но в этом случае образование комплексов или соединений осложняет подбор условий выращивания. При выращивании кристаллов из растворов в расплавах разумно использовать затравочные кристаллы, что ограничивает число растущих кристаллов, а рост происходит в нужной области наиболее благоприятных пересыщений.
Необходимо учитывать, что при росте кристаллов может произойти захват части растворителя (маточного раствора), особенно если осуществляется изоморфное вхождение элементов растворителя в решетку выращиваемого вещества. Для исключения этого размерные параметры компонентов должны сильно отличаться или растворитель и растворяемое вещество должны обладать общими составными частями. Экспериментальные трудности кристаллизации из растворов в расплавах определяются агрессивностью участников реакции, величиной температуры кристаллизации и точностью ее поддержания.
При кристаллизации в изотермических условиях для роста кристаллов создается локальный температурный градиент, что влечет за собой возникновение в области фисталлтоации высокого пересыщения. Алпаратурно это достигается применением охлаждаемого стержня.
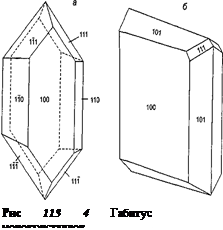
Раствор-расплавный метод широко используется для получения кристаллов ТЭЛ. Рассмотрим в качестве примера рост кристаллов литийпроводящих материалов Li3М2(Р04)3 (где М = Fe, Sc) [В, 14]. В качестве растворителя использовали смесь LiF—V205, причем фторид лития здесь является и растворителем, и источником ионов Li+ для кристаллизуемого соединения. Локализация зародышеобразования происходила на вращающемся платиновом стержне, диаметром 6 мм при средней скорости охлаждения системы 0,5 град./ч. Темперарный интервал кристаллизации составлял 800-650°С.. Исследование фазообразования в - хтемах М205—NH4НзР04—LiF-—\/205 позволило определить температурные области устойчивости фосфатов заданных составов и найти условия монофазной кристаллизации сочинений Li2М2(Р04)з Габитус кристаллов существенно зависит от условий кристаллизации в частности, от скорости охлаждения системы) и концентрации кристаллообразующих компонентов призматические кристаллы формируются при более низких концентрациях и чалых скоростях охлаждения, а пластинчатые — при более высоких концентрациях и больших скоростях охлаждения
2.3.4 Электролитическое осаждение
При электрокристаллизации из растворов или расплавов возникновение новой фазы на поверхности электрода происходит из более или менее сольватированных или комплексных ионов, находящихся в растворе (расплаве) В электрическом поле катионы (или анионы), нейтрализуясь, переходят из электролитической фазы на катод или анод. При этом процесс кристаллизации протекает в окружении посторонних катионов, анионов, нейтральных молекул или диполей растворителя электролитического раствора.
Например, монокристаллы β-AgI были выращены достаточно редко встречающимся методом электрокристаллизации. При пропускании тока 50 мкА через ячейку Аg/AgI/2IPy (где Ру — пирен) в течение 2-3 месяцев на границе Аg/AgI/2IPy образовывались кристаллы β-AgI в виде гексагональных пластинок или пирамид размером до 10 мкм. Пластинки и пирамиды ориентированы осью [0001] перпендикулярно направлению пропускания тока [15].
2.3.5 Гидротермальный синтез
Одним из путей повышения растворимости исходных компонентов служит повышение температуры раствора. Гидротермальная кристаллизация — это рост кристаллов из водных растворов при температурах выше 100°С и давлениях выше атмосферного. Существенной особенностью гидротермального выращивания кристаллов является применение минерализатора (или растворителя), вводимого в систему А—Н20 для увеличения растворимости труднорастворимого компонента А., Таким образом, за счет высоких температур, давлений и введения минерализатора можно перевести в растворенное состояние кристаллизуемое вещество, обеспечить необходимое пресыщение раствора и провести кристаллизацию исследуемого соединения.
К недостаткам метода следует отнести трудность, а зачастую и невозможность прямого наблюдения процессов, происходящих в закрытых автоклавах. Экспериментатор вынужден точно прогнозировать опыт и реконструировать процесс роста путем исследования продуктов реакции в охлажденном состоянии и при отсутствии давления.
Требованиям гидротермального способа удовлетворяют автоклавы, изготовленные из специальных сталей, с внутренними вкладышами из платины, тефлона или других шелоче - (кислото) - стойких материалов.
2.З.6 Выращивание из расплавов
Кристаллизацию из расплавов можно рассматривать как рост кристаллов растворителя, при котором растворенный компонент, например примесь, остается в растворе, а чистый растворитель выкристаллизовывается. Из расплава можно выращивать кристаллы только таких веществ, которые не только плавятся без разложения, но и выдерживают перегрев.
Различают методы выращивания кристаллов в тиглях и без использования тиглей. Преимуществом первых по сравнению со вторыми является большая простота технологии. Кроме того, такие способы дают возможность получать кристаллы относительно сложной грмы (в том числе профилированные). К недостаткам тигельных методов надо отнести пличные виды взаимодействия расплава с тиглем, что сказывается на качестве кристаллов Тигельные методы разбиваются на группы с неподвижным тиглем и с перемещением тигля или печей.
3. Твёрдые полимерные электролиты: структура, свойства и применение
3.1 Введение
Электролиты вообще и твёрдые полимерные электролиты в частности нельзя рассматривать отдельно от электрохимической системы, компонентом которой является электролит. Поэтому начнём с определения некоторых основных электрохимических понятий.
Электрохимию можно определить как часть химии, изучающую превращения веществ на границе раздела проводник электричества первого рода (электронный проводник) — проводник электричества второго рода (ионный проводник), происходящие с участием свободных электронов. Система, состоящая из двух проводников первого рода и находящегося с ними в контакте проводника второго рода, в которой могут протекать как минимум одна электрохимическая реакция окисления и одна электрохимическая реакция восстановления вещества, называется электрохимической системой. Составные части электрохимической системы имеют следующие названия. Электронный проводник, находящийся в контакте с ионным проводником, называется электродом. Электрод, на котором идёт электрохимическая реакция восстановления, называется катодом; электрод, на котором идёт электрохимическая реакция окисления, анодом. Ионопроводящую среду в электрохимической системе называют электролитом. Вещество, участвующее в окислительно-восстановительных реакциях на электродах, называется электроактивным веществом (ЭАВ).
3.2 Твердый электролит
Чаще всего понятие "электролит" относят к жидким растворам и расплавам веществ, хотя давно известны многие твёрдые вещества, обладающие ионной проводимостью. Твёрдыми полимерными электролитами (ТПЭ) называют вещества, имеющие полимерное строение, причём в состав полимеров входят функциональные группы, способные к диссоциации с образованием катионов или анионов, направленное движение которых, внутри структуры полимера обусловливает его ионную проводимость. В качестве примера приведены формулы двух наиболее широко известных представителей ТПЭ.
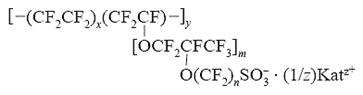
"Nafion" (x = 5–113; y = 1000; m = 0–33; n = 2–66)
"Nafion" представляет собой фторуглеродный полимер, содержащий функциональные сульфогруппы, способные к обмену с внешней средой электростатически связанными катионами К. Ионная проводимость этого ТПЭ обусловлена движением катионов, поэтому подобные электролиты получили название катионных или (по аналогии с ионообменными смолами) катионообменных.
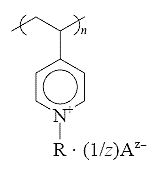
Поли (винилпридин)
Второй ТПЭ — поли (винилпиридин) состоит из углеводородных полимерных цепей, имеющих функциональные пиридиновые группы, способные электростатически или координационное связывать анионы А. Электропроводность данного электролита обусловлена движением анионов, поэтому его относят к группе анионных или анионообменных. Из-за уникальных качеств (устойчивость, высокая электропроводность, прочность) широкое распространение получили только фторуглеродные катионные ТПЭ, поэтому в дальнейшем свойства и применение полимерных электролитов будем рассматривать на их примере.
В 1964 году американская фирма "Дюпон" ("Du Pont") запатентовала способ получения фторуглеродных виниловых эфиров, содержащих сульфогруппы, полимеризацией которых в водной среде с использованием пероксида водорода в качестве инициатора и были получены первые полимерные мембраны, широко известные под торговой маркой "Nafion". Позднее аналогичные ТПЭ стали выпускаться и в России под названием МФ-4СК. Первые в мире промышленные установки с применением мембран "Nafion" запущены в Японии в 1975–1976 годах. В 70-е годы были начаты широкие научные исследования свойств этих полимерных электролитов, главным образом механизма их проводимости.
3.3 Свойства ТПЭ "Nafion"
Внешне мембрана "Nafion" представляет собой оптически прозрачные в видимой части спектра листы толщиной от 0,1 до 1 мм. Вследствие инертности своей фторуглеродной основы этот ТПЭ чрезвычайно устойчив к химическим воздействиям (выдерживает кипячение в концентрированной азотной кислоте), механически прочен и термически устойчив (до 100°С). Обычно он выпускается в протонированной или натриевой форме (K = H + или Na + соответственно). Эквивалентная масса "Nafion" составляет от 900 до 1200 г в расчёте на эквивалент сульфогрупп.
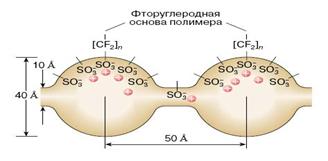
Рис. 1. Внутренняя структура ТПЭ "Nafion"
Исследования внутреннего строения ТПЭ "Nafion" показали, что он имеет двухфазную структуру (рис. 1). Основа полимера (гидрофобная фаза) состоит из фторуглеродных и эфирных цепей, расположенных в пространстве таким образом, что функциональные сульфогруппы группируются внутри сферических полостей диаметром порядка 40 Å. Система связанных узкими каналами полостей, содержащих гидратированные катионы, представляет собой вторую, гидрофильную фазу мембраны.
Перенос заряда в ТПЭ осуществляется в простейшем случае за счёт перехода катионов с одной сульфогруппы на другую. Специальными исследованиями было установлено, что небольшие по размеру катионы могут легко переходить из одной полости в другую, тогда как движение анионов через узкие каналы затруднено из-за отталкивания от одноимённо заряженных функциональных групп. Это свойство определяет возможность использования "Nafion" как ион-селективных мембран, способных пропускать одни ионы и задерживать другие.
Главной особенностью "Nafion" является её чрезвычайно высокая ионная проводимость. Величину проводимости ТПЭ или, другими словами, скорость транспорта заряда через них принято оценивать через коэффициент диффузии заряженных частиц (коэффициент диффузии заряда) D (см 2/c). Коэффициент диффузии ионов Na + в мембране "Nafion" составляет около 1·10 –6 см 2/c, что сравнимо с коэффициентом диффузии этих ионов в концентрированном водном растворе хлорида натрия.
Рассматриваемые полимеры, подобно ионообменным смолам, способны обменивать входящие в их состав катионы на катионы внешней среды. Методом ионного обмена в ТПЭ можно внедрять как простые, так и достаточно крупные комплексные катионы типа [Ru(bipy)3] 2+ , где bipy = 2,2'-бипиридин. При этом концентрация катионов в мембране может превышать предельно возможную концентрацию данных катионов в растворе. Так, после выдерживания мембраны в водном растворе, содержащем 10 –3 моля [Ru(bipy)3] 2+ на литр, концентрация этих ионов в ТПЭ может быть в 500–700 раз больше. Причём внедрённые комплексные катионы прочно удерживаются мембраной: уменьшения концентрации комплекса не было обнаружено даже после промывки мембраны в проточной воде в течение нескольких дней.
Полимеры с эквивалентной массой 900–1000 г/экв могут медленно растворяться в этаноле или диметилформамиде. Это свойство является весьма важным, поскольку даёт возможность получать на поверхности электродов различных электрохимических систем тонкие плёнки ТПЭ путём нанесения раствора и выпаривания растворителя при небольшом нагревании. Такие электроды с тонким слоем ТПЭ на поверхности и введённым в полимер для придания электроду каких-либо специфических свойств ЭАВ называют полимерными электродами. Они, в свою очередь, относятся к классу химически модифицированных электродов (ХМЭ). Химически модифицированными называют электроды, на поверхность которых нанесены молекулярно организованные химические системы, предназначенные для целенаправленного изменения электрохимических, каталитических или оптических свойств электрода.
Краткое рассмотрение свойств ТПЭ "Nafion" позволяет выделить основные направления его практического использования (рис. 2).
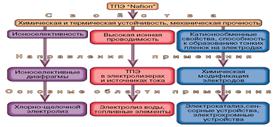
Рис. 2. Свойства и основные области применения ТПЭ "Nafion"
3.4 Электрохимическое получение хлора и гидроксида натрия
Хлор является важнейшим химическим продуктом, используемым для получения полимерных материалов, пестицидов, тканей. Его получают в настоящее время практически исключительно путем электролиза водного раствора хлорида натрия.
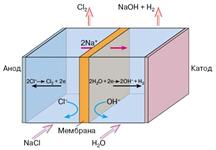
Рис. 3. Схема электрохимического синтеза хлора и гидроксида натрия с применением ТПЭ "Nafion"
Как показано на схеме процесса (рис. 3), на катоде (обычно сделанном из стали) происходит выделение водорода и образование гидроксильных ионов, дающих с находящимися в растворе ионами натрия гидроксид натрия. На аноде хлоридные анионы окисляются до молекулярного хлора. Этот процесс катализируется материалом анода, поверхность которого покрыта смесью оксидов титана и рутения (IV). При отсутствии разделительной диафрагмы гидроксильные ионы могут попадать из катодного пространства в анодное и взаимодействовать с хлором:
Cl2 + 2OH – → ClO – + Cl – + H2O
Кроме того, гипохлорит-ионы могут далее окисляться по реакции
6ClO – + 3H2O → 2ClO3 – + 4Cl – + 6H + + 1,5O2 + 6e –
Оба приведённых побочных процесса приводят к загрязнению щёлочи хлоратом натрия и появлению примеси кислорода в хлоре, резкому уменьшению выхода по току (показатель, характеризующий эффективность электрохимического процесса). Таким образом, присутствие разделительной мембраны, предотвращающей смешивание продуктов анодной и катодной реакций, является необходимым условием эффективного ведения процесса в целом. Мембрана должна соответствовать следующим требованиям:
— хорошо пропускать ионы Na +, но быть непроницаемой для ионов Cl – и OH — быть химически стабильной в высокоагрессивной среде (щелочной раствор хлорида натрия 6 моль/л при температуре 80–95&ddeg;С) в течение длительного времени;— иметь высокую электрическую проводимость; — быть механически прочной.
Эти требования были выполнены в полной мере только после появления мембран "Nafion", установки, на основе которых занимают в настоящее время, лидирующее положение в области хлорно-щелочного электролиза.
3.5 Кислородно-водородные генераторы и топливные элементы
Появление фторуглеродных катионообменных мембран произвело настоящую революцию в таких областях, как электролиз воды для получения водорода и кислорода и преобразование химической энергии в электрическую с помощью топливных элементов. Обе области науки и техники взаимосвязаны и являются необходимыми компонентами так называемой водородной энергетики. Суть последней состоит в преимущественном использовании водорода как экологически чистого и экономически выгодного энергоносителя. Действительно, водород может быть получен с помощью электролиза воды принципиально экологически чистого процесса. Наиболее выгодно делать это в периоды наименьшей внешней загрузки электростанций. Далее, по существующим подсчётам, транспортировка водорода по системе трубопроводов обойдётся в пять раз дешевле передачи электрической энергии по высоковольтным линиям. У конечного потребителя водород может быть использован непосредственно как экологически чистый химический реагент (топливо, восстановитель) или для получения электрической энергии в топливных элементах. Использование водорода как энергоносителя поможет, таким образом, уменьшить расход углеводородного топлива и приведёт к уменьшению выбросов углекислого газа в атмосферу. Однако для реального внедрения концепции водородной энергетики необходимо решить несколько проблем, одной из которых является повышение эффективности электрохимического получения водорода и обратного преобразования химической энергии в электрическую. Как было отмечено, большую роль здесь сыграло появление мембраны "Nafion", которая в рассматриваемых системах является не только ион-селективной диафрагмой, но и действительно твёрдым полимерным электролитом. Принцип работы твёрдополимерного электролизёра может быть пояснён с помощью рис. 4.
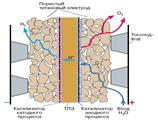
Рис.4. Схема твёрдополимерного электрохимического генератора водорода и кислорода.
Дистиллированная вода подаётся в анодное пространство электролизёра и проникает через поры анода (пластина из пористого титана) к границе раздела электрод/ТПЭ. На этой границе происходит электроокисление воды с выделением кислорода: 2H2O + 4e – → O2 + 4H +
Кислород удаляется из реакционной зоны через поры электрода, газонепроницаемость ТПЭ препятствует проникновению его в катодное пространство и образованию взрывоопасной гремучей смеси. По описанному выше механизму гидратированные протоны движутся через мембрану к катоду, где происходит их восстановление с выделением газообразного водорода: 2H + + 2e → H2
Подобно кислороду, водород удаляют через систему пор катода и каналы токоподвода. Протекание катодной и анодной реакций стимулируется введением на границы раздела электроды/ТПЭ катализаторов — мелкодисперсных платины и оксида иридия (IV) соответственно, причём разработанные к настоящему времени технологии позволяют уменьшить количества применяемых благородных металлов до 0,1 мг в расчёте на квадратный сантиметр поверхности электрода. Некоторые количественные характеристики твёрдополимерных электролизеров, демонстрирующие их эффективность, таковы:
— напряжение на электродах 1,6–1,8 В при номинальной плотности тока 1 А на квадратный сантиметр геометрической поверхности электродов; — толщина ТПЭ 0,2–0,5 мм, толщина всей электролизной ячейки не превышает нескольких миллиметров;
— практически стопроцентная чистота выделяющихся газов, что позволяет применять их как чистые химические реагенты и в медицинских целях (кислород).
Очевидно, что как с экологической точки зрения, так и с точки зрения экономической эффективности электролизёры с ТПЭ не идут ни в какое сравнение с генераторами водорода и кислорода, использующими в качестве электролитов жидкие растворы щелочей. Уже то обстоятельство, что работают твёрдополимерные электролизёры на дистиллированной воде (причём, чем чище вода, тем больше срок службы ТПЭ), говорит об их экологической чистоте. И последний пример: электролизёр размером со спичечную коробку в течение последних 10 лет без всякой замены электродов или ТПЭ обеспечивает все потребности кафедры, на которой работает автор этой статьи, в кислороде и водороде для препаративных работ. Разумеется, этим примером не исчерпываются области применения твёрдополимерных генераторов кислорода и водорода. Их успешно используют в течение последнего десятилетия в медицине. Они вытеснили тяжёлые и пожароопасные кислородные баллоны, нашли широкое применение в промышленности (водород используют в качестве восстановителя, оба газа — в сварочных аппаратах), в энергетике и даже бытовых условиях — для повышения концентрации кислорода в воздухе помещений, что необходимо для лёгочных больных, заполнения кислородных подушек и т. д.. Готовыми к широкому применению (экономичными, безопасными, необслуживаемыми), водород-кислородные электролизёры сделало именно использование твёрдых полимерных электролитов.
Конструкция водород-кислородных топливных элементов с ТПЭ принципиально не отличается от схемы электролизёра. Топливом здесь служат газообразные водород и кислород, реакции на электродах протекают в обратном направлении по сравнению с реакциями при электролизе, продуктами же являются дистиллированная вода и электрическая энергия. Существуют лишь различия в составе каталитических слоёв на границах раздела электроды/ТПЭ и конструкции электродов. Однако КПД топливных элементов с ТПЭ, известных к настоящему времени, не превышает 50%, а напряжение составляет лишь 0,8 В. Это вызвано в первую очередь низкой эффективностью протекания реакции электровосстановления кислорода при сравнительно низких температурах (80–90°С) функционирования данных устройств. Серьёзным препятствием на пути широкого распространения топливных элементов является также высокая цена получаемой с их помощью электроэнергии — от 3 до 8 тыс. долларов за 1 кВт. Тем не менее, топливные элементы с ТПЭ вследствие своих уникальных качеств (безопасности, экологической чистоты и компактности) нашли применение на подводных и космических кораблях, где их используют для получения пресной воды и электрической энергии.
3.6 Химическая модификация электродов с помощью ТПЭ
Суть химической модификации электродов, сравнительно нового направления электрохимии, можно пояснить на следующем примере. Предположим, что необходимо провести реакцию электрохимического восстановления вещества Ox: Ox + e – → Red. Однако данная реакция на известных электродных материалах (реальный выбор которых, кстати, невелик) протекает с низкой скоростью. Выход известен — подбор катализатора, повышающего скорость реакции и иммобилизация его в реакционной зоне, то есть на границе раздела электрод/электролит. Собственно, одной из основных задач химической модификации электродных поверхностей и является организация эффективного протекания электрохимических процессов с помощью катализаторов, находящихся в модифицирующем слое.
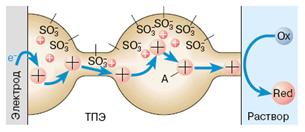
Рис. 5. Схема химически модифицированного электрода с ТПЭ и внедрённым в него электроактивным веществом А.
Предположим далее, что такой катализатор найден — некое вещество А (рис. 5). Нанесём слой ТПЭ на поверхность электрода и методом ионного обмена внедрим в него катализатор, заместив часть катионов натрия, находящихся в мембране. В этом случае реакция восстановления вещества Ox будет протекать не на поверхности электрода, а на границе раздела ТПЭ/раствор: Ox + A → Red + A +. Катализатор возвращается в исходную форму, восстанавливаясь на электроде: А + + е – → A. Однако для этого катион А + должен переместиться через слой полимера к электроду и, восстановившись, вернуться обратно к границе раздела полимер/раствор.
Механизм переноса заряженных частиц или просто заряда через слой полимера является ключевым вопросом, определяющим функционирование химически модифицированных электродов. Скорость переноса заряда часто определяет скорость электрохимических и каталитических процессов с участием ХМЭ, именно поэтому процессы переноса заряда в полимерах были и являются предметом многочисленных исследований.
В рассматриваемом примере катион А+ может достичь поверхности электрода по двум механизмам, первым из которых является физическая диффузия. Движущей силой диффузии является градиент концентрации А+ в ТПЭ в направлении, перпендикулярном поверхности электрода. Этот градиент возникает вследствие уменьшения концентрации А+ у поверхности электрода из-за электрохимического восстановления ЭАВ. Однако физическая диффузия практически всех катионов (за исключением H + и Na +) в ТПЭ "Nafion" протекает медленно, скорость движения резко падает с увеличением размера и заряда ионов. Скорость диффузии комплексных катионов в "Nafion" обычно характеризуется низкими коэффициентами диффузии в диапазоне 10–11 —10–13 см 2/с. Низкая скорость транспорта заряда делает малоэффективным и весь процесс на ХМЭ в целом.
Альтернативным механизмом, позволяющим А+ из глубины мембраны "достичь" поверхности электрода, является обмен электроном между близлежащими молекулами вещества А: A+ + А → А + A+. Восстановившись на электроде, ближайшая к нему молекула восстанавливает соседнюю и т. д. до границы раздела полимер/раствор. Разумеется, это возможно только в том случае, если расстояние между молекулами А в ТПЭ достаточно мало для переноса электрона, то есть концентрация А достаточно велика.
Относительный вклад переноса электрона (электронной проводимости) и диффузии в общий процесс переноса заряда в электрохимических системах, содержащих растворы электролитов, был рассмотрен Дамсом (H. Dahms) и Раффом (I. Ruff) в конце 70-х — начале 80-х годов. Аналогичная теоретическая модель переноса заряда была несколько позднее развита и для ТПЭ. Скорость процесса переноса заряда в рамках рассматриваемой модели может быть выражена через коэффициент диффузии заряда Dct , состоящий из двух слагаемых:
Dct = D + kδ 2 πCA/4,где D — коэффициент реальной диффузии вещества А в полимере, k — константа скорости процесса обмена электроном, л·моль –1 ·с –1,СА — концентрация вещества А в полимере, δ — расстояние между редокс-центрами, на которое переносится электрон.
Относительный вклад обеих составляющих транспорта заряда можно показать на следующих примерах. Так, в растворах электролитов при СА = 0,1М, δ = 10 –7 см, k = 10 9 см 3 ·моль –1 ·с –1 вклад электронного переноса составляет 8·10 –9 см 2 ·с –1. Эта величина значительно меньше коэффициентов физической диффузии веществ, обычно наблюдаемых в водных растворах ~10 –6 см 2 ·с –1. Иначе говоря, вклад электронного переноса в общий процесс переноса заряда в водных растворах незначителен. Дело обстоит иначе в ТПЭ, где физическая диффузия веществ, естественно, протекает с меньшей скоростью. Так, в системе, состоящей из комплекса [Ru(bipy)3] 2+ введённого в ТПЭ "Nafion", коэффициент диффузии заряда Dct, равный 4·10 –10 см 2 ·с –1, складывается из величин 0,3·10 –10 см 2 ·с –1 и 3,7·10 –10 см 2 ·с –1, отражающих соответственно физическое движение комплекса в полимере и электронный перенос заряда. Таким образом, в полимерных электродах для повышения эффективности протекающих на них процессов необходимо стремиться к организации наряду с диффузионным и электронного переноса заряженных частиц через полимер.
Перспективные области применения полимерных электродов весьма разнообразны:
— электрохромные устройства — системы, изменяющие свой цвет при изменении подаваемого на них электрического сигнала. Основой электрохромных устройств являются оптически прозрачные электроды (кварцевые пластины с прозрачным электропроводным слоем оксидов олова и индия). В ТПЭ, нанесённый на этот электрод, вводится электроактивное вещество, способное изменять свой цвет при электрохимическом окислении или восстановлении. Подобные устройства применяются, в частности, как оптические фильтры с регулируемой интенсивностью поглощения света; — сенсорные устройства, работающие аналогично электрокаталитическим системам, принцип действия которых описан в этом разделе (см. рис. 5). Задача сенсорных устройств мониторинг окружающей сенсор среды, информирование о появлении в ней определённого вещества и его концентрации. Так, при появлении во внешней среде вещества Ox (см. рис. 5) концентрация вещества А в ТПЭ будет уменьшаться за счёт реакции с ним (разумеется, вещество А в этом случае должно быть подобрано так, чтобы быстро и селективно реагировать с Ox). Уменьшение концентрации А в ТПЭ приведёт к изменению потенциала ХМЭ или протекающего через него тока. К настоящему времени на основе полимерных электродов разработаны сенсоры, реагирующие на водород, сероводород, углекислый газ, кислород; — модельные фотоэлектрохимические преобразователи, то есть устройства, преобразующие энергию света в электрическую за счёт протекания в них фотохимических и электрохимических реакций.
Заключение
Появившись сравнительно недавно, твёрдые полимерные электролиты уже послужили основой для создания новых электрохимических устройств, характеризующихся отсутствием жидкого агрессивного электролита, уменьшенными массогабаритными характеристиками, высокой степенью надёжности и экологической безопасности. Большое число исследований, ведущихся в области ТПЭ и химически модифицированных электродов научными группами всего мира, обещает получение в ближайшем будущем новых революционных результатов в энергетике, создание новых типов оптоэлектронных и логических компьютерных устройств, биомедицинских микросенсорных систем.
4. Твёрдые оксидные электролиты
4.1 Общие сведенья
Жидкие электролиты водные растворы, или расплавы, солей, кислот и оснований — известны давно. Они работают в аккумуляторах и "сухих" батарейках, применяются для получения и очистки металлов, щелочей, органических соединений, для никелирования и анодирования. Свойства жидких электролитов знакомы многим — их изучают даже в школе. Но есть ещё один класс подобных веществ так называемые твёрдые электролиты. В 1820 году Ханс Кристиан Эрстед обнаружил магнитное действие электрического тока. На рисунке Р. Шторха виден гальванический элемент того времени: пара электродов из разных металлов, погруженных в жидкий электролит — раствор кислоты или щёлочи. Сегодня наиболее перспективными считаются устройства, работающие на твёрдых оксидных электролитах — материалах, изучение которых началось совсем недавно. Знают о них в основном только специалисты-химики, история их изучения коротка, широкое применение только начинается. Твёрдые электролиты связывают в основном с надеждой создать лёгкий и ёмкий аккумулятор для электромобиля. Сегодня аккумулятор массой 50–60 килограммов способен запасти гораздо меньше энергии, чем её "хранится" в бензобаке. Источник тока на твёрдом электролите, над созданием которого работают ведущие компании мира, по удельной энергоёмкости обещает сравняться с топливом.
Спектр применения твёрдых электролитов очень широк. На их основе можно делать "вечные" печи и источники света, анализаторы газов, устройства для получения чистого кислорода, генераторы электричества и многое другое. Будущее твёрдых электролитов представляется весьма многообещающим, поэтому знать о них следует.
4.2 Электролиты
В конце прошлого века Вальтер Нернст, известный немецкий исследователь, много сделавший для развития электрохимии, использовал в осветительных лампах спресованную смесь оксидов циркония и кальция. Электрический ток, проходя через стерженёк из этой "массы Нернста", нагревал его до белого каления. Так нашёл своё первое практическое применение твёрдый электролит.
Как известно, в металлах электрический ток создают покинувшие свои атомы, то есть свободные, электроны. В электролитах это делают другие заряженные частицы — ионы — целые атомы с недостающими электронами (положительные ионы, катионы) или с лишними (отрицательные ионы, анионы).
Растворы кислот, щелочей и солей образуют электролит — смесь положительных катионов (чёрные кружки) и отрицательных анионов (белые). Если в раствор опустить пару электродов, подключенных к источнику постоянного напряжения, катионы начнут двигаться к отрицательному электроду, анионы — к положительному. Через электролит пойдёт электрический ток, обусловленный движением зарядов разных знаков.
Если в жидкий электролит погрузить два электрода и приложить напряжение, то в электролите возникнет ток, направленное движение ионов: катионы пойдут к отрицательному ("–") электроду, к катоду; анионы — к положительному ("+"), к аноду.
Возможен и обратный процесс: если погрузить в жидкий электролит два электрода из определённым образом подобранных металлов, то на одном из них в результате химических реакций появится избыток электронов ("–"), а на другом — недостаток ("+"). Между электродами будет действовать электродвижущая сила, и, значит, вся система электроды–электролит превратится в химический генератор электрического тока. Так работал первый химический источник тока — гальванический элемент из медной и цинковой пластин, погружённых в раствор поваренной соли или серной кислоты. Так работают все нынешние гальванические элементы, батарейки и аккумуляторы.
В принципе то же самое происходит в химических электрогенераторах с твёрдыми электролитами.
4.3 Особенности твёрдых электролитов
Твёрдых электролитов известно великое множество — это оксиды, соли, кислоты и даже полимеры. В твёрдых растворах оксидов металлов разной валентности ток создаётся отрицательными ионами (анионами) кислорода.
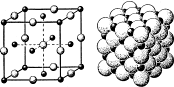
Модель типичного ионного кристалла — знакомой всем поваренной соли NaCl (А). Её кубическую решётку образуют две кубические же подрешётки, сдвинутые одна относительно другой на половину длины ребра куба. В узлах одной находятся катионы натрия Na+ (чёрные шарики), в узлах другой — анионы хлора Cl– (белые). Если же в модели соблюсти точный масштаб, станет видно, что ионы в решётке упакованы очень плотно (Б), и для наглядности кристаллическую структуру нередко рисуют двумерной.
Большинство этих твёрдых растворов — ионные кристаллы: в узлах кристаллической решётки находятся не нейтральные атомы, а заряженные ионы. Они образуют две подрешётки — катионную и анионную. Ионы совершают колебательные движения, но перемещаться по кристаллу, как в жидкости, не могут. Как же тогда в твёрдых электролитах возникает ток — движение заряженных частиц?
Ситуация меняется, если основное вещество "разбавить" другим похожим соединением, в котором анионов меньше, а катионов — столько же. Тогда катионная решётка этого твёрдого раствора остаётся прежней, а в анионной появляются свободные места — вакансии. Пустые места в отрицательно заряженной решётке можно рассматривать как положительные заряды. Под действием внешнего напряжения в них начнут переходить анионы с достаточно большой энергией, а вакансии "побегут" в противоположном направлении — к катоду. Возникнет электрический ток, обусловленный движением ионов только одного сорта. Это одна из особенностей твёрдых электролитов.
Ионная проводимость тем выше, чем больше в кристалле вакансий. Однако с ростом их количества уменьшается подвижность анионов, причём довольно быстро, поэтому проводимость сначала достигает максимума, а потом начинает падать. Для твёрдых оксидных электролитов на основе ZrO2, например, максимум электропроводности соответствует концентрации катионов 10–15%.
Свойства твёрдых оксидных электролитов
Анионы с достаточной кинетической энергией есть всегда, но при комнатной температуре их очень мало, и твёрдые оксидные электролиты ведут себя как хороший изолятор. По мере нагрева подвижность анионов увеличивается очень быстро, и при 150°С проводимость электролитов становится уже вполне ощутимой. Но основная их рабочая температура лежит между 700 и 1000°С, в связи, с чем они и называются высокотемпературными электролитами.
 А
А
 Б
Б
 В
В
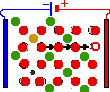 Г
Г
Цветом обозначены:
Зелёный — анион M, Красный ион G, Жёлтый — анион M *, Фиолетовый — ион M*, Красный с белой точкой вакансия
Двумерная решётка соединения типа MG2 (например, ZrО2) (А). Ионы элементов G и M образуют регулярные структуры — кристаллические подрешётки. Если смешать два соединения MG2 и M*G (скажем, СаО), в анионной подрешётке G появятся пустые места вакансии (Б). Соседние катионы при достаточной энергии станут занимать пустые места, и вакансии начнут хаотично двигаться (направление указано стрелками) по кристаллу (В). Если к кристаллу приложить постоянное напряжение, вакансии устремятся к положительному электроду — аноду (Г). Через кристалл — твёрдый электролит — пойдёт электрический ток, обусловленный движением зарядов только одного знака.
Твёрдые электролиты всегда находятся в атмосфере определённых газов, состав которой меняет их свойства. Чтобы понять, в чём тут дело, вспомним, что такое динамическое равновесие. В жидкости, например, всегда есть "быстрые" молекулы, которые с её поверхности переходят в пар. Но и из пара молекулы возвращаются в жидкость — между ними происходит непрерывный обмен молекулами. Пар находится в равновесии с жидкостью, и, чтобы подчеркнуть, что оно сопряжено с движением на молекулярном уровне, его называют динамическим.
Характер обмена между твёрдым телом и газом сложнее. Ион кислорода в поверхностном слое превращается в нейтральный атом. Два атома соединяются в молекулу кислорода, которая отрывается от поверхности и переходит в газ. Возвращение кислорода из газа в твёрдое тело происходит в обратном порядке. Обе эти реакции идут одновременно: между электролитом и газом, содержащим определённое количество кислорода, существует динамическое равновесие. Оно нарушается, когда концентрация кислорода в газе меняется. Итак, твёрдый электролит в виде смеси оксидов циркония и кальция проводит ток только при высоких температурах. Поэтому лампы Нернста включали, предварительно сильно прогрев их стержень. И появление в 1905 году лампы "немедленного действия" с вольфрамовой нитью предопределило её абсолютный успех. Однако известно, что кое-где и сегодня можно встретить странный электрический фонарь, который нужно поджигать спичкой. Это, судя по всему, лампы Нернста, дожившие до наших дней: твёрдые растворы на основе диоксида циркония — исключительно стойкие вещества, они могут работать на воздухе десятилетиями, не окисляясь. Кстати, вполне современные печи с такими нагревателями были разработаны в свердловском Восточном институте огнеупоров в начале 80-х годов.
Главное предназначение твёрдых оксидных электролитов виделось в создании топливных элементов химических источников тока, в которых энергия газа непосредственно превращается в электрическую. Топливные элементы — близкие родственники гальванических элементов. Но те служат, пока в их электролите и электродах есть активные вещества, а топливные элементы могут работать сколь угодно долго, пока к ним подводится горючее. Систематические исследования твёрдых оксидных электролитов начались в Германии в начале 50-х годов, а с конца 50-х развернулись в СССР, США и Канаде. В нашей стране эти работы с самого начала вёл Институт химии Уральского филиала АН СССР (Свердловск, ныне Екатеринбург), и школа высокотемпературной электрохимии твёрдых электролитов, созданная на Урале, стала уникальной по широте охвата проблемы и глубине её изучения.
Устройства с твёрдыми оксидными электролитами

Цветом обозначены:
Пробирка из ТОЭ, Корпус, Электроды, Нагреватель, Теплоизоляция, Стрелки — потоки газа
Схема электрохимического устройства. Пробирка из твёрдого оксидного электролита с металлическими электродами на стенке помещена в замкнутый объём, окружённый теплоизоляцией. Рабочую температуру около 1000°С создает нагреватель. Внутрь пробирки и в окружающий её объём подаётся газ. Это несложное устройство может работать и как источник тока, и как химический реактор.
Конструкций, в основе которых лежат твёрдые оксидные электролиты, запатентовано очень много, но принцип их действия одинаков и довольно прост. Это пробирка с парой электродов на стенке, снаружи и внутри. Она помещена в нагреватель; внутрь пробирки и в пространство, её окружающее, можно подводить газ. Посмотрим, какие функции могут выполнять такие устройства.
Потенциометрические датчики состава газа. Наверное, они наиболее просты. Мы уже знаем, что электроды в разных газах приобретают разные потенциалы. Если, скажем, внутри пробирки находится чистый кислород, а снаружи — газ с неизвестной его концентрацией, то по разности потенциалов электродов можно эту концентрацию определить.
Потенциометрические датчики позволяют определять состав и более сложных газовых смесей, содержащих углекислый и угарный газы, водород и водяной пар. Если стерженёк из твёрдого электролита с электродами на торцах нагрет неравномерно, он начнёт терять кислород и между электродами возникнет разность потенциалов. По её величине можно определить, например, состав выхлопных газов автомобильного двигателя. На Западе, где требования к чистоте выхлопных газов очень строги, такие датчики выпускаются миллионами. У нас же на такие "пустяки" пока не обращают внимания.
Кислородные датчики пока единственные устройства с твёрдыми оксидными электролитами, нашедшие практическое применение.
Кислородные насосы. Пусть во внешнее пространство пробирки подаётся воздух или газ, содержащий кислород. Если внешний электрод стал анодом, а внутренний — катодом, то из газа в пробирку пойдёт чистый кислород. Подобные устройства — кислородные насосы — могут найти применение там, где потребление кислорода невелико или требуется его высокая чистота.
В медицине, например, используется и чистый кислород, и воздух с пониженным содержанием кислорода так называемая "гипоксическая смесь", или "горный воздух". Электрохимические насосы наряду с мембранными оксигенаторами (см. "Наука и жизнь" № 2, 1999 г.) позволят решить массу проблем, особенно в медицинских учреждениях, удалённых от промышленных центров. В атмосфере с пониженным содержанием кислорода значительно дольше хранятся продукты питания, и устройства с кислородными насосами могут стать экономичней привычных холодильников.

На основе твёрдых оксидных электролитов можно создавать разные электрохимические устройства. А. Топливный элемент. Внутрь пробирки подаётся водород H2 или угарный газ CO, во внешнее пространство — воздух. На внутреннем электроде газы окисляются, образуя либо воду, либо углекислый газ. Между электродами возникает разность потенциалов. Б. Электролизер для разложения водяного пара и углекислого газа. На внутреннем электроде под действием приложенного напряжения они восстанавливаются до водорода и окиси углерода:
Н2О + 2е– = Н2 + О2–
СО2 + 2е– = СО + О2–
Освободившиеся ионы кислорода O2– мигрируют сквозь стенку трубки, воссоединяются и выделяются на внешнем электроде в виде кислорода O2. В. Кислородный насос. Кислород воздуха, поступающего в пробирку, на внутреннем электроде превращается в O2–, а на внешнем выделяется в виде чистого кислорода. Г. Датчик состава газа. Воздух или чистый кислород поступает внутрь пробирки, исследуемый газ — во внешнее пространство. На электродах возникнет разность потенциалов, величина которой определяется составом газа.
Электролизеры. Теперь к внешнему электроду — катоду — подводят водяной пар или углекислый газ. На катоде будет происходить разложение пара или углекислого газа, а на аноде в обоих случаях выделяется кислород. Уникальная способность этого высокотемпературного электролизера одновременно разлагать водяной пар и углекислый газ позволяет создать систему жизнеобеспечения, скажем, на космических объектах.
Теплоэлектрогенераторы. Человек сделал первый шаг к независимости от природы, научившись сохранять огонь, поистине универсальный источник энергии. Костёр давал тепло и свет, на нём готовили пищу, он расходовал ровно столько топлива, сколько было необходимо. Костёр тысячелетиями оставался главной энергетической установкой человека, и неудивительно, что мы испытываем какую-то ностальгию по очагу с горящими дровами.
Ещё в конце прошлого века свет давали свечи и керосиновые лампы, а тепло — печи. Лишь немногим более ста лет назад на человека начало работать электричество, которое могло давать свет, тепло, механическую работу. Одно время казалось, что достаточно подвести к жилищу только электрическую энергию, а уж там преобразовывать её во что угодно. Но сказала своё слово экономика: кпд электростанции менее 40%, потери при передаче и обратном превращении электричества в другие виды энергии тоже значительны. Ясно, что там, где нужно только тепло, его целесообразно получать прямо из топлива. И не случайно сегодня обсуждается простая идея: вернуть "очаг" в дом в виде электрохимического генератора с топливным элементом, преобразующим энергию топлива в электричество и тепло.
Топливные элементы. Пусть к внешним стенкам пробирки подаётся водород, а внутрь её — кислород. Между электродами возникнет напряжение около вольта, по соединяющей их цепи потечёт ток, и на электродах пойдут реакции, обратные тем, что проходят в электролизере. Внешний электрод станет анодом, внутренний — катодом, а устройство превратится в источник тока — твёрдооксидный топливный элемент.
Одно и то же устройство может служить и топливным элементом, и электролизером, позволяя аккумулировать электрическую энергию. В период низкого её потребления невостребованная мощность электростанций используется для получения водорода. В пике потребления электролизер начинает работать как топливный элемент, производя электричество из водорода.
Топливом в элементе может быть и угарный газ. В него нетрудно превратить уголь, нефть, различные газы и спирты (которые, например, в Бразилии используют как горючее для автомобилей). Элемент послужит основой электрохимического генератора, способного существенно изменить концепцию снабжения жилища энергией. Наиболее прост в техническом отношении генератор на природном газе — метане или пропане.
Как показывают исследования, его электрический кпд достигает 70%. Остальные 30% энергии топлива выделяются в виде тепла, которое можно использовать в паровых турбинах. Кпд такой комбинированной установки способно превысить 80% — столь высокой эффективности нет ни у одного генератора.
Восемь лет назад в Институте высокотемпературной электрохимии Уральского отделения РАН был изготовлен демонстрационный генератор на метане мощностью один киловатт. Но до практической реализации дело никак не дойдёт. Опытно-конструкторские работы, которые уже начинались, до конца так и не доведены. Задача очень сложна, её необходимо решать в рамках национальной программы, попытки, разработать которую оказались пока безуспешными.
5. Материалы ионики твердого тела
5.1 Исторические сведенья
Первые упоминания о высокой проводимости ионных кристаллов относятся, по-видимому, к началу XIX в.: в 1833 г. М.Фарадей отметил аномально большую электропроводность сульфида серебра, сравнимую с таковой для металлов. Аналогичный эффект в оксидных материалах был обнаружен В.Нернстом, который использовал керамику на основе оксида циркония, легированного иттрием, в качестве материала для ламп накаливания. Только в начале XX в. ученые доказали, что высокая проводимость таких веществ обусловлена движением не электронов, а разнозаряженных ионов, как это наблюдается в жидких электролитах. Подобные соединения получили название твердых электролитов или суперионных проводников.
5.2 Непоседливые ионы
При нормальных условиях перенос заряда ионами в обычных твердых телах - как кристаллических, так и аморфных - не очень значителен и при комнатной температуре удельная проводимость не превышает 10–10-10–12 Ом–1·см–1. Электропроводность же суперионных проводников составляет величину порядка 10–1 Ом–1·см–1 (при комнатной температуре!). Это значение близко к проводимости расплавов и концентрированных растворов жидких электролитов. Таким образом, речь идет о материалах, сочетающих свойства жидкостей (проводимость, характерную для жидкого расплава или раствора, ионную термоэдс) и твердых тел (механическую жесткость кристаллов). В настоящее время твердые электролиты перестали быть экзотическими объектами исследований благодаря открытию и синтезу нескольких сотен новых соединений с высокой ионной проводимостью. Они незаменимы при создании полностью твердотельных топливных элементов, газовых и жидкостных сенсоров, миниатюрных аккумуляторов (все знают о литиевых батарейках, но не все задумываются, из чего они сделаны). Для эффективного поиска таких веществ потребовались новые теоретические подходы к изучению явлений аномально быстрого ионного переноса в конденсированных средах и развитие специальных современных экспериментальных методик. Этим обусловлено возникновение нового раздела науки - ионики твердого тела, находящейся на пересечении физики и химии твердого тела, электроники и электрохимии, кристаллографии и неорганической химии, материаловедения и энергетики. Существование суперионной проводимости во многом зависит от структурных особенностей материала: чтобы ионы могли перемещаться, энергетически близких кристаллографических позиций для размещения потенциально подвижных ионов в элементарной ячейке должно быть больше, чем самих ионов; энергия разупорядочения ионов по позициям в кристаллической решетке и энергия, затрачиваемая на движение, должны быть малыми (~kT, где, как обычно, k - постоянная Больцмана, T - температура). Энергетические барьеры между соседними позициями должны быть небольшими (в сравнении с kT), что при наличии в кристаллической решетке вакантных мест приведет к статистическому распределению мобильных ионов по разрешенным позициям; в кристаллической структуре "сетка каналов" для движения ионов должна быть сквозной, в противном случае быстрое движение заряженных частиц будет возможным лишь в пределах одной или нескольких элементарных ячеек. Перечисленным требованиям удовлетворяют лишь особые кристаллы, в структуре которых для атомов одного или нескольких сортов отсутствует дальний порядок в их пространственном расположении, хотя для остальных частиц дальний порядок сохраняется. Такие соединения рассматриваются как кристаллы с собственным структурным разупорядочением.
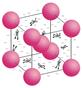
Рис.1. Подвижные положительные ионы серебра, как аквалангисты, легко перемещаются в пространстве между рифами - атомами иода (сферы) - в кристалле AgI.
Хорошим примером служит структура модельного кристалла AgI (рис.1). Кристаллический каркас "держат" анионы иода, а два катиона серебра могут размещаться по 12 тетраэдрическим позициям элементарной ячейки. Именно для такой ажурной структуры, в которой нарушен дальний порядок для атомов одного типа, было введено наглядное (может быть, не совсем удачное) понятие "квазирасплавленная подрешетка", и считалось, что жесткая анионная подрешетка находится в "катионном расплаве".
Подвижные частицы относительно свободно перемещаются по всему объему кристалла, за исключением той его части, которая занята ионами неподвижного остова. Поэтому здесь более разумно говорить не об "ионном расплаве", а о существовании в матрице кристалла "проводящего пространства". Такое качественное рассмотрение находит подтверждение в полиэдрическом представлении одной из подрешеток кристалла (см., например, рис.2).
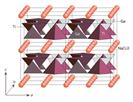
Рис.2. Кристаллическая структура Na2TiGeO5: выделены слои из жестко связанных тетраэдров [GeO4] и пирамид [TiO5]. В пространстве между слоями могут свободно перемещаться подвижные ионы.
Растущую потребность в суперионных материалах - как новых соединений, так и известных в ином качестве (газоплотная керамика, пленочные покрытия, наноструктурные системы) - нельзя удовлетворить, ограничиваясь лишь полуэмпирическими подходами и классическими методами синтеза. Решение этой сложной проблемы возможно лишь в случае, если опираться на фундаментальные закономерности, установленные при изучении синтеза новых материалов и процессов ионного транспорта в них. В чистом виде такие закономерности наиболее четко прослеживаются при исследовании монокристаллических твердых электролитов. В то же время при использовании твердых электролитов в качестве рабочих сред функциональных элементов необходимо учитывать, что нужны материалы заданного вида и формы, например в виде плотной керамики или пленочного покрытия. И здесь на помощь могут прийти наноматериалы, которые зачастую либо обладают улучшенными характеристиками по сравнению с объемными монокристаллами, либо даже дополнительно приобретают новые свойства. Основная особенность всех типов наноматериалов (нанопористых, нанокристаллических, нанокомпозитных систем) заключается в преобладающей роли поверхности, а не объема. Поскольку структура поверхности как границы раздела твердое тело-окружающая среда значительно отличается от структуры объема, можно говорить о существенно дефектной (по отношению к объему) структуре поверхности и ожидать заметного изменения характеристик материала.
5.3 Некоторые аспекты поиска, создания и изучения объектов ионики твердого тела на примере работ, выполненных в Институте кристаллографии РАН
Целенаправленные исследования в этой области были начаты в 1980 г. Ионная проводимость твердых электролитов обеспечивается переносом самых различных ионов - одно-, двух-, трехзарядных катионов (Ag+, Cu+, Li+, Na+, K+, Rb+, Tl+, Cs+, Ca2+, Zn2+, Mg2+, Pb2+, Al3+, Sc3+, Ce3+, Eu3+) и анионов (F–, Cl–, Br–, O2–, S2–). Существуют материалы, где носителями заряда служат ионы двух или даже трех сортов, и вещества со смешанной ионно-электронной проводимостью. Особый интерес представляют суперионные проводники с Li+- и Na+- ионной проводимостью, поскольку именно они дают максимальный выигрыш в энергии, что гарантирует им будущее в производстве миниатюрных литиевых батареек и тяговых аккумуляторов для электромобилей. Поэтому все стремятся улучшить характеристики известных соединений или найти для этих ионов принципиально новые проводящие матрицы. Целенаправленное изменение характеристик соединений возможно только в случае, если нам удастся заглянуть в глубь кристалла, чтобы узнать, как и насколько эффективно способны перемещаться ионы в кристаллической решетке. Иначе говоря, нужно оценить потенциальные каналы проводимости и найти способы увеличения скорости движения заряженных частиц по ним. Рассмотрим в этом плане как достаточно известное соединение - ортофосфат лития Li3PO4, так и сравнительно новое - литий-замещенный титанат лантана La2/3-xLi3x}1/3–2xTiO3 ( - вакансия в позиции крупного катиона).
С середины 70-х годов ортофосфат лития известен как ионный проводник, в структуре которого пустоты кристаллического каркаса формируют сквозные прямые каналы вдоль осей а и с и зигзагообразные вдоль оси b (рис.3). Однако величина электропроводности не очень высока, поскольку, несмотря на "рыхлость" структуры, все катионы лития участвуют в постройке жесткого каркаса и не способны свободно перемещаться по каналам. Решение задачи увеличения ионной проводимости напрашивается само собой: необходимо поместить в каналы дополнительные катионы Li. Это достигается специальным введением в базовый материал гетеровалентных примесей, что и наблюдается в твердых растворах со структурой высокотемпературной модификации Li3PO4.
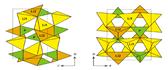
Рис.3. Каналы проводимости в структуре Li3PO4 образуются при формировании каркаса из связанных общими вершинами тетраэдров [Li1O4], [Li2O4] и [PO4]. а - проекция bc, б - проекция аb.
Получаемые нестехиометрические фазы систем Li4GeO4-Li3VO4 и Li4GeO4-Li3PO4 обладают ионной проводимостью, значения которой составляют 10–4-10–5 Ом–1·см–1 уже при комнатной температуре. Чтобы понять механизм ионного транспорта, потребовалось провести экспериментальные исследования на монокристаллах больших размеров и хорошего качества. Монокристаллы Li3+xP1–xGexO4 (x=0.34) были выращены в Институте кристаллографии методом кристаллизации из раствора в расплаве. Величины удельной проводимости кристалла Li3.34P0.66Ge0.34O4 составляют 1.8·10–6 и 3.7·10–2 Ом–1·см–1 при 40° и 400°С соответственно - что, как видно из рис.4, на несколько порядков выше проводимости номинально чистого -Li3PO4.

Рис.4. Ионная проводимость монокристаллов Li3PO4 и Li3+xP1–xGexO4. Разными значками изображены величины проводимости в различных кристаллографических направлениях.
Миграция ионов лития в твердом растворе Li3+xP1–xGexO4 связана с внедрением дополнительных катионов Li+ в пустоты кристаллического каркаса, что приводит к разупорядочению литиевой подрешетки не только в каналах проводимости, но и в жестком каркасе (рис.5), и число доступных для миграции лития позиций существенно возрастает. Кристаллическая структура при этом становится приблизительно одинаково "прозрачной" для ионного транспорта во всех направлениях, благодаря чему значения проводимости по трем главным кристаллографическим направлениям почти выравниваются (анизотропия проводимости в твердом растворе Li3+xP1–xGexO4 по сравнению с Li3PO4 понижается).
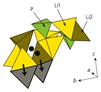
Рис.5. Фрагмент кристаллической структуры твердого раствора Li3+xP1–xGexO4. Зеленым цветом показаны тетраэдры PO4, желтым и коричневым - тетраэдры LiO4. Дополнительные ионы лития (темные кружки) при образовании твердого раствора смещаются в направлении, показанном стрелками. Собственные ионы лития переходят в тетраэдры, ребра которых выделены жирными линиями (в чистом -Li3PO4 эти тетраэдры незаняты).
Литий-замещенный титанат лантана Li0.255La0.582TiO3 может служить еще одним примером целенаправленного конструирования твердого электролита. Внедрение достаточно большого количества посторонних атомов, в том числе и лития, в кристаллическую матрицу перовскито-подобной фазы La2/3TiO3 приводит к образованию нестехиометрических фаз La2/3–xLi3x}1/3–2xTiO3. Ионный перенос осуществляется за счет перескока внедренных ионов лития по вакантным позициям. Создание монокристаллов таких сложных фаз сродни искусству, и это в полной мере относится к синтезу литий-замещенного титаната лантана методом бестигельной зонной плавки (блок-схема установки показана на рис.6). В полученных кристаллах высокая ионная проводимость при комнатной температуре (около 5·10–4 Ом–1·см–1) соседствует с пренебрежимо малой величиной электронной проводимости.
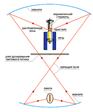
Рис.6. Схема установки для выращивания кристаллов методом бестигельной зонной плавки.
Чтобы вырастить монокристаллы, керамический стержень плавят направленным световым пучком мощной лампы. При опускании стержня в печь, имеющую температурный градиент, происходит кристаллизация расплава с формированием массивного монокристалла. Позвольте пройти, или "Окно проводимости". На первый взгляд кристаллическая структура Li0.255La0.582TiO3 не должна допускать высокой ионной проводимости, поскольку размеры "окна проводимости" (рис.7) недостаточны для беспрепятственного перемещения ионов Li+ по каналам. Наблюдаемое противоречие можно объяснить особой ролью тепловых колебаний атомов кристаллического каркаса, из-за которых размер "окна проводимости" постоянно меняется - каналы "дышат". Перескок ионов в соседнюю позицию может происходить в момент наибольшей открытости "окна".

Рис.7. "Окно проводимости" в Li0.255La0.582TiO3 - наиболее узкий участок канала проводимости (выделен красным цветом) для перескока иона лития из одной позиции в другую (соседнюю).
Получить новые структурные матрицы с ажурной структурой, пригодной для заполнения "ионным расплавом", не так просто, поэтому ученые обращаются за помощью к природе и исследуют известные минералы, создавая искусственные кристаллические матрицы на их основе. Так были найдены катионные проводники в семействе сложных оксидов (-глинозем), силикатов (цирконосиликаты - насикон, лисикон, алюмосиликаты - сподумен, эвкриптит), фторионные проводники на основе флюорита. Наше внимание привлек силикат натрия-титана - натисит Na2TiSiO5. В его структуре между слоями, составленными Ti-полуоктаэдрами и Si-тетраэдрами (рис.2), можно увидеть "прослойки" из катионов натрия, что позволяло надеяться на достаточно высокую подвижность щелочных ионов. Нам удалось синтезировать и изучить электрические свойства массивных монокристаллов двух членов семейства A2TiGeO5 со структурой типа натисита: Na2TiGeO5 и Li2TiGeO5. Ярко выраженный слоистый характер кристаллической структуры этих соединений обусловливает высокую спайность в направлении, перпендикулярном оси с, и объясняет высокую анизотропию проводимости: отношение проводимостей в направлениях, параллельном и перпендикулярном слоям, достигает 104 (рис.8).
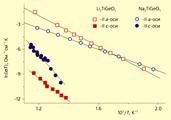
Рис.8. Температурные зависимости проводимости кристаллов Na2TiGeO5 и Li2TiGeO5 вдоль осей a и c.
Подвижными в кристаллах могут быть не только катионы, но и анионы, например фтора в нестехиометрических фазах М1–xRxF2+x со структурой флюорита (М=Ва, Sr, Ca; R=La-Lu,Y). Здесь надо отметить, что электропроводность чистых и слаболегированных дифторидов MF2 со структурой флюорита не очень велика и не превышает 10–6-10–5 Ом–1·см–1 при 500-600 К. Твердые растворы на основе МF2 с большой концентрацией примеси, являясь однофазными, имеют переменный состав и повышенную концентрацию анионов фтора. Ионный перенос трактуется в рамках предложенной нами модели дефектных областей, характеристики которых зависят как от типа катиона матрицы, так и от сорта ионов R3+, изоморфно замещающих ионы М2+ в матрице. В ядре дефектной области располагаются редкоземельные ионы и "замороженные" комплексообразованием атомы фтора в виде кластеров различного типа, а в периферийной части, т.е. прилегающей к ядру искаженной флюоритовой матрице, могут находиться слабо связанные, а потому подвижные анионы фтора, которые и переносят ток. Поэтому характеристики ионного переноса в сильнонестехиометрических фазах определяются главным образом атомным строением дефектных областей, так как подвижность междоузельных анионов F– зависит от типа катиона матрицы (Ca2+, Sr2+, Ba2+) и сорта редкоземельных ионов R3+. Совместный анализ электрофизических и структурных характеристик нестехиометрических фаз позволил предложить конкретный механизм ионного переноса, связанный со строением ядер дефектных областей.
Монокристаллы твердых электролитов хороши и необходимы как объекты для выяснения фундаментальных аспектов быстрого ионного переноса в твердых телах. Так выбираются оптимальные материалы, которые находят практическое применение уже в виде поликристаллов (керамика, порошки, покрытия).
Поликристаллические образцы обычно изготавливают классическим методом твердофазных реакций, который обладает рядом существенных недостатков: сложно получить полностью однофазные продукты из-за плохой гомогенизации исходных реагентов, нужна высокая температура отжига, синтез длителен и трудоемок. К одним из лучших литийпроводящих материалов относятся соединения семейства сложных литиевых фосфатов Li3M2(PO4)3, характеризующиеся (для монокристаллов и стандартной керамики) рабочими температурами выше 300°С. Чтобы понизить эти температуры, мы попытались приготовить сложные фосфаты в наноструктурном виде. Нанопорошки Li3M2(PO4)3 были синтезированы путем пиролиза ультрадисперсных растворов (рис.9), в котором гомогенизация исходных реагентов осуществляется на молекулярном (нано-)уровне, что значительно облегчает получение полностью однофазных материалов.

Рис.9. Схема получения кристаллического материала при ультразвуковом диспергировании и термической обработке растворов.
Суть метода заключается в следующем: в раствор, содержащий исходные реагенты, помещается мембрана, колеблющаяся с ультразвуковой частотой (рис.10). Над поверхностью раствора образуется "туман", состоящий из ультрадисперсных капель размером от сотен нанометров до микрометров. При быстром нагреве "тумана" происходит испарение растворителя, а затем химическое взаимодействие между реагентами. Этим методом были изготовлены сплошные гладкие пленки твердых растворов Li3FexSc2–x(PO4)3 толщиной 3-5 мкм. Снимки поверхности образцов, сделанные методом атомно-силовой микроскопии (рис.11), показывают столбчатую структуру пленок с диаметром зерен от 1 до 5 мкм. Каждое зерно состоит из множества кристаллитов размером 10-20 нм для х=2 и 50-100 нм для пленки состава х=0.5. Значения объемной ионной проводимости плотных керамических образцов Li3Fe2(PO4)3 из нанокристаллитов и нанокристаллических пленок близки и составляют 2·10–6 Ом–1·см–1 при комнатной температуре. Измеренные величины электропроводности более чем на порядок выше по сравнению с таковыми монокристаллов (рис.12).

Рис.11. Структура поверхности пленок Li3Sc2–хFeх(PO4)3 (данные атомно-силовой микроскопии): а - х=2; б - х=0.5.
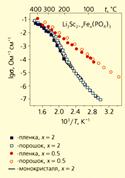
Рис.12. Температурные зависимости объемной ионной проводимости пленок и порошков Li3Sc2–хFex(PO4)3, полученных методом пиролиза диспергированных растворов.
"Интервенция" в кристаллические матрицы
Литийсодержащие фазы привлекательны не только как потенциальные твердые электролиты, но и как электродные материалы для литиевых источников тока - литий-ионных аккумуляторов (рис.13). При наложении электрического поля ионы лития выходят из анода и внедряются в материал катода, создавая эдс. При включении нагрузки происходит разрядка аккумулятора, и концентрации ионов лития на аноде и катоде выравниваются. После этого цикла требуется повторная зарядка системы. Напомним, что электродные материалы должны обладать смешанным, ионно-электронным, типом проводимости. Такому условию отвечают нестехиометрические ванадаты лития. Литий-ванадиевая бронза представляет собой фазу переменного состава, которая образуется при внедрении лития в "туннели" кристаллической структуры оксида ванадия. Сравнение структур бронз различных типов показывает, что наибольшей емкостью по литию обладает бронза типа Li1+xV+4xV+53–xO8.
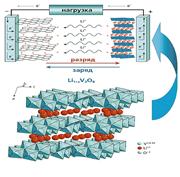
Рис.13. Принцип работы литиевого аккумулятора.
Оксидная ванадиевая бронза Li1+xV3O8 служит как анодом, так и катодом.
Наиболее эффективно источники тока будут работать при максимально большой емкости материала по проводящему иону (литию) и при высокой устойчивости материалов при циклическом чередовании заряда и разряда ячейки (циклировании). Улучшить характеристики материала можно разными способами, например, модифицируя состав введением примесей (легирование) либо изменяя микроструктуру материала (варьирование форм-фактора).
Мы синтезировали фазы внедрения со структурой Li1+xV3O8 и изучили их свойства. Полное заполнение всех вакантных позиций соответствует составу Li5V3O8, т.е. максимальная (теоретическая) емкость этого материала по литию достигается при х=4. Но все попытки разных исследователей добиться полного заполнения литиевых позиций в чистом ванадате лития LiV3O8 окончились неудачей: максимальное значение х достигло лишь 2.85. Мы попытались решить проблему, варьируя геометрические размеры элементарной ячейки кристалла путем легирования. Оказалось, что гетеровалентное замещение части ванадия на крупные катионы молибдена Mo6+ несколько улучшает ситуацию - для Li1+xMo0.25V2.75O8 емкость увеличивается, однако только до х=2.9.
Таким образом, легирование материала не позволило заполнить литием все доступные позиции в структуре. Здесь затруднения создают кинетические факторы, связанные с микроструктурой поликристаллического объекта, т.е. необходимо учитывать размер частиц, их взаимную ориентацию, наличие текстуры и т.п. Поэтому нами был применен новый способ синтеза исследуемого материала с наноразмерными кристаллитами на основе методов "мягкой химии" (низкие температуры синтеза, средние значения рН, органические прекурсоры и т.д.).
Для оптимизации форм-фактора материалов на основе Li1+xMoyV3–yO8 был использован золь-гель синтез этих фаз из растворов алкоголятов соответствующих металлов (рис.14)
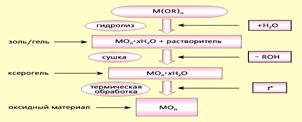
Рис.14. Золь-гель синтез Li1+xMoyV3–yO8 из растворов алкоголятов соответствующих металлов.
Самые интересные результаты были получены для тонких пленок Li1+xMoyV3–yO8 с использованием капельного нанесения растворов-прекурсоров на вращающуюся подложку. В этом случае удалось избежать нежелательного текстурирования покрытий и сформировать пленки субмикронной толщины из изотропных частиц с размерами от десятков до сотен нанометров. Такое направленное изменение форм-фактора привело к существенному улучшению разрядных характеристик пленок с высоким уровнем легирования молибденом: удалось практически полностью заполнить литиевую подрешетку (х=3.9).
4.Обобщающие сведенья
Мы рассмотрели только несколько примеров поиска и создания новых материалов, но они наглядно показывают, что ионика твердого тела - интенсивно развивающаяся отрасль науки, открывающая широкие возможности получения новых интересных результатов в области и фундаментальных, и прикладных исследований. Главный вопрос - как найти эффективные суперионные проводники, как повысить ионную проводимость соединений при относительно невысоких температурах - остается актуальным и решается на основе широкого спектра экспериментальных и теоретических данных.
Развитие современной энергетики выводит на передний план задачи конструирования нетрадиционных источников электрической энергии. Этот процесс будет определяться как миниатюризацией современных источников тока, так и развитием работ по созданию мощных аккумуляторных устройств. Успех здесь невозможен без развития молодых технологий (в частности, нанотехнологий) и способов получения твердых электролитов. Разнообразие областей применения твердотельных ионных материалов объясняет востребованность и возрастающий интерес к новым суперионным проводникам в виде монокристаллов, порошков, плотных керамик, пленочных покрытий.
Заключение
Ионика твердого тела очень быстро развивающееся направление современного материаловедения. Изложенный материал показывает перспективность использования физико-химических шэиндилов как основы систематического подхода к созданию СИП. Наряду с классическими, традиционными методами синтеза продемонстрированы большие возможности новых методов синтеза, таких, как взрывное сжатие, ионное и молекулярное наслаивание, разнообразные методики СУГ технологии. Проведен анализ работ по исследованию разнообразных катнонных проводников. Широкий спектр ядерно-физических и физико-химических методов изучения дает возможность детально рассмотреть ионные и электродные процессы в СИП, процессы образования и подвижности ионных дефектов.
Несмотря на большой прогресс, достигнутый в ионике твердого тела в последние годы, несомненно, что в ближайшем будущем мы станем свидетелями появления новых методов синтеза, прежде всего в области "мягкой химии", получения новых материалов в различном агрегатном состоянии с уникальными электрофизическими характеристиками, а также привлечения новых экспериментальных и теоретических методов, которые позволят получить информацию о природе суперионной проводимости на атомном уровне.
Литература
1.Хауффе К Реакции в твердых телах и на поверхности / Пер с нем М, 1962
2.Крегер Ф. Химия несовершенных кристаллов / Пер с англ М, 1960
3.Третьяков ЮД Твердофазные реакции М, 1978
4.Третьяков Ю. Д, Лепис X Химия и технология твердофазных материалов М, 1985
5.Жуковский В М, ТкаченкоЕВ //Изв Сиб отд. АН СССР Сер ким наук 1982 Т 15, №6 С 35
6.БудниковП П., Гисшлинг А М Реакции в смесях твердых веществ М, 1971
7.Дубовик M Ф., Промоскаяъ А И, Смирнов И H //Изв АН СССР Неорг материалы 1968 Т 4,№9 С 1580
8.Мурчи И В Процессы образования и переноса дефектов в бинарных галидах элементов I—ГУ групп Докт дис Л,1983
9.Соболев. Б П. Нестехиометрия в системах из фторидов щелочноземельных и редкоземельных элементов Авто-реф докт дис M, 1978
10.Мурчи ИВ. Андреев A M', Амелин Ю. В //Вести Леиингр ун-та 1982 №10 С 39
11.МуринИВ, Черное С В //Вести Леиингр ун-та 1982 № 10 С 105
12.ИгуенДН, Глумов OB, Мурин HB //Вести С-Петерб ун-та Сер 4 Физика, химия 1994 Вып 2 <№ II) С 50
13.Москвин А Л Неорганические материалы со смешанной ионно-элекгронной проводимостью на основе фторидов олова (П) свинца (П) Канд. дис Л, 1990
14.Лялина M Ю., Андреев A M, Калинина Л А и др. //Вести С-Петерб ун-та Сер 4 Физика, химия 1994 Вып 1 (№4) С 99
15.Фоминых ЕГ, Калинина Л А, Мурин ИВ, Широкова Г И II Вести С - Петерб ун-та Сер 4 Физика, химия 1997 Вып 1 (№4) С 71
16.Ушакова ЮН, Калинина Л А, Мурин И В, Широкова Г И /I Там же С 64
17.ГрузикАА, Елисеев А А Телешова В A, Шмидт E В //Журн. неорг химии 1972 Т 17, вып 1 С 11
18.Кустова T H, Обжерина К Ф, Камарзин Е В идр //Жури струкг химии 1969 Т 10 С 609
19.Самсонов ГВ, Радзиковская С В II Успехи химии 1961 Т 30, 1 С 60
20.Миронов К Е, Камарзин Л А СоколовВВ идр Редкоземельные полупроводники Баку, 1981
21.Препаративные методы в химии твердого тела / Пер с франц, Под ред П Хагенмюллера M, 1976
22.Бацанов С С, Лихова В Ф, Мороз Э M II Журн. неорг химии 1971 T 16 С 312
23.Бацанов С С. Мороз Э M II Физ. - хим. обработка материалов 1972. Т 6 С 127
24.Бацанов С С. Дерибас Л А, Кустова T H /I Жури неорг химии 1967 Т 12 С 2283
25.Бацанов С С, Доронин Г С, Мороз Э M идр //Физ. горен взрыва 1969 Т 5 С 283
26.Бацанов С С, Мороз ЭМ. РучкинЕД, Лазарева ЕВ //Изв АН СССР Сер хим наук 1973 Т 10 С 2323
27.МорозЭМ, Кетчик С В, Бацанов С С //Жури неорг химии 1972 Т 17 С 1775
28.Политое A A , Фусенко Б A, Простое И Ю //Докл РАН 1994 Т 334 С 194
29.Вольхин В И Ионный обмен и ионометрня Вып 9 /Под ред ФА. Белинской СПб, 1996 С 3
30.Уваров НФ Ионная проводимость твердофазных нанокомпознтов Докт дис Новосибирск, 1997
31.Немудрый А П. Порошина И A, Исупов В Л и др //Изв Сиб отд АН СССР Сер хим наук 1987 Выл 2, №5 С 48
32.Хауффе К Реакции в твердых телах и на поверхности / Пер с нем М, 1962
33.Крегер Ф Химия несовершенных кристаллов / Пер с англ М, 1960
34.Третьяков ЮД Твердофазные реакции М, 1978
35.Третьяков Ю Д, Лепис X Химия и технология твердофазных материалов М, 1985
36.Жуковский В М, ТкаченкоЕВ //Изв Сиб отд АН СССР Сер ким наук 1982 Т 15, №6 С 35
37.БудниковП П, Гисшлинг А М Реакции в смесях твердых веществ М, 1971
38.Дубовик M Ф, Промоскаяъ А И, Смирнов И H //Изв АН СССР Неорг материалы 1968 Т 4,№9 С 1580
39.Мурчи И В Процессы образования и переноса дефектов в бинарных галидах элементов I—ГУ групп Докт дис Л,1983
40.Соболев Б П Нестехиометрия в системах из фторидов щелочноземельных и редкоземельных элементов Авто-реф докт дис M, 1978
41.Мурчи ИВ. Андреев A M', Амелин Ю В //Вести Леиингр ун-та 1982 №10 С 39
42.МуринИВ, Черное С В //Вести Леиингр ун-та 1982 № 10 С 105
43.ИгуенДН, Глумов OB, Мурин HB //Вести С-Петерб ун-та Сер 4 Физика, химия 1994 Вып 2 <№ II) С 50
44.Москвин А Л Неорганические материалы со смешанной ионно-элекгронной проводимостью на основе фторидов олова(П)свинца(П) Канд дис Л, 1990
45.Лялина M Ю, Андреев A M, Калинина Л А и др //Вести С-Петерб ун-та Сер 4 Физика, химия 1994 Вып 1 (№4) С 99
46.Фоминых ЕГ, Калинина Л А, Мурин ИВ, Широкова Г И II Вести С -Петерб ун-та Сер 4 Физика, химия 1997 Вып 1 (№4) С 71
47.Ушакова ЮН, Калинина Л А, Мурин И В, Широкова Г И /I Там же С 64
48.ГрузикАА, Елисеев А А Телешова В A, Шмидт E В //Журн неорг химии 1972 Т 17, вып 1 С 11
49.Кустова T H, Обжерина К Ф, Камарзин Е В идр //Жури струкг химии 1969 Т 10 С 609
50.Самсонов ГВ, Радзиковская. С В II Успехи химии 1961. Т 30, 1. С 60
51.Миронов К Е, Камарзин Л А СоколовВВ идр Редкоземельные полупроводники Баку, 1981
52.Препаративные методы в химии твердого тела / Пер с франц, Под ред П. Хагенмюллера M, 1976 - 1983 P 332
53.Уваров НФ Ионная проводимость твердофазных нанокомпознтов Докт дис Новосибирск, 1997
54.Немудрый А П. Порошина И A, Исупов В Л и др. //Изв Сиб отд. АН СССР Сер хим. наук 1987 Выл 2, №5 С 48
55. Иванов-Шиц А.К., Мурин И.В. Ионика твердого тела. СПб., 2000.
56. Иванов-Шиц А.К. Электрофизические свойства твердых электролитов Li3M2(PO4)3 (M=Fe, Sc) // Электроника твердотельных систем / Под ред. М.В.Перфильева. Свердловск, 1991. С.70-88.
57. Иванов-Шиц А.К. Особенности ионного переноса в сильнонестехиометрических фазах M1–xRxF2+x (M=Ba, Sr, Ca; R=La-Lu, Y) со структурой флюорита // Электроника твердоэлектролитных систем / Под ред. М.В.Перфильева. Свердловск, 1991. С.89-105.
58. Иванов-Шиц А.К., Демьянец Л.Н. // Кристаллография. 1995. Т.40. №6. С.1077-1112
© 2009 База Рефератов