
Рефераты по рекламе
Рефераты по физике
Рефераты по философии
Рефераты по финансам
Рефераты по химии
Рефераты по хозяйственному праву
Рефераты по цифровым устройствам
Рефераты по экологическому праву
Рефераты по экономико-математическому моделированию
Рефераты по экономической географии
Рефераты по экономической теории
Рефераты по этике
Рефераты по юриспруденции
Рефераты по языковедению
Рефераты по юридическим наукам
Рефераты по истории
Рефераты по компьютерным наукам
Рефераты по медицинским наукам
Рефераты по финансовым наукам
Рефераты по управленческим наукам
психология педагогика
Промышленность производство
Биология и химия
Языкознание филология
Издательское дело и полиграфия
Рефераты по краеведению и этнографии
Рефераты по религии и мифологии
Рефераты по медицине
Контрольная работа: Витамины пиримидинового ряда (тиамин)
Контрольная работа: Витамины пиримидинового ряда (тиамин)
Федеральное агентство по здравоохранению и социальному развитию
Саратовский медицинский колледж Росздрава
Контрольная работа
Учебная дисциплина Фармацевтическая химия
2009 год
1. Теоретическая часть
Методы количественного анализа производных пиразола
1) Йодометрическое определение, обратный метод в присутствии ацетата натрия, спирта или хлороформа (антипирин).
2) Йодометрическое определение, прямое титрование (анальгин)
3) Кислотно-основное титрование в неводной среде (амидопирин, бутадион)
Методы установления подлинности никотинамида, никодина, изониазида
Общие реакции на замещенный цикл пиридина.
1. Пиролиз. При нагревании кристаллических веществ, производных пиридина с карбонатом натрия, образуется пиридин, обнаруживаемый по характерному запаху.
2. Цветная реакция с лимонной кислотой и уксусным ангидридом. При нагревании препарата с кристаллической лимонной кислотой и уксусным ангидридом возникает вишневое окрашивание.
Никотинамид. 1) Щелочной гидролиз при нагревании. Образуется аммиак.
2) Нагревание безводного препарата с безводным натрия карбонатом. Образуется пиридин, обнаруживаемый по характерному запаху.
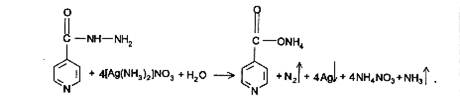
Изониазид. 1) Реакция окисления изониазида аммиачным раствором серебра нитрата и меди сульфата. Если реакцию проводить в нейтральной среде, сначала образуется комплексная соль, а затем (при нагревании) процесс переходит в окислительно-восстановительный с выделением металлического серебра.
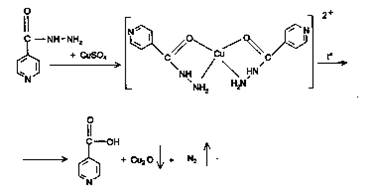
2) Реакция с меди сульфатом происходит в 2 этапа. За счет кислотных свойств изониазида сначала образуется комплексная соль голубого цвета. При последующем нагревании происходит окисление препарата с получением желто-зеленого, а затем грязно-желтого окрашивания с одновременным выделением пузырьков газа.
Производные хинолина. Его формула, источники получения
Хинолин (бензопиридин) — конденсированная система, образованная ароматическим бензольным ядром и пиридиновым циклом:
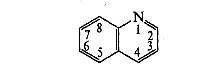
Хинолин представляет собой основание (рКа = 4,9), более сильное, чем анилин (рКа = 4,6), и более слабое, чем пиридин (рКа = 5,2). Как основание хинолин протонируется по атому азота, образуя с минеральными кислотами ограниченно растворимые и устойчивые соли.
Хинолин обладает бактерицидным, антисептическим и жаропонижающим действием, но в медицине не применяется из-за высокой токсичности (низкого значения терапевтического индекса). В настоящее время синтезированы многочисленные производные хинолина с различной фармакологической активностью и среди них хинин, являющийся противомалярийным средством.
К числу природных соединений, производных хинолина, относится большая группа алкалоидов, содержащихся в растениях семейства рутовых, мареновых (в основном в двух родах этого семейства: парнолистниковых, сложноцветных).
Хинное дерево произрастает в Южной Америке (дикорастущее) и культивируется в Индии. В коре этих растений (в «хинной корке») насчитывается более 20 алкалоидов (их содержание колеблется от 2 до 15%). Хинная корка известна как противомалярийное средство с начала XVII в.
Наибольшее значение имеют 4 алкалоида, выделенные из хинной корки, - хинин, хинидин, цинхонин и цинхонидин. Их структурной основой служат две гетероциклические системы: хинолин и хинуклидин (конденсированная система, состоящая из двух пиперидиновых циклов). Эти циклы связаны между собой вторичной спиртовой группой.
Источник получения хинина и его солей — хинная корка «аптечная» и «фабричная». Первую получают главным образом из Cinchona Succiruba, где содержится около 2 % хинина. «Фабричные корки» получают в основном из Cinchona Ledgeriana и Cinchona Calisaya, от 7 до 15 %. Поскольку в растительном сырье алкалоиды находятся в виде солей хинной кислоты, измельченную хинную корку обрабатывают смесью известкового молока со щелочью. Образовавшиеся основания извлекают бензолом: хинин отделяют в виде малорастворимого сульфата, который очищают дальнейшей перекристаллизацией.
Хинина сульфат вновь переводят в основание. Из основания получают хинина дигидрохлорид и гидрохлорид.
Напишите формулу дротаверина гидрохлорида, укажите свойства, применение, условия хранения
Дротаверина гидрохлорид (Но-шпа) – Drotaverini hydrochloridum (No-spa),
1-[(3,4 диэтоксифенил)метилен]-6,7-диэтокси-1,2,3,4-тетрагидроизлхинолина гидрохлорид.
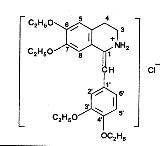
Зеленовато-желтый кристаллический порошок со слабым запахом. Раствори в оде и спирте.
Действие: Вазодилататор (сосудорасширяющее средство). Миотропный спазмолитик. Применяется при спазмах желудка и кишечника, спазматических запорах, приступах желчно-каменной болезни, язвенной болезни желудка и двенадцатиперстной кишки.
Лекарственные формы: таблетки, раствор для инъекций.
Хранение. Список Б
Отличия рибофлавина от рибофлавина мононуклеотида
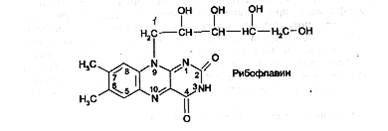
Витамин В2 (рибофлавин) представляет собой 6,7-диметил-9-(В-1' -рибитил) -изоаллоксазин:
Кроме рибофлавина, в медицинской практике применяют его коферментную форму - рибофлавина мононуклеотид: 7,8-диметил-10-(1-О-рибитил)-изоаллоксазин-5'-фосфат натрия, или рибофлан – 5 – монофосфат натрия:
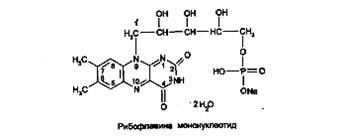
Рибофлавин и рибофлавина мононуклеотид - желто-оранжевые кристаллические порошки со слабым специфическим запахом. Мало растворимы в воде, практически нерастворимы в спирте, эфире, хлороформе, растворимы в растворах щелочей. Водные растворы препаратов имеют желтовато-оранжевый цвет с интенсивной флюоресценцией в УФ-свете.
Являются лабильными химическими веществами, легко разлагаются на свету.
Рибофлавин и его производные обладают характерными спектрами поглощения в УФ-области и оптической активностью в щелочной или слабо щелочной среде (в кислой и нейтральной средах оптически неактивен). При определении оптической активности рибофлавина в присутствии 0,1 М спиртового раствора калия гидроксида величина удельного вращения регламентируется в пределах от -110° до -130°. В среде 0,1 М раствора натрия гидроксида величина удельного вращения составляет -170°. Если к щелочному раствору препарата добавить раствор кислоты борной в количестве, необходимом для нейтрализации щелочи, поменяется направление оптической активности, а величина удельного вращения возрастет до +370°.
Рибофлавин и его производные как полифункциональные вещества обладают определенными кислотно-основными и восстановительными свойствами, а также способностью к гидролитическому расщеплению.
Рибофлавин и его производные — амфотерные соединения. Кислотные свойства связаны главным образом с наличием имидной группы. Очень слабыми кислотными свойствами обладают и спиртовые гидроксильные группы рибитильного остатка. За счет амид-ного фрагмента молекулы рибофлавина образуют комплексные нерастворимые соединения с солями А§+, Со2+, Нg2+ и с солями других тяжелых металлов.
Как основание рибофлавин растворяется в ледяной уксусной кислоте и минеральных кислотах, образует осадки с общеалкалоидными осадительными реактивами.
Окислительно-восстановительные свойства рибофлавина и его производных связаны с наличием сопряженной изоаллоксазиновой системы. Восстановление рибофлавина приводит к образованию бесцветного лейкорибофлавина, который может окисляться до характерно окрашенного рибофлавина.
Химичеcкое строение рибофлавина обусловливает различные типы окисления в зависимости от условий проведения процесса. Рибофлавин окисляется при действии различных окислителей (калия перманганат, калия дихромат и др.).
При окислении препарата концентрированной Н2SО4 образуется продукт красного цвета.
При действии на препарат раствора периодата натрия окисляется рибитильный фрагмент молекулы (реакция Малапрада). Данная реакция лежит в основе одной из методик количественного определения лекарственного вещества:
Выделившуюся в результате реакции кислоту муравьиную оттитровывают (потенциометрически или в присутствии индикатора) стандартным раствором натрия гидроксида.
По другой методике после действия периодатом к раствору прибавляют натрия йодид и кислоту серную. Выделившийся в результате реакции иод оттитровывают стандартным раствором натрия тиосульфата.
Разбавленный раствор рибофлавина в воде имеет яркую зеленую флюоресценцию при подсвечивании в УФ-свете, исчезающую при добавлении как раствора кислоты, так и раствора щелочи.
Добавление гидросульфита натрия приводит к исчезновению и флюоресценции, и окрашивания.
При действии кислоты и УФ-света образуется люмихром (производное изоаллоксазина), а при действии щелочи — люмифлавин (производное изоаллоксазина):
Количественное определение.
Химическая структура рибофлавина позволяет применять для его количественного определения различные методики химического и физико-химического анализа:
1) УФ-спектрофотометрию (Д.тах = 267 нм);
2) спектрофотометрию в видимой области (А,тах = 444 нм);
3) флуориметрические методики;
4) периодатное окисление (реакция Малапрада);
5) метод ацетилирования.
2. Ответ на тестовые задания
8 – В
17 – В
24 – Б,В
33 – В
44 – Г
56 – Б
67 – А
74 – В
85 - А
3. Витамины пиримидинового ряда (тиамин)
ВведениеТермин «витамин» (буквально «амин жизни») предложен Функом, выделившим фракцию из водного экстракта рисовых отрубей, обладающую выраженными основными свойствами (1911—1912). В 1934 г. Вильяме из 1 т рисовых отрубей выделил несколько граммов витамина В12 а в 1936 г. доказал его строение.
Организм животных и человека нуждается в поступлении витамина В1 (тиамина) извне с продуктами питания. Тиамин содержится в отрубях хлебных злаков (особенно в рисовых отрубях), дрожжах.
Тиамин, всасываясь из кишечника, фосфорилируется и превращается в тиамин-пирофосфат (дифосфат). В этой форме он является коферментом декарбоксилаз, участвующих в окислительном декарбоксилировании кетокислот (пировиноградной, α-кето-глугаторовой).
Тиамин является двукислотным основанием и поэтому образует 2 рода солей — хлориды и гидрохлориды (бромиды и гидробромиды). Фосфотиамин и кокарбоксилаза - сложные эфиры тиамина и фосфорной кислоты, т.е. коферменты.
Эти препараты белые порошки с характерным запахом, хорошо растворимы в воде, имеют кислую реакцию среды (как соли слабых органических оснований с сильными минеральными кислотами).
Бенфотиамин синтетический лекарственный препарат, близкий по строению к тиамину и его коферментным формам. В отличие от препаратов-предшественников практически нерастворим в воде.
1. Стабильность. Реакции подлинности
Тиамин и его производные принадлежат к очень неустойчивым соединениям витаминов. Так, тиамин под действием кислорода воздуха превращается в тиохром и тиаминдисульфид.
Разрушение тиамина вызывают также восстановители, сильно кислая или щелочная среда, свет (особенно УФ-лучи), повышение температуры. В растворах тиамина значение рН не должно превышать 4. За пределами оптимальной области рН повышение температуры больше способствует разложению препарата, чем присутствие кислорода.
Реакции подлинности.
Специфическая общегрупповая реакция подлинности тиамина и его препаратов — образование тиохрома. Сущность испытания заключается в постепенном окислении тиамина в щелочной среде (всего затрачивается 3 эквивалента щелочи) с образованием трицикличе-ского производного тиамина (тиохрома), способного давать синюю флюоресценцию в среде бутанола или изоамилового спирта при УФ-облучении.
Реакция идет в несколько стадий. На 1-й стадии происходит частичная нейтрализация препарата как соли галогеноводородной кислоты (1-й эквивалент щелочи):
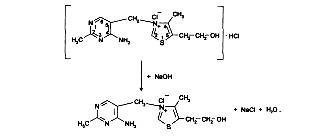
На 2-й стадии образовавшийся тиамина хлорид нейтрализуется (2-м эквивалентом щелочи) как соль четвертичного аммониевого основания до тиамина гидроксида:
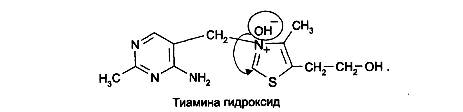
Образовавшийся тиамина гидроксид изомеризуется в псевдооснование тиамина:
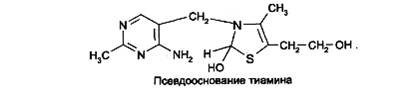
При действии 3-го эквивалента щелочи происходит раскрытие тиазолового кольца с образованием тиольной формы тиамина, которая при дегидратации превращается в циклическую форму тиаминтиола. Окисление последнего приводит к образованию тиохрома:
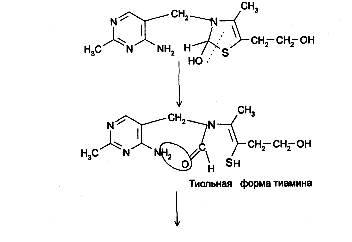
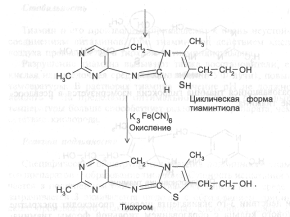
Тиохром образуют также фосфотиамин и кокарбоксилаза, но не бенфотиамин.
Как соли азотистых оснований препараты тиамина взаимодействуют с общеалкалоидными осадительными реактивами (реактивы Вагнера, Драгендорфа, Майера, гетерополикислотами кремневоль-фрамовой, пикриновой, танином и др.) с образованием характерно окрашенных осадков.
2. Методы количественного определения
Химическая структура лекарственных веществ, производных витамина В1, позволяет применить различные методы их химического и физико-химического количественного определения:
1)кислотно-основное титрование (в водной и неводной средах);
2)осадительное титрование (аргентометрия);
3)физико-химические методики (спектрофотометрические, ФЭК, нефелометрические);
4)гравиметрия.
Тиамина бромид количественно определяют гравиметрически в виде комплекса препарата с кремневольфрамовой кислотой.
Для количественного определения тиамина бромида применяют также аргентометрическую методику. Определение проводят в 4 стадии. На 1-й стадии осуществляют нейтрализацию тиамина бромида как NН- кислоты 0,1 М раствором натрия гидроксида.
Далее (2-я стадия) готовят индикатор — железа (III) тиоцианат. Для этого к определенному объему 0,1М раствора аммония тиоцианата добавляют раствор железоаммониевых квасцов.
На 3-й стадии сумму бромидов оттитровывают 0,1М раствором серебра нитрата.
На заключительной, 4-й стадии оттитровывают полученный на 2-й стадии железа (III) тиоцианат 0,1 М раствором серебра нитрата.
Объем 0,1 М раствора серебра нитрата, пошедшего на титрование непосредственно тиамина бромида, рассчитывают по разнице между общим объемом титранта и объемами растворов натрия гидроксида и аммония тиоцианата.
Количественное определение тиамина хлорида проводят методом кислотно-основного титрования в среде ледяной уксусной кислоты (как соли двукислотного основания). Для связывания галогенид-иона добавляют ртути (II) ацетат.
Заключение
Недостаток тиамина ведет к нарушению углеводного обмена, а затем и к другим нарушениям метаболизма (в мышечных тканях накапливаются пировиноградная и молочная кислота), функции нервной системы (проявляются полиневритом и мышечной слабостью), к заболеванию бери-бери, парезам, параличам, кожной патологии.
Применяют препараты тиамина при невритах, невралгиях, радикулите, кожных заболеваниях, а также для профилактики и лечения авитаминоза В1.
Потребность человека в тиамине составляет примерно 1 мг в день.
Препараты витамина В1: тиамина бромид (хлорид) и его коферментные формы кокарбоксилазы гидрохлорид, фосфотиамин и бенфотиамин.
В настоящее время препараты тиамина получают синтетически.
Список литературы
1) www.medkurs.ru
2) www.xumuk.ru
3) Фармацевтическая химия: учебное пособие / под ред. А.П. Арзамасцева. – 3 –е изд., испр. – М.: ГЭОТАР Медиа, 2006.
4) Глущенко Н.Н., Плетнева Т.В., Попков В.А, Фармацевтическая химия – М.: Академия, 2004.
5) Сборник приказов для фармацевта – 2002.
© 2009 База Рефератов