
Рефераты по рекламе
Рефераты по физике
Рефераты по философии
Рефераты по финансам
Рефераты по химии
Рефераты по хозяйственному праву
Рефераты по цифровым устройствам
Рефераты по экологическому праву
Рефераты по экономико-математическому моделированию
Рефераты по экономической географии
Рефераты по экономической теории
Рефераты по этике
Рефераты по юриспруденции
Рефераты по языковедению
Рефераты по юридическим наукам
Рефераты по истории
Рефераты по компьютерным наукам
Рефераты по медицинским наукам
Рефераты по финансовым наукам
Рефераты по управленческим наукам
психология педагогика
Промышленность производство
Биология и химия
Языкознание филология
Издательское дело и полиграфия
Рефераты по краеведению и этнографии
Рефераты по религии и мифологии
Рефераты по медицине
Лабораторная работа: Аналіз субстанції гліцину
Лабораторная работа: Аналіз субстанції гліцину
Кафедра фармацевтичної хімії і фармакогнозії
Курсова робота на тему:
«Аналіз субстанції гліцину та його ЛФ»
Зміст
Вступ
1. Добування
2. Властивості
3. Аналіз субстанції
Висновок
Список літератури
Вступ
В даний час хвороби судин і нервової системи є дуже поширеними. Темп життя дуже швидкий і люди постійно знаходяться в умовах стресу та напруження, а це призводить до виникнення неврозів, депресій, порушення сну, загального виснаження організму в цілому та зниження працездатності. Саме тому препарати гліцину широко призначаються лікарями та мають великий попит в аптеках міста.
Гліцин регулятором обміну речовин, нормалізує й активує процеси захисного гальмування в центральній нервовій системі, зменшує психоемоційну напругу, підвищу розумову працездатність, володіє ГАМК-ергічною, α1-адреноблокуючою, антиоксидантною, антитоксичною дією, регулює діяльність глютамінових рецепторів, за рахунок чого препарат здатний підвищувати розумову працездатність і зменшувати вегето-судинні розлади. Також гліцин полегшу засипання, нормалізує сон і зменшує виразність загально мозкових розладів при шемічному інсульті й черепно мозковій травмі.
Гліцин також назначають при різних функціональних та органічних захворюваннях нервово системи, станах з підвищеною збудливістю та емоційною нестабільністю. Призначається дітям і дорослим при лікуванні астенічних станів, вегето-судинної дистонії, для підвищення розумової працездатності (як засіб, що поліпшує розумові процеси та здатність сприймати і запам'ятовувати інформацію), при психоемоційному напруженні, підвищеної дратівливості, депресивних станах, для нормалізації сну, як засіб, послаблює потяг до алкоголю, що зменшує явища абстиненції; при різних функціональних і органічних захворюваннях нервової системи (порушення мозкового кровообігу, інфекційні захворювання нервової системи, наслідки перенесених черепно-мозкових травм, перинатальні та інші форми енцефалопатії, у тому числ алкогольного походження).
1. Добування
Метод отримання 1
До киплячої суспензії 253 г. (0,8 мол.) гідроокису барію в 500 мл води, яка знаходиться в літровому стакані, додають частинами 61,6 г (0,4 мол.) кислої сірчаної кислоти аміноацетонітрила з такою швидкістю, щоб реакційна маса не пінилась занадто швидко та не виливалась з стакану. Потім на стакан ставлять літрову круглодонну колбу, через яку пропускають холодну водопровідну воду, і місткість стакана кип’ятять до тих пір, доки не зупиниться виділення аміаку; на це знадобиться 6–8 годин. Барій кількісно осаджують додаванням точно розрахованої кількості 50%- сірчаної кислоти. Фільтрат запарюють на водяній бані до об’єму 50–75 мл; по охолодженні випадають кристали гліцину, який відфільтровують. Фільтрат знову запарюють, охолоджують та знову відфільтровують кристали. Цей процес повторюють до тих пір, поки об’єм фільтрату не буде 5 мл. Вихід отриманого таким чином неочищеного гліцину буде 25–27 г. Його піддають систематичній перекристалізаціі з води, знебарвлюючи розчин вуглем; при цьому отримується продукт, який плавиться при 246° чи більше. Промивка всіх послідуючих порцій кристалів 50%-м етиловим спиртом слугує звільненню кристалів з маточника.
![]()
Вихід чистого гліцину: 20–26 г. (67-87% теоретич.).
Корисно додавати невеликий залишок сірчаної кислоти, нагрівати на водяній бані з тим, щоб осад легко фільтрувався та, нарешті, завершують операцію додаванням розведеного розчину гідроксиду барію до тих пір, поки не зупиниться випадіння осаду. Операцію можна закінчити також додаванням невеликого залишку гідроксиду барію, який видаляють додаванням к киплячому розчину вуглекислого амонію.
Метод отримання 2
В 12-літрову круглодонну колбу поміщають 8 л (120 мол.) водного аміаку і при працюючій мішалці послідовно додають 189 г. (2 мол.) монохлороцтової кислоти. Розчин перемішують до повного розчинення хлороцтової кислоти та потім залишають його на 24 години при кімнатній температурі. Безкольоровий чи злегка жовтий розчин запарюють на водяній бані у вакуумі до об’єму приблизно 200 мл.
Концентрований розчин гліцину та хлористого амонію переносять в 2-літровий стакан, колбу ополіскують невеликою кількістю води, яку додають до головної порції. Додаванням води об’єм розчину доводять до 250 мл і гліцин осаджують послідовним додаванням метилового спирту.
При додаванні метилового спирту розчин добре перемішують, після чого його охолоджують в холодильній шафі на протязі 4–6 годин для завершення кристалізації. Потім розчин фільтрують і кристали гліцину промивають, всколомутивши їх попередньо в 500 мл 95%-го метилового спирту. Кристали знову відсмоктують і промивають спершу невеликою кількістю метилового спирту, а потім ефіру. Після сушки на повітрі вихід гліцину дорівнює 108 – 112 г.
![]()
Продукт вміщує невелику кількість хлористого амонію. З метою очистки його розчиняють при нагріванні в 200-215 мл води та розчин взбалтують з 10 г. пермутиту, після чого його фільтрують. Гліцин осаджають додаванням приблизно 5-кратно кількості (по об’єму; приблизно 1250 мл) метилового спирту. Гліцин збирають на воронці Бюхнера, промивають метиловим спиртом и ефіром и сушать на повітрі. Вихід: 96–98 г. (64–65% теоретич.) продукту з температурою потемніння 237° температурою плавлення 240°. Тестування його на наявність хлоридів, так само як і аміачних солей (з реактивом Несслера), дає негативний результат.
2. Властивості
Фізичн властивості:
Зовнішній вигляд: безкольорові кристали;
Молярна маса 75,07 г./моль
Температура плавлення 290С
Густина речовини 1,607 г./см
рКа 2,34
Питома теплота паротворення 528.6 Дж/кг
Питома теплота плавлення 981,1 Дж/кг
Ізоелектрична точка 5,97
Розчинність:
Ацетон: малорозчинний
вода: 57,5 (75°C)
діетиловий ефір: не розчинний піридин: мало розчинний етанол: 0,043 (25°C)
Хімічн властивості
Горіння. Гліцин при горінні розпадається на вуглекислий газ воду та нітроген:
4NH2CH2COOH + 13O2 ![]() 8CO2
8CO2![]() + 10H2O +
2N2 (1)
+ 10H2O +
2N2 (1)
Взаємодія з водою. При взаємодії з водою дисоціює:
NH2CH2COOH + H2O ![]() +NH3CH2COOH
+ OH – NH2CH2COOH + H2O
+NH3CH2COOH
+ OH – NH2CH2COOH + H2O ![]() NH2CH2COO-
+ H3O+ (NH2CH2COOH
NH2CH2COO-
+ H3O+ (NH2CH2COOH ![]() NH2CH2COO-
+ H+) (2)
NH2CH2COO-
+ H+) (2)
Наявність аміногрупи визначає основні властивості, а карбоксильно кислотні, тому α-амінокислоти є амфотерними сполуками. Утворюють солі як з кислотами так і з лугами
Реакції з розчинами основ. При додаванні до гліцину основи NaOH утворюється сіль аміноацетат натрію:
NH2CH2COOH + NaOH ![]() NH2CH2COO–Na+
+ H2O (3)
NH2CH2COO–Na+
+ H2O (3)
(NH2CH2COONa – аміноацетат натрію)
Реакції з розчинами кислот. При додаванні до гліцину сірчано кислоти утворюється сіль сульфату гліцину.
2NH2CH2COOH + H2SO4 ![]() (NH3CH2COOH)2SO4
(сульфат гліцину) (4)
(NH3CH2COOH)2SO4
(сульфат гліцину) (4)
Етерифікація. Гліцин – амінокислота, при додаванні спирту утворюється складний єстер:
NH2CH2COOH + C2H5OH ![]() NH2CH2COOC2H5
+ H2O (5)
NH2CH2COOC2H5
+ H2O (5)
Міжмолекулярна взаємодія амінокислот призводить до утворення пептидів. При взаємодії двох амінокислот утворюється дипептид.
H2N-CH2-C-OH + H-N-CH-COOH![]() H2N-CH2-C-N-CH-COOH (6)
H2N-CH2-C-N-CH-COOH (6)
При нагріванні з нінгідрином утворюється синьо-фіолетове забарвлення (комплекс Руєманна).
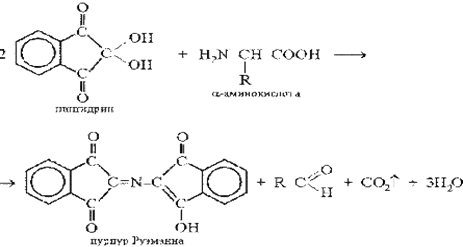 (7)
(7)
3 Аналіз субстанції
Відповідно до ДФУ ідентифікація гліцину проводять:
1. Інфрачервоний спектр субстанції, одержаний у дисках з 1 мг субстанції і 0.4 г. калію броміду, має відповідати спектру ФСЗ гліцину. У раз різниці спектрів окремо розчиняють субстанцію та ФСЗ гліцину в мінімальному об'ємі спирту (60% об/об), упарюють насухо і повторно записують спектри одержаних залишків.
2. На хроматограмі випробовуваного розчину, одержаній у випробуванні «Речовини, виявлювані нінгідрином», має виявлятися основна пляма на рівні основної плями на хроматограмі розчину порівняння, відповідна їй за розміром і забарвленням.
3. 50 мг субстанції розчиняють у 5 мл води Р. До одержаного розчину додають 1 мл розчину натрію гіпохлориту концентрованого, кип'ятять протягом 2 хв., додають 1 мл кислоти хлористоводневої і кип'ятять протягом 4–5 хв. Потім додають 2 мл кислоти хлористоводневої і 1 мл розчину 20 г./л резорцину, кип'ятять протягом 1 хв. і охолоджують. Додають 10 мл води і перемішують. До 5 мл одержаного розчину додають 6 мл розчину натрію гідроксиду розведеного; розчин забарвлюється у фіолетовий колір із зеленувато-жовтою флуоресценцією. Через декілька хвилин забарвлення розчину переходить в оранжеве, потім у жовте, а нтенсивна флуоресценція залишається.
Випробування на чистоту
Розчин. 5.0 г. субстанції розчиняють у воді, вільній від вуглецю діоксиду, і доводять об'єм розчину тим самим розчинником до 50 мл.
Прозорість розчину. Розчин має бути прозорим.
Кольоровість розчину. Забарвлення розчину має бути не інтенсивнішим за еталон Y7.
рН. Від 5.9 до 6.4. 10 мл розчину доводять водою, вільною від вуглецю діоксиду, Р до об'єму 20 мл.
Речовини, виявлювані нінгідрином. Визначення проводять методом тонкошарової хроматографії, використовуючи ТШХ пластинки із шаром силікагелю Р.
Випробовуваний розчин (а). 0.10 г. субстанції розчиняють у вод Р і доводять об'єм розчину тим самим розчинником до 10.0 мл.
Випробовуваний розчин (b). 1.0 мл випробовуваного розчину (а) доводять водою до об'єму 10.0 мл.
Розчин порівняння (а). 10 мг ФСЗ гліцину розчиняють у воді Р і доводять об'єм розчину тим самим розчинником до 10.0 мл.
Розчин порівняння (b). 1.0 мл випробовуваного розчину (а) доводять водою до об'єму 200 мл.
Розчин порівняння (с). 10 мг ФСЗ гліцину та 10 мг ФСЗ аланіну розчиняють у воді Р і доводять об'єм розчину тим самим розчинником до 25 мл.
На лінію старту хроматографічної пластинки наносять 5 мкл (50 мкг) випробовуваного розчину (а), 5 мкл (5 мкг) випробовуваного розчину (b), 5 мкл (5 мкг) розчину порівняння (а), 5 мкл (0.25 мкг) розчину порівняння (b) і 5 мкл (2 мкг гліцину та 2 мкг аланіну) розчину порівняння (с). Пластинку помішають у камеру із сумішшю розчинників кислота оцтова льодяна Р – вода Р – бутанол Р (20:20:60). Коли фронт розчинників пройде 2/3 довжини пластинки, пластинку виймають із камери, сушать при температурі 80°С протягом 30 хв., обприскують розчином нінгідрину і нагрівають при температурі від 100°С до 105°С протягом 15 хв.
На хроматограмі випробовуваного розчину (а) будь-яка пляма, крім основної, не має бути інтенсивнішою за пляму на хроматограмі розчину порівняння (b) (0.5%).
Результати аналізу вважаються вірогідними, якщо на хроматограм розчину порівняння (с) виявляються дві чітко розділені плями. А
Хлориди. Не більше 0.0075% (75 ррm). 0.67 г. субстанц розчиняють у воді Р і доводять об'єм розчину тим самим розчинником до 15 мл. Одержаний розчин має витримувати випробування на хлориди.
Важкі метали. Не більше 0.001% (10 ррm). 12 мл розчину мають витримувати випробування на важкі метали. Еталон готують із використанням еталонного розчину свинцю (1 ррm Рb).
Втрата в масі при висушуванні. Не більше 0.5%. 1.000 г. субстанції сушать при температурі від 100°С до 105°С протягом 2 год.
Сульфатна зола. Не більше 0.1%. Визначення проводять з 1.0 г. субстанції.
Нефармакопейні методи
1. При нагріванні з нінгідрином утворюється синьо-фіолетове забарвлення (комплекс Руєманна). В пробірку наливають 1 мл 1%-го розчину гліцину и 0,5 мл 1%-го розчину нінгидрину. Вміст пробірки обережно нагрівають до появи синьо-фіолетового забарвлення. (Див.хім.реакції №7.)
2. Реакція Циммермана.
До 2 мл 0,1%-го розчину гліцину, доведеного додаванням 10%-го розчином основи до рН = 8, доливають 0,5 мл водного розчину о-фталевого диальдегіду. Реакційна суміш починає забарвлюватись в яскраво-зелений колір. Через декілька хвилин випада зелений осад.
Кількісне визначення
Відповідно до ДФУ кількісне визначення гліцину проводять:
1. Проводять метод неводної ацидиметрії.
70.0 мг субстанції розчиняють у 3 мл кислоти мурашиної безводної, додають 30 мл кислоти оцтової льодяної Р і відразу титрують 0.1 М розчином кислоти хлорної потенціометрично.
1 мл 0.1 М розчину кислоти хлорної відповідає 7.51 мг С2Н51ЧО2.
Нефармокопейні методи
1. Алкаліметрія за методом Серенсена (формольне титрування).
До розчину амінооцетової кислоти додають нейтралізований за фенолфталеїном формалін. При цьому утворюється N‑метиленова похідна, а звільнена карбоксильна група може бути від титрована натрію гідроксидом:
R-CH-COO![]() + HC-H
+ HC-H![]() R-CH-COOH + H2O
R-CH-COOH + H2O
NH3![]() N=CH2
N=CH2
2. Метод К’єльдаля. Речовину мінералізують кип’ятінням у спеціальному приладів присутності K2SO4,і концентровано H2SO4. Амоніак, що виділяється, відганяють у колбу-приймач, що містить розчин борної кислоти. Утворюються амонію мета- тетра-борати, які відтитровують розчином HCl за змішаним індикатором (суміш метилового червоного і метиленового синього у співвідношенні 2:1).Для підвищення точності результатів паралельно проводять контрольний дослід.
H-CH-COOH + H2SO4 ![]() CO2
CO2![]() + H2O + NH4HSO4
+ H2O + NH4HSO4
NH2
NH4HSO4 + 2NaOH ![]() NH3
NH3![]() + 2H2O +
Na2SO4
+ 2H2O +
Na2SO4
NH3 + H3BO3 ![]() NH4BO2
+ H2O
NH4BO2
+ H2O
2NH3 + 4H3BO3 ![]() (NH4)2B4O7
+ 5H2O
(NH4)2B4O7
+ 5H2O
NH4BO2 + HCl + H2O ![]() NH4Cl + H3BO3
NH4Cl + H3BO3
(NH4)2B4O7 + 5H2O
+ 2HCl ![]() 2NH4Cl + 4 H3BO3
2NH4Cl + 4 H3BO3
3. Спектрофотометрія за реакцією з нінгідрином (при 570 нм пік)
4. Аналіз лікарської форми
Аналіз таблеток «Гліцину»
Контроль якості препарату «Гліцин таблетки під’язичні 0,1г» для кожної серії проводиться в лабораторіях відділів контролю якості на підприємствах, виробляючих лікарськ засоби, та в тестувальних лабораторіях центрів по сертифікації.
Спочатку готують суміш розчиненням 2,5 г розтертих в порошок таблеток в 250 мл води очищеної. Розчинення роблять протягом 20 хв. при 37С в пристрої для визначення розчинності типу «лопастна мішалка» «Ервека» при швидкості обертання мішалки 150 об/хв.
Потім суміш витримують протягом 10 хв.
Відбирають 4 мл суміші та визначають світлопропускання на спектрофотометрі при довжин хвилі 700±2 нм в кюветі з товщиною слою 10 мм відносно води очищеної.
Величина світлопропускання в діапазоні значень 50–70% відповідає препарату «Гліцин таблетки під’язичні 0,1г» належної якості, які мають необхідний терапевтичний ефект та до складу яких входить амінооцтова кислоти 0,100г, метилцелюлоза водорозчинна марки МЦ‑100 0,001г, магній стеариновокислий 0,001г.
Для цього відбирають 1 мл отриманої суміші до її витримки, до якої додають 9 мл води очищеної ті 0,2 мл розчину нінгідрину в ацетоні (0,85 г. нінгідрину в 50 мл ацетона). Склад нагрівають до появи сине-фіолетового забарвлення.
Пляма на хроматограмі, яка відповідає амінооцетовій кислоті, отримана при досліджуванн препарату на посторонні домішки, повинно бути на одному рівні з плямою стандартного зразку гліцину.
Інш етапи контролю проводяться за стандартними методиками. Перевіряється час распадаемост таблеток, яке повинно відповідати діапазону 10 20 хв. Перевіряється міцність таблеток на раздавлюваність.
Підтвердження взаємозв'язку певного якісного складу препарату «Гліцин таблетки під'язиков 0,1 г» і величини світлопропускання ілюструється у таблиці, що відображає результати аналізів, проведених у відповідності з поданими нижче прикладами.
Приклад 1
2,5 г таблеток препарату «Глицин таблетки під'язикові 0,1 г» розчиняли в 250 мл води протягом 20 хв при температурі 37С в приладі для визначення розчинення типу «лопатевого мішалки» «Ервека». Швидкість обертання мішалки 150 об / хв. Таблетки з елементами мармуровість мали час розпаду в межах 10 – 20 хв, міцність – в межах 10-30 Н. Таблетки містили 0,1±7,5% амінооцтової кислоти, 0,001±7,5% водорозчинний метилцелюлози марки МЦ -100 та 0,001±7,5% магнію стеариновокислого в одній таблетці. Після повного розчинення таблеток протягом 20 хв суміш витримували протягом 10 хвилин, після чого обирали 4 мл і в кюветі з товщиною шару 10 мм фотометріровали на спектрофотометрі проти розчинника (вода очищена) при довжин хвилі 700±2 нм. Коефіцієнт пропускання склав 65%.
Приклад 2
2,5 г розтерта в порошок таблеток препарату «Гліцин таблетки під'язикові 0,1 г» розчиняли в 250 мл води протягом 20 хв при температурі 37С в приладі для визначення розчинення типу «лопатевого мішалка» «Ервека». Швидкість обертання мішалки 150 об / хв. Після розчинення таблеток протягом 20 хв суміш витримували протягом 10 хвилин, після чого обирали 4 мл і в кюветі з товщиною шару 10 мм фотометріровали на спектрофотометр проти розчинника (вода очищена) при довжині хвилі 700±2 нм. Коефіцієнт пропускання склав 63%.
Приклад 3
1,25 г. розтерта в порошок таблеток препарату «Гліцин таблетки під'язикові 0,1 г» аналогічно прикладу 2 розчиняли і проводили спекторофотометрічне дослідження. Коефіцієнт пропускання склав 79%.
Приклад 4
5 г розтертих в порошок таблеток препарату «Гліцин таблетки під'язикові 0,1 г» аналогічно прикладу 2 розчиняли і проводили спекторофотометрічне дослідження. Коефіцієнт пропускання склав 37%.
Приклад 5
2,5 г розтертих в порошок таблеток, що містять в одній таблетці 0,099 г. амінооцтової кислоти, 0,002 г. метилцелюлози і 0,001 г. магнію стеариновокислого розчиняли і проводили спекторофотометрічне дослідження аналогічно прикладу 2. Коефіцієнт пропускання склав 79%.
Приклад 6
2,5 г розтерта в порошок таблеток, що містять в одній таблетці 0,1 г амінооцтовоїкислоти, 0,001 г. карбоксіметилцелюлози і 0,001 г. магнію стеариновокислого розчиняли і проводили спекторофотометрічне дослідження аналогічно прикладу 2. Коефіцієнт пропускання склав 75-85%.
Приклад 7
2,5 г розтерта в порошок таблеток, що містять в одній таблетці 0,1 г аміно оцтової кислоти, 0,001 г. метилцелюлози водорозчинній марки МЦ 100 і 0,001 г. кальцію стеариновокислого розчиняли і проводили спекторофотометрічне дослідження аналогічно прикладу 2. Коефіцієнт пропускання склав 45%.
| пример | Якісний склад | Кількісний склад, % ± 7,5% | Коефіцієнт світлопропускания% |
| 1 | амінооцтова кислота водорозчинна метилцелюлоза марки МЦ‑100 магній стеариновокислий, вода |
0,98 |
65 (60±16,6) |
| 2 | амінооцтова кислота водорозчинна метилцелюлоза марки МЦ‑100 магній стеариновокислий, вода |
0,98 |
63 (60±16,6) |
| 3 | амінооцтова кислота водорозчинна метилцелюлоза марки МЦ‑100 магній стеариновокислий, вода |
0,49 |
79 (75±5) |
| 4 | аминоуксусная кислота водорастворимая метилцеллюлоза марки МЦ‑100 магний стеариновокислый вода |
1,96 |
37 (36±10) |
| 5 | амінооцтова кислота водорозчинна метилцелюлоза марки МЦ‑100 магній стеариновокислий, вода |
0,97 |
78 (75±5) |
| 6 | амінооцтова кислота водорозчинна метилцелюлоза марки МЦ‑100 магній стеариновокислий, вода |
0,98 |
80 (80±6) |
| 7 | амінооцтова кислота водорозчинна метилцелюлоза марки МЦ‑100 магній стеариновокислий, вода |
0,98 |
45 |
Список літератури
1. Безлугий П.О., Українець І.В., Таран С.Г. «Фарм. хімія. Навч. посіб. для студ. вищ. фарм. закл.»
2. Габріелян О.С. и др. «Хімія 10 кл.» М., Дрофа, 2002;
3. Гузей Л.С., Суровцева Р.П., Лисова Г.Г. «Химия 11 кл.» Дрофа, 1999.
4. Полянська А.С., Шевелєва А.О. «Методичні розробки до лабораторних робіт: Амінокислоти та білки». Л., 1996, 37 с.
5. Пустовалова Л.М. «Практикум по біохімії». 1999, 541 с.
6. Родіонов В.М. «Посібник до практичних занять з органічної хімії.» М., 1954–111 с.
7. Рудзитис Г.Е., Фельдман Ф.Г. «Хімія 10 кл.» М., Просвіта, 2001.
8. Соловйов Н.А. «Лабораторні роботи з біологічної хімії.», 1996, 70 с.
9. Філіппович Ю.Б., Єгорова Т.А., Севастьянова Г.А. Практикум з загальної біохімії. М., 1992, 311 с.
10. http://www.geocities.com/bioelectrochemistry/sorensen.htm
© 2009 База Рефератов