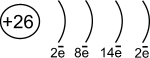Рефераты по рекламе
Рефераты по физике
Рефераты по философии
Рефераты по финансам
Рефераты по химии
Рефераты по хозяйственному праву
Рефераты по цифровым устройствам
Рефераты по экологическому праву
Рефераты по экономико-математическому моделированию
Рефераты по экономической географии
Рефераты по экономической теории
Рефераты по этике
Рефераты по юриспруденции
Рефераты по языковедению
Рефераты по юридическим наукам
Рефераты по истории
Рефераты по компьютерным наукам
Рефераты по медицинским наукам
Рефераты по финансовым наукам
Рефераты по управленческим наукам
психология педагогика
Промышленность производство
Биология и химия
Языкознание филология
Издательское дело и полиграфия
Рефераты по краеведению и этнографии
Рефераты по религии и мифологии
Рефераты по медицине
Курсовая работа: Методические особенности изучения темы "Железо" на уроках химии в средней школе
Курсовая работа: Методические особенности изучения темы "Железо" на уроках химии в средней школе
ВВЕДЕНИЕ
Железо играло и играет исключительную роль в материальной истории человечества. Первое металлическое железо, попавшее в руки человека, имело, вероятно, метеоритное происхождение. Руды железа широко распространены и часто встречаются даже на поверхности Земли, но самородное железо на поверхности крайне редко. Вероятно, еще несколько тысяч лет назад человек заметил, что после горения костра в некоторых случаях наблюдается образование железа из тех кусков руды, которые случайно оказались в костре. При горении костра восстановление железа из руды происходит за счет реакции руды как непосредственно с углем, так и с образующимся при горении оксидом углерода (II) СО. Возможность получения железа из руд существенно облегчило обнаружение того факта, что при нагревании руды с углем возникает металл, который далее можно дополнительно очистить при ковке. Получение железа из руды с помощью сыродутного процесса было изобретено в Западной Азии во 2-м тысячелетии до нашей эры. Период с 9 – 7 века до нашей эры, когда у многих племен Европы и Азии развилась металлургия железа, получил название железного века, пришедшего на смену бронзовому веку. Усовершенствование способов дутия (естественную тягу сменили меха) и увеличение высоты горна (появились низкошахтные печи — домницы) привело к получению чугуна, который стали широко выплавлять в Западной Европе с 14 века. Полученный чугун переделывали в сталь. С середины 18 века в доменном процессе вместо древесного угля начали использовать каменно-угольный кокс. В дальнейшем способы получения железа из руд были значительно усовершенствованы, и в настоящее время для этого используют специальные устройства — домны, кислородные конвертеры, электродуговые печи.
Целью моей работы является освещение основных наиболее остро стоящих экологических проблем, связанных с железом и его соединениями, и возможные пути их решения.
Задачи:
1. Обзор состояния данного вопроса в современной российской школе.
2. Анализ школьных программ и учебников, а также другой литературы, показывающих как тема: «Железо и его соединения»изучаются в средней школе.
3. Составить план урока, на котором была бы успешно проведена экологизация знаний.
ГЛАВА 1. ИЗУЧЕНИЕ ТЕМЫ: «ЖЕЛЕЗО И ЕГО СОЕДИНЕНИЙ» В ШКОЛЬНОМ КУРСЕ ХИМИИ
Историческая справка
В земной коре железо распространено достаточно широко — на его долю приходится около 4,1% массы земной коры (4-е место среди всех элементов, 2-е среди металлов). Известно большое число руд и минералов, содержащих железо. Наибольшее практическое значение имеют красные железняки (руда гематит, Fe2O3; содержит до 70% Fe), магнитные железняки (руда магнетит, Fe3О4; содержит 72,4% Fe), бурые железняки (руда гидрогетит НFeO2·nH2O), а также шпатовые железняки (руда сидерит, карбонат железа, FeСО3; содержит около 48% Fe). В природе встречаются также большие месторождения пирита FeS2 (другие названия — серный колчедан, железный колчедан, дисульфид железа и другие), но руды с высоким содержанием серы пока практического значения не имеют. По запасам железных руд Россия занимает первое место в мире. В морской воде 1·10–5 — 1·10–8% железа.
1.2 Тема «Железо и его соединения» в школьных программах по химии
В программе школьного курса химии на изучении темы «Железо и его соединения» отводится 5 часов; эта тема разбита на следующие подразделы: Общие понятия о положении железа в периодической системе химических элементов и строение атома. Основные методы получения железа-восстановление из оксидов железа и электролиз водных растворов солей железа. Физические, химические свойства и применение. Основные соединения железа и их получение. Экологические аспекты данной темы в школьной литературе изложены очень поверхностно или не изложены вовсе.
В школьных учебниках «Химия.9 класс»/Г. Е. Рудзитис, Ф. Г. Фельдман, «Химия. 9класс»/Н. С. Ахметов, и Пособие по химии для поступающих в вузы/ Г. П. Хомченко, на эту тему выделено три основных параграфа: § 1.Положение железа в периодической системе химических элементов и строение атома § 2.Нахождение железа в природе,его получение, свойства и применение § 3.Соединения железа, и мы будем рассматривать каждый параграф более подробно.
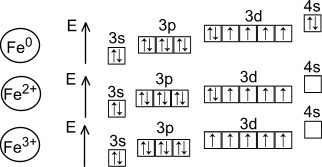
§ 1. Положение железа в периодической системе химических элементов и строение атома
Fe
d- элемент VIII группы; порядковый номер 26; атомная масса – 56; (26p11; 30 n01), 26ē[1]
|
|
1s22s22p63s23p63d64s2 |
Металл средней активности, восстановитель.
Основные степени окисления - +2, +3
§ 2. Нахождение железа в природе,его получение и свойства
Нахождение в природе.
Железо является вторым по распространенности металлом в природе (после алюминия). В свободном состоянии железо встречается только в метеоритах, падающих на землю [2]. Наиболее важные природные соединения:
Fe2O3 3H2O - бурый железняк;
Fe2O3 - красный железняк;
Fe3O4(FeO Fe2O3) - магнитный железняк;
FeS2 - железный колчедан (пирит).
Соединения железа входят в состав живых организмов.
Получение железа.
В промышленности железо получают восстановлением его из железных руд углеродом (коксом) и оксидом углерода (II) в доменных печах [1, 3]. Химизм доменного процесса следующий:
C + O2 = CO2,
CO2 + C = 2CO.
3Fe2O3 + CO = 2Fe3O4 + CO2,
Fe3O4 + CO = 3FeO + CO2,
FeO + CO = Fe + CO2.
Его также можно получить:
1)восстановлением железа
из его оксида, например, ![]() водородом при нагревании;
водородом при нагревании;
2)восстановлением железа
из его оксидов ![]() и
и ![]() алюминотермическим методом;
алюминотермическим методом;
3)электролизом водных растворов солей железа (II) [1].
Физические свойства.
Железо – серебристо серый металл, обладает большой ковкостью, пластичностью и сильными магнитными свойствами. Плотность железа – 7,87 г/см3, температура плавления 1539°С [1].
У Хомченко [3] также
написано, что железо легко намагничивается и размагничивается, а потому
применяется в качестве сердечников динамомашин и электромоторов. Кроме того,
железо состоит из четырех стабильных изотопов с массовыми числами 54,
56(основной), 57 и 58. Применяются радиоактивные изотопы ![]() и
и ![]() .
.
Химические свойства
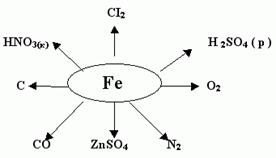
В реакциях железо является восстановителем. Однако при обычной температуре оно не взаимодействует даже с самыми активными окислителями (галогенами, кислородом, серой), но при нагревании становится активным и реагирует с ними:
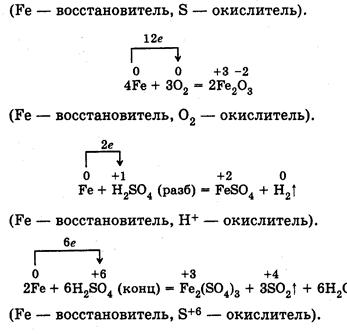
2Fe + 3Cl2 = 2FeCl3 Хлорид железа (III)
3Fe + 2O2 = Fe3O4(FeO · Fe2O3) Оксид железа (II,III)
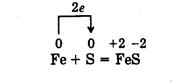
Fe + S = FeS Сульфид железа (II)
При очень высокой температуре железо реагирует с углеродом, кремнием и фосфором:
3Fe + C = Fe3C Карбид железа (цементит)
3Fe + Si = Fe3Si Силицид железа
3Fe + 2P = Fe3P2 Фосфид железа (II)
Железо реагирует со сложными веществами.
Во влажном воздухе железо быстро окисляется (корродирует):
4Fe + 3O2 + 6H2O = 4Fe(OH)3,
O
Fe(OH)3 = Fe
O – H + H2O
Ржавчина
Железо находится в середине электрохимического ряда напряжений металлов, поэтому является металлом средней активности. Восстановительная способность у железа меньше, чем у щелочных, щелочноземельных металлов и у алюминия. Только при высокой температуре раскаленное железо реагирует с водой(700-900):
3Fe + 4H2O = Fe3O4 + 4H2
Железо реагирует с разбавленными серной и соляной кислотами, вытесняя из кислот водород:
Fe + 2HCl = FeCl2 + H2
Fe + H2SO4 = FeSO4 + H2
При обычной температуре железо не взаимодействует с концентрированной серной кислотой, так как пассивируется ею [3]. При нагревании концентрированная H2SO4 окисляет железо до сульфита железа (III):
2Fe + 6H2SO4 = Fe2(SO4)3 + 3SO2 + 6H2O.
Разбавленная азотная кислота окисляет железо до нитрата железа (III):
Fe + 4HNO3 = Fe(NO3)3 + NO + 2H2O.
Концентрированная азотная кислота пассивирует железо.
Из растворов солей железо вытесняет металлы, которые расположены правее его в электрохимическом ряду напряжений:
Fe + CuSO4 = FeSO4 + Cu, Fe0 + Cu2+ = Fe2+ + Cu0.
Применение и биологическая роль железа и его соединений.
Важнейшие сплавы железа – чугуны и стали являются основными конструкционными материалами практически во всех отраслях современного производства [1].
Хлорид железа (III) FeCl3 применяется для очистки воды. В органическом синтезе FeCl3 применяется как катализатор. Нитрат железа Fe(NO3)3 · 9H2O используют при окраске тканей.
Железо является одним из важнейших микроэлементов в организме человека и животных (в организме взрослого человека содержится в виде соединений около 4 г Fe). Оно входит в состав гемоглобина, миоглобина, различных ферментов и других сложных железобелковых комплексов, которые находятся в печени и селезенке. Железо стимулирует функцию кроветворных органов [2, 3].
§ 3.Соединения железа
Соединения железа (II)
Оксид железа (II) FeO – черное кристаллическое вещество, нерастворимое в воде. Оксид железа (II) получают восстановлением оксида железа(II,III) оксидом углерода (II):
Fe3O4 + CO = 3FeO + CO2.
Оксид железа (II) – основной оксид, легко реагирует с кислотами, при этом образуются соли железа(II):
FeO + 2HCl = FeCl2 + H2O, FeO + 2H+ = Fe2+ + H2O.
Гидроксид железа (II) Fe(OH)2 – порошок белого цвета, не растворяется в воде. Получают его из солей железа (II) при взаимодействии их со щелочами:
FeSO4 + 2NaOH = Fe(OH)2¯ + Na2SO4,
Fe2+ + 2OH- = Fe(OH)2¯.
Гидроксид железа () Fe(OH)2 проявляет свойства основания, легко реагирует с кислотами:
Fe(OH)2 + 2HCl = FeCl2 + 2H2O,
Fe(OH)2 + 2H+ = Fe2+ + 2H2O.
При нагревании гидроксид железа (II) разлагается:
Fe(OH)2 = FeO + H2O.
Соединения со степенью окисления железа +2 проявляют восстановительные свойства, так как Fe2+ легко окисляются до Fe+3:
Fe+2 – 1e = Fe+3
Так, свежеполученный зеленоватый осадок Fe(OH)2 на воздухе очень быстро изменяет окраску – буреет. Изменение окраски объясняется окислением Fe(OH)2 в Fe(OH)3 кислородом воздуха:
4Fe+2(OH)2 + O2 + 2H2O = 4Fe+3(OH)3.
Восстановительные свойства проявляют и соли двухвалентного железа, особенно при действии окислителей в кислотной среде. Например, сульфат железа (II) восстанавливает перманганат калия в сернокислотной среде до сульфата марганца (II):
10Fe+2SO4 + 2KMn+7O4 + 8H2SO4 = 5Fe+32(SO4)3 + 2Mn+2SO4 + K2SO4 + 8H2O.
Качественная реакция на катион железа (II).
Реактивом для определения катиона железа Fe2+ является гексациано (III) феррат калия (красная кровяная соль) K3[Fe(CN)6]:
3FeSO4 + 2K3[Fe(CN)6] = Fe3[Fe(CN)6]2¯ + 3K2SO4.
При взаимодействии ионов [Fe(CN)6]3- с катионами железа Fe2+ образуется темно-синий осадок – турнбулева синь:
3Fe2+ +2[Fe(CN)6]3- = Fe3[Fe(CN)6]2¯ [3].
Соединения железа (III)
Оксид железа (III) Fe2O3 порошок бурого цвета, не растворяется в воде. Оксид железа (III) получают:
А) разложением гидроксида железа (III):
2Fe(OH)3 = Fe2O3 + 3H2O
Б) окислением пирита (FeS2):
4Fe+2S2-1 + 11O20 = 2Fe2+3O3 + 8S+4O2-2.
![]()
![]()
![]() Fe+2 – 1e ® Fe+3
Fe+2 – 1e ® Fe+3
2S-1 – 10e ® 2S+4
![]() O20 + 4e ® 2O-2 11e
O20 + 4e ® 2O-2 11e
Оксид железа (III) проявляет амфотерные свойства:
А) взаимодействует с твердыми щелочами NaOH и KOH и с карбонатами натрия и калия при высокой температуре:
Fe2O3 + 2NaOH = 2NaFeO2 + H2O,
Fe2O3 + 2OH- = 2FeO2- + H2O,
Fe2O3 + Na2CO3 = 2NaFeO2 + CO2.
Феррит натрия
Гидроксид железа (III) получают из солей железа (III) при взаимодействии их со щелочами:
FeCl3 + 3NaOH = Fe(OH)3¯ + 3NaCl,
Fe3+ + 3OH- = Fe(OH)3¯.
Гидроксид железа (III) является более слабым основанием, чем Fe(OH)2, и проявляет амфотерные свойства (с преобладанием основных). При взаимодействии с разбавленными кислотами Fe(OH)3 легко образует соответствующие соли:
Fe(OH)3 + 3HCl « FeCl3 + H2O
2Fe(OH)3 + 3H2SO4 « Fe2(SO4)3 + 6H2O
Fe(OH)3 + 3H+ « Fe3+ + 3H2O
Реакции с концентрированными растворами щелочей протекают лишь при длительном нагревании. При этом получаются устойчивые гидрокомплексы с координационным числом 4 или 6:
Fe(OH)3 + NaOH = Na[Fe(OH)4],
Fe(OH)3 + OH- = [Fe(OH)4]-,
Fe(OH)3 + 3NaOH = Na3[Fe(OH)6],
Fe(OH)3 + 3OH- = [Fe(OH)6]3-.
Соединения со степенью окисления железа +3 проявляют окислительные свойства, так как под действием восстановителей Fe+3 превращается в Fe+2:
Fe+3 + 1e = Fe+2.
Так, например, хлорид железа (III) окисляет йодид калия до свободного йода:
2Fe+3Cl3 + 2KI = 2Fe+2Cl2 + 2KCl + I20
Качественные реакции на катион железа (III)
А) Реактивом для обнаружения катиона Fe3+ является гексациано (II) феррат калия (желтая кровяная соль) K2[Fe(CN)6].
При взаимодействии ионов [Fe(CN)6]4- с ионами Fe3+ образуется темно-синий осадок – берлинская лазурь:
4FeCl3 + 3K4[Fe(CN)6] « Fe4[Fe(CN)6]3¯ +12KCl,
4Fe3+ + 3[Fe(CN)6]4- = Fe4[Fe(CN)6]3¯.
Б) Катионы Fe3+ легко обнаруживаются с помощью роданида аммония (NH4CNS). В результате взаимодействия ионов CNS-1 с катионами железа (III) Fe3+ образуется малодиссоциирующий роданид железа (III) кроваво-красного цвета:
FeCl3 + 3NH4CNS « Fe(CNS)3 + 3NH4Cl,
Fe3+ + 3CNS1- « Fe(CNS)3 [1,3]
ГЛАВА II. ЭКОЛОГИЧЕСКИЕ АСПЕКТЫ, СВЯЗАННЫЕ С ИЗУЧЕНИЕМ ТЕМЫ: « ЖЕЛЕЗО И ЕГО СОЕДИНЕНИЯ»
Железо присутствует в организмах всех растений и животных как микроэлемент, то есть в очень малых количествах (в среднем около 0,02%). Однако железобактерии, использующие энергию окисления железа (II) в железо (III) для хемосинтеза, могут накапливать в своих клетках до 17-20% железа. Основная биологическая функция железа участие в транспорте кислорода (O) и окислительных процессах. Эту функцию железа выполняет в составе сложных белков — гемопротеидов, простетической группой которых является железопорфириновый комплекс — гем. Среди важнейших гемопротеидов дыхательные пигменты гемоглобин и миоглобин, универсальные переносчики электронов в реакциях клеточного дыхания, окисления и фотосинеза цитохромы, ферменты каталоза и пероксида, и других. У некоторых беспозвоночных железосодержащие дыхательные пигменты гелоэритрин и хлорокруорин имеют отличное от гемоглобинов строение. При биосинтезе гемопротеидов железо переходит к ним от белка ферритина, осуществляющего запасание и транспорт железа. Этот белок, одна молекула которого включает около 4 500 атомов железа, концентрируется в печени, селезенке, костном мозге и слизистой кишечника млекопитающих и человека. Суточная потребность человека в железе (6-20 мг) с избытком покрывается пищей (железом богаты мясо, печень, яйца, хлеб, шпинат, свекла и другие). В организме среднего человека (масса тела 70 кг) содержится 4,2 г железа, в 1 л крови — около 450 мг. При недостатке железа в организме развивается железистая анемия, которую лечат с помощью препаратов, содержащих железо. Препараты железа применяются и как общеукрепляющие средства. Избыточная доза железа (200 мг и выше) может оказывать токсичное действие. Железо также необходимо для нормального развития растений, поэтому существуют микроудобрения на основе препаратов железа [4,5]. Однако железо может представлять определенную экологическую опасность для окружающей среды, и это следует также рассматривать при изучении темы: «Железо и его соединения». Рассмотрим экологические проблемы, связанные с железом.
В зонах металлургических комбинатов в твердых выбросах содержится от22000 до 31000 мг/кг железа. В прилегающие к комбинатам почвы поступает до 31-42 мг/кг железа. Вследствие этого железо накапливается в огородных культурах [6].
Содержание железа в составе сырого осадка, выпадающего в первичных отстойниках крупного промышленного города, может достигать 1428 мг/кг. Пыль, дым промышленных производств могут содержать большие количества железа в виде аэрозолей железа, его оксидов, руд.
Пыль железа или его оксидов образуется при заточке металлического инструмента, очистке деталей от ржавчины, прокате железных листов, электросварке и при других производственных процессах, в которых имеют место железо или его соединения. Железо может накапливаться в почвах, водоемах, воздухе, живых организмах [6,7].
Основные минералы железа подвергаются в природе фотохимическому разрушению, комплексообразованию, микробиологическому выщелачиванию, в результате чего, железо из труднорастворимых минералов переходит в водные объекты.
Железосодержащие минералы окисляются бактериями типа Th. Ferrooxidans. Пирит – обычный примесный компонент угольных месторождений, и его выщелачивание приводит к закислению шахтных вод. По одной из оценок, в1932г. в реку Огайо (США) с шахтными водами поступило около 3 млн. тонн H2SO4. Микробиологическое выщелачивание железа осуществляется не только за счет окисления, но и при восстановлении окисленных руд. В нем принимают участие микроорганизмы относящиеся к разным группам. В частности, восстановление Fe3+ до Fe2+ осуществляют представители родов Bacillus и Pseudomonas, а так же некоторые грибы.
Упомянутые здесь широко распространенные в природе процессы протекают так же в отвалах горнорудных предприятий, металлургических комбинатов, производящих большое количество отходов (шлаки, огарки и т.п.). С дождевыми, паводковыми и грунтовыми водами высвобождающиеся из твердых матриц металлы переносятся в реки и водоемы. Железо находится в природных водах в разных состояниях и формах: в истинно растворенной форме входит в состав донных отложений и гетерогенных систем (взвеси и коллоиды).
Донные отложения рек и водоемов выступают в качестве накопителя железа. При определенных условиях железо может высвобождаться из них, в результате чего происходит вторичное загрязнение воды [8].
В воздух рабочей зоны на металлургических, предприятиях поступает пыль, аэрозоли из частиц железа и его соединений.
При воздействии на кожу возможны аллергические дерматиты, при вдыхании такого воздуха происходит раздражение дыхательных путей, разрушение легких, плевры, нарушения функции печени, желудочные заболевания. Поэтому установлено ПДК (Предельно Допустимая Концентрация) для железосодержащих частиц в воздухе рабочей зоны в зависимости от типа частиц от 2 до 4мг/м3.
При сгорании железного порошка, при операциях, связанных с работой электрической дуги, в окружающую атмосферу поступает дым оксида железа Fe2O4, который вызывает патологические изменения функции легких. ПДК для Fe2O3 в воздухе (в пересчете на Fe) – 0,04мг/м3.
Сульфаты и хлориды железа являются наиболее токсичными вредными примесями. ПДК для сульфата (в пересчете на Fe) в атмосферном воздухе –0,007 мг/м3, для хлорида – 0,004 мг/м3.
Аэрозоли (пыль, дым) железа и его оксидов, руд и других соединений при длительном воздействии откладываются в легких и вызывают специфическое заболевание легких – сидероз. Различают, так называемый «красный сидероз», вызываемый оксидом железа (III) и «черный сидероз», возникающий от вдыхания пыли железа, его карбонатов и фосфатов.
У рабочих, обрабатывающих пириты, наблюдаются желудочные заболевания (гастриты, дуодениты) [6].
У рабочих доменного и мартеновского производств наблюдается нарушение обоняния.Среди электросварщиков, сталеваров часты воспалительные заболевания верхних дыхательных путей.
У рабочих железорудных шахт и горнообогатительных фабрик особенно часты хронические бронхиты, иногда осложненные астмой, эмфиземой легких. Встречаются стоматиты, воспаления десен, поражения зубов, поражения слизистой рта.
Мероприятия, обеспечивающие безопасность работы в атмосфере с повышенным содержанием частиц железа и его соединений, заключаются в очистке воздуха от вредных примесей, в эффективной вентиляции помещений, в применении спецодежды, респираторов, очков.
Реальную опасность при приеме внутрь представляют железо, поступающее в организм в составе лекарственных веществ и сульфат железа (II). Токсические дозы FeSO4 или чистого железа (для человека ЛД = 200-250 мг/кг) приводят к смертельному исходу в результате химического ожога внутренних органов.
Токсичность соединений железа в воде зависит от pH. В щелочной среде токсичность возрастает. От избыточного содержания железа в воде могут гибнуть рыбы, водоросли. Большую опасность представляют сточные воды и шламы производств, связанных с переработкой железосодержащих продуктов.
Подпороговые концентрации в воде водоемов: сульфат и нитрат железа (III), гидроксид железа (II) – 0,5 мг/л; хлорид железа (III) – 0,9 мг/л.
Соединения железа (II) обладают общим токсическим действием. Соединения железа (III) менее ядовитые, но действуют прижигающе на пищеварительный канал и вызывают рвоту.
ПДК железа в питьевой воде 0,3 мг/л.
В природных водоемах, например, в Ладожском озере, в Неве, содержание железа меньше 0,3 мг/л. Перед поступлением в сети городского водоснабжения вода из водоемов подвергается фильтрации и действию коагулянтов, которые вместе с органическими примесями удаляют и часть железа.
Обработка воды с повышенным содержанием железа заключается в фильтровании на механических фильтрах (антрацит), коагуляции, глинозем Al2(SO4)3), иногда - в обработке магнитными полями (в случае магнитных форм железа).
Профилактические мероприятия, обеспечивающие безопасные условия труда при воздействии на работающих железа и его соединений определяются нормативными документами применительно к конкретным условиям производства [7,8].
В этой главе мы рассмотрели некоторые (на самом деле их гораздо больше) экологические вопросы, связанные с железом и его соединениями, а также способами устранения. И в следующей главе мы будем рассматривать, способы проведения уроков в школе по этой теме.
ГЛАВА 3. ИЗУЧЕНИЕ ТЕМЫ «ЖЕЛЕЗО И ЕГО СОЕДИНЕНИЯ» НА УРОКЕ ПО ХИМИИ В СРЕДНЕЙ ШКОЛЕ
3.1 План урока
Железо: его строение и свойства
“Век девятнадцатый, железный,
Воистину жестокий век!
Тобою в мрак ночной, беззвездный
Беспечный брошен человек!”
Цели урока:
· сформировать представление о физических и химических свойствах железа в зависимости от проявляемой им степени окисления и природы окислителя;
· развивать теоретическое мышление учащихся и их умения прогнозировать свойства вещества, опираясь на знания о его строении;
· развивать понятийное мышление таких операций, как анализ, сравнение, обобщение, систематизация;
· развивать такие качества мышления, как объективность, лаконизм и ясность, самоконтроль и активность.
Задачи урока:
· актуализировать знания учащихся по теме: “Строение атома”;
· организовать коллективную работу учащихся от постановки учебной задачи до конечного результата (составить опорную схему к уроку);
· обобщить материал по теме: “Металлы” и рассмотреть свойства железа и его применение;
· организовать самостоятельную исследовательскую работу в парах по изучению химических свойств железа;
· организовать взаимоконтроль учащихся на уроке.
Тип урока: изучение нового материала.
Реактивы и оборудование:
· железо (порошок, пластина, скрепка),
· сера,
· соляная кислота,
· сульфат меди (II),
· кристаллическая решетка железа,
· плакаты для игры,
· магнит,
· подборка иллюстраций по теме,
· пробирки,
· спиртовка,
· спички,
· ложка для сжигания горючих веществ,
· географические карты.
Структура урока
1. Вводная часть.
2. Изучение нового материала.
3. Сообщение домашнего задания.
4. Закрепление изученного материала.
Ход урока
1. Вводная часть
Организационный момент.
Проверка наличия учащихся.
Сообщение темы урока. Запись темы на доске и в тетрадях учащихся.
2. Изучение нового материала
– Как вы думаете, как будет звучать тема нашего сегодняшнего урока?
1. Появление железа в человеческой цивилизации положило начало железному веку.
Откуда же древние люди брали железо в то время, когда еще не умели добывать его из руды? Железо в переводе с шумерского языка – это металл, “капнувший с неба, небесный”. Первое железо, с которым столкнулось человечество, было железом из метеоритов. Впервые доказал, что “железные камни падают с неба”, в 1775 г. русский ученый П.С. Палас, который привез в Петербург глыбу самородного железного метеорита весом 600 кг. Самым крупным железным метеоритом является найденный в 1920 г. в Юго-Западной Африке метеорит “Гоба” весом около 60 т. Вспомним гробницу Тутанхамона: золото, золото. Великолепная работа восхищает, блеск слепит глаза. Но вот что пишет К.Керрам в книге “Боги, гробницы, ученые” о маленьком железном амулете Тутанхамона: “Амулет относится к числу наиболее ранних изделий Египта, и …в гробнице, наполненной чуть ли не до отказа золотом, именно эта скромная находка имела наибольшую с точки зрения истории культуры ценность”. Всего несколько железных изделий было найдено в гробнице фараона, среди них железный амулет бога Гора, небольшой кинжальчик с железным клинком и золотой рукояткой, маленькая железная скамеечка “Урс”.
Ученые предполагают, что именно страны Малой Азии, где проживали племена хеттов, были местом возникновения черной металлургии. В Европу железо пришло из Малой Азии уже в I тыс. до н.э.; так в Европе начался железный век.
Знаменитую булатную сталь (или булат) делали на Востоке еще во времена Аристотеля (IV в. до н.э.). Но технология ее изготовления держалась в секрете много веков.
Мне приснилась иная печаль
Про седую дамасскую сталь.
Я увидел, как сталь закалялась,
Как из юных рабов одного
Выбирали, кормили его,
Чтобы плоть его сил набиралась.
Выжидали положенный срок,
А потом раскаленный клинок
В мускулистую плоть погружали,
Вынимали готовый клинок.
Крепче стали, не видел Восток,
Крепче стали и горше печали.
Поскольку булат – это сталь с очень большой твердостью и упругостью, изготовленные из нее изделия обладают способностью не тупиться, будучи остро заточенными. Раскрыл секрет булата русский металлург П.П. Аносов. Он очень медленно охлаждал раскаленную сталь в специальном растворе технического масла, подогретого до определенной температуры; в процессе охлаждения сталь ковалась.
2. Положение железа в ПСХЭМ.
Выясняем положение железа в ПСХЭМ, заряд ядра и распределение электронов в атоме.
3. Физические свойства железа.
– Какие физические свойства железа вы знаете?
Железо – это серебристо-белый металл с температурой плавления 1539оС. Очень пластичный, поэтому легко обрабатывается, куется, прокатывается, штампуется. Железо обладает способностью намагничиваться и размагничиваться, поэтому применяется в качестве сердечников электромагнитов в различных электрических машинах и аппаратах. Ему можно придать большую прочность и твердость методами термического и механического воздействия, например, с помощью закалки и прокатки.
Различают химически чистое и технически чистое железо. Технически чистое железо, по сути, представляет собой низкоуглеродистую сталь, оно содержит 0,02 -0,04% углерода, а кислорода, серы, азота и фосфора – еще меньше. Химически чистое железо содержит менее 0,01% примесей. Химически чистое железо – серебристо-серый, блестящий, по внешнему виду очень похожий на платину металл. Химически чистое железо устойчиво к коррозии (вспомним, что такое коррозия? Демонстрация коррозионного гвоздя) и хорошо сопротивляется действию кислот. Однако ничтожные доли примесей лишают его этих драгоценный свойств.
4. Химические свойства железа.
Исходя из знаний о химических свойствах металлов, как вы думаете, какими химическими свойствами будет обладать железо?
| +2 | +3 |
| Взаимодействие с неметаллами | |
| Fe + S= FeS |
2Fe +3CL2 = 2FeCL3 |
| С кислотами | |
|
Fe + 2HCL= FeCL2 + H2 |
|
| С солями | |
|
Fe + CuSO4 = FeSO4 + Cu |
|
| С водой | |
|
3 Fe + 4H2O (пары) = Fe3O4 + 4H2 |
При температуре 700-900оС |
Демонстрация опытов.
· Взаимодействие железа с серой.
Практическая работа.
· Взаимодействие железа с соляной кислотой.
· Взаимодействие железа с сульфатом меди (II).
5. Применение железа.
Беседа по вопросам:
– Как выдумаете, каково распространение железа в природе?
Железо – один из самых распространенных элементов в природе. В земной коре его массовая доля составляет 5,1%, по этому показателю оно уступает только кислороду, кремнию и алюминию. Много железа находится и в небесных телах, что установлено по данным спектрального анализа. В образцах лунного грунта, которые доставила автоматическая станция “Луна”, обнаружено железо в неокисленном состоянии.
Железные руды довольно широко распространены на Земле. Названия гор на Урале говорят сами за себя: Высокая, Магнитная, Железная. Агрохимики в почвах находят соединения железа.
– В виде, каких соединений железо встречается в природе?
Железо входит в состав большинства горных пород. Для получения железа используют железные руды с содержанием железа 30-70% и более. Основными железными рудами являются: магнетит – Fe3O4 содержит 72% железа, месторождения встречаются на Южном Урале, Курской магнитной аномалии; гематит – Fe2O3 содержит до 65% железа, такие месторождения встречаются в Криворожском районе; лимонит – Fe2O3*nH2O содержит до 60% железа, месторождения встречаются в Крыму; пирит – FeS2 содержит примерно 47% железа, месторождения встречаются на Урале. (Работа с контурными картами).
– Какова роль железа в жизни человека и растений?
Биохимики открыли важную роль железа в жизни растений, животных и человека. Входя в состав чрезвычайно сложно построенного органического соединения, называемого гемоглобином, железо обусловливает красную окраску этого вещества, от которого в свою очередь, зависит цвет крови человека и животных. В организме взрослого человека содержится 3 г чистого железа, 75% которого входит в состав гемоглобина. Основная роль гемоглобина – перенос кислорода из легких к тканям, а в обратном направлении – CO2.
Железо необходимо и растениям. Оно входит в состав цитоплазмы, участвует в процессе фотосинтеза. Растения, выращенные на субстрате, не содержащем железа, имеют белые листья. Маленькая добавка железа к субстрату – и они приобретают зеленый цвет. Больше того, стоит белый лист смазать раствором соли, содержащей железо, и вскоре смазанное место зеленеет.
Так от одной и той же причины – наличия железа в соках и тканях – весело зеленеют листья растений и ярко румянятся щеки человека.
Примерно 90% используемых человечеством металлов – это сплавы на основе железа. Железа выплавляется в мире очень много, примерно в 50 раз больше, чем алюминия, не говоря уже о прочих металлах. Сплавы на основе железа универсальны, технологичны, доступны, дешевы. Железу еще долго быть фундаментом цивилизации.
3. Сообщение домашнего материала
4. Закрепление изученного материала
1. Используя опорную схему, записанную на доске, сделайте вывод: что же представляет собой железо и каковы его свойства?
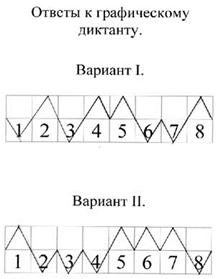
2. Графический диктант (заранее приготовить листочки с начерченной прямой, разделенной на 8 отрезков и пронумерованной соответственно вопросам диктанта. Отметить шалашиком ^” на отрезке номер положения, которое считается верным).
Вариант 1.
1. Железо это активный щелочной металл.
2. Железо легко куется.
3. Железо входит в состав сплава бронзы.
4. На внешнем энергетическом уровне атома железа 2 электрона.
5. Железо взаимодействует с разбавленными кислотами.
6. С галогенами образует галогениды со степенью окисления +2.
7. Железо не взаимодействует с кислородом.
8. Железо можно получить путем электролиза расплава его соли.
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
Вариант 2.
1. Железо это металл серебристо-белого цвета.
2. Железо не обладает способностью намагничиваться.
3. Атомы железа проявляют окислительные свойства.
4. На внешнем энергетическом уровне атома железа 1 электрон.
5. Железо вытесняет медь из растворов ее солей.
6. С галогенами образует соединения со степенью окисления +3.
7. С раствором серной кислоты образует сульфат железа (III).
8. Железо не подвергается коррозии.
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
После выполнения задания учащиеся меняются своими работами и проверяют их (ответы к работам вывешены на доске, или показать через проектор).
Критерии отметки:
· 5 0 ошибок,
· 4 1-2 ошибки,
· 3 3-4 ошибки,
· 2 5 и больше ошибок.
Приложения
Интересный материал к уроку
Знаете ли вы, что?
Железо – один из важнейших элементов жизни. Кровь содержит железо, и именно оно определяет цвет крови, а также ее основное свойство – способность связывать и отдавать кислород. Такой способностью обладает комплексное соединение – гем – составная часть молекулы гемоглобина. Кроме гемоглобина железо в нашем организме есть еще в миоглобине – белке, запасающем кислород в мышцах. Есть также железосодержащие ферменты.
Близ г. Дели в Индии стоит железная колонна без малейшего пятнышка ржавчины, хотя ее возраст почти 2800 лет. Это знаменитая Кутубская колонна высотой около семи метров и массой 6.5 т. Надпись на колонне говорит о том, что она была поставлена в IX в. До н. э. Ржавление железа – образование метагидроксида железа – связано с взаимодействием его с влагой и кислородом воздуха.
Однако эта реакция при отсутствии в железе различных примесей, и прежде всего углерода, кремния и серы, не протекает. Колонна была изготовлена из очень чистого металла: железа в колонне оказалось 99,72%. Этим и объясняется ее долговечность и коррозионная устойчивость.
В 1934 г. в "Горном журнале" появилась статья "Улучшение железа и стали посредством...ржавления в земле". Способ превращения железа в сталь через ржавление в земле известен людям с глубокой древности. Например, черкесы на Кавказе закапывали полосовое железо в землю, а откопав его через 10-15 лет, выковывали из него свои сабли, которые могли перерубить даже ружейный ствол, щит, кости врага.
Гематит
Гематит, или красный железняк – основная руда главного металла современности – железа. Содержание железа достигает в нем 70%. Гематит известен с давних пор. В Вавилоне и Древнем Египте он использовался в украшениях, для изготовления печатей, наряду с халцедоном служил излюбленным материалом в качестве резного камня. У Александра Македонского был перстень с вставкой из гематита, который, как он полагал, делал его неуязвимым в бою. В древности и в Средние века гематит слыл лекарством, останавливающим кровь. Порошок из этого минерала издревле использовали для золотых и серебряных изделий.
Название минерала происходит от греческого дета – кровь, что связано с вишневым или сургучно-красным цветом порошка этого минерала.
Важной особенностью минерала является способность стойко хранить цвет и передавать его другим минералам, в которые попадает хотя бы небольшая примесь гематита. Розовый цвет гранитных колонн Исаакиевского собора – это цвет полевых шпатов, которые в свою очередь окрашены тонкораспыленным гематитом. Живописные узоры яшмы, используемой при отделке станций столичного метро, оранжевые и розовые сердолики Крыма, кораллово-красные прослойки сильвина и карналлита в соляных толщах – все обязаны своим цветом гематиту.
Издавна из гематита делали красную краску. Все известные фрески, выполненные 15-20 тыс. лет назад, замечательные бизоны Альтамирской пещеры и мамонты из знаменитой Капской пещеры – выполнены и коричневыми оксидами и гидроксидами железа.
Магнетит
Камень, чье имя магнит, залегает в земле троглодитов;
Впрочем, не меньше того им богаты индийские страны.
Он узнается легко по бурому ржавому цвету
И потому как он тянет к себе железные вещи.
М. Реннский
Магнетит, или магнитный железняк – минерал, содержащий 72% железа. Это самая богатая железная руда. Замечательное в этом минерале его природный магнетизм – свойство, благодаря которому он был открыт.
Как сообщал римский ученый Плиний, магнетит назван в честь греческого пастуха Магнеса. Магнес пас стадо возле холма над р. Хинду в Фессалии. Неожиданно посох с железным наконечником и подбитые гвоздями сандалии притянула к себе гора, сложенная сплошным серым камнем. Минерал магнетит дал в свою очередь название магниту, магнитному полю и всему загадочному явлению магнетизма, которое пристально изучается со времен Аристотеля и по сей день.
Магнитные свойства этого минерала и сегодня используются, прежде всего для поиска месторождений. Именно так были открыты уникальные месторождения железа на площади Курской магнитной аномалии (КМА). Минерал тяжелый: образец магнетита размером с яблоко весит 1,5 кг.
В древности магнетит наделяли всевозможными лечебными свойствами и способностью творить чудеса. Его использовали для извлечения металла при ранениях, а Иван Грозный среди своих сокровищ наравне с другими камнями хранил его непримечательные кристаллы.
Пирит – минерал, подобный огню
Не все золото, что блестит. Пословица
Пирит – один из тех минералов, увидев который хочется воскликнуть: "Неужели это так и было?" Трудно поверить, что высший класс огранки и полировки, поражающий нас в рукотворных изделиях, в кристаллах пирита – щедрый дар природы.
Пирит получил свое название от греческого слова "пирос" – огонь, что связано с его свойством искрить при ударе стальными предметами. Этот красивый минерал поражает золотистым цветом, ярким блеском на почти всегда четких гранях. Благодаря своим свойствам пирит известен с глубокой древности, а во время эпидемий золотой лихорадки пиритовые блестки в кварцевой жиле вскружили не одну горячую голову. Да и сейчас начинающие любители камня нередко принимают пирит за золото.
Железо и его соединения
Лабораторная работа № 4
Тема. Железо и его соединения.
Цель:
· познакомить с некоторыми химическими свойствами соединений железа в различных степенях окисления.
Реактивы: железные опилки Fe, соль Мора (NH4)2SO4·FeSO4·6H2O, раствор хлорида железа (III) FeCl3, раствор гексационоферрата (III) калия K3[Fe(CN)6], раствор гексационоферрата (II) калия K4[Fe(CN)6], раствор роданида калия KCNS, раствор соляной кислоты HCl (концентрированный и разбавленный), раствор серной кислоты H2SO4 (концентрированный и разбавленный), раствор азотной кислоты HNO3 (концентрированный и разбавленный), раствор гидроксида натрия NaOH (концентрированный и разбавленный).
Посуда и оборудование: спиртовка, держатель для пробирок, штатив для пробирок, шпатель, пробирки, стеклянная палочка.
Ход работы
Опыт 1. Свойства металлического железа
Испытайте действие на железо концентрированных и разбавленных кислот при обычных условиях и при нагревании.
Для этого поместите железные опилки в пробирку и прилейте несколько капель разбавленной соляной кислоты, запишите наблюдаемые явления и дайте им объяснения. Опыт повторите с разбавленными растворами серной и азотной кислот. Осторожно нагрейте те пробирки, в которых не происходит взаимодействие железа с кислотой. Отметьте наблюдения.
Повторите опыт с концентрированными растворами кислот. Запишите наблюдаемые явления, обратите внимание на цвет и запах выделяющихся газов и на цвет растворов.
| № эксп. | Порядок выполнения | Наблюдения | Уравнение реакции | Выводы |
| 1 |
1. В пробирку поместили железные опилки и прилили несколько капель разбавленной соляной кислоты. 2. … |
Наблюдается выделение бесцветного газа, раствор окрашивает-ся в бледно-зеленый цвет |
Fe + 2HCl = FeCl2 + H2 Fe0
2e 2H+
+ 2e окислитель |
Железо взаимодействует с соляной кислотой, проявляя восстановитель-ные свойства, в результате реакции образуется соль – хлорид железа (II)и выделяется бесцветный газ - водород |
Опыт 2. Гидроксид железа (II), получение и свойства
Вскипятите немного воды, охладите ее и добавьте несколько кристаллов соли Мора (NH4)2SO4·FeSO4·6H2O. В пробирку со свежеприготовленным раствором соли Мора прилейте раствор гидроксида натрия до выпадения осадка. Отметьте цвет осадка. Оставьте осадок на воздухе и наблюдайте за быстрым изменением окраски.
Запишите уравнение реакции получения гидроксида железа (II) (в уравнении учитывайте только FeSO4) в молекулярной и ионной форме и уравнение окисления гидроксида железа (II) кислородом воздуха. Сделайте вывод об устойчивости ионов двухвалентного железа.
Опыт 3. Гидроксид железа (III), получение и свойства
В пробирку поместите несколько капель раствора хлорида железа (III) и прибавьте по каплям раствор гидроксида натрия до выпадения осадка. Отметьте цвет осадка. Полученный осадок разделите на две части. К первой прилейте по каплям раствор соляной кислоты, ко второй – концентрированный раствор гидроксида натрия. Запишите наблюдаемые явления.
Запишите уравнения получения гидроксида железа (III). Приведите уравнения растворения гидроксида железа (III) в кислоте и в щелочи, сделайте вывод о кислотно-основных свойствах гидроксида железа (III).
Опыт 4. Качественные реакции на ионы Fe (II) и Fe (III)
Взаимодействие соли железа (II) с гексационоферратом (III) калия (качественная реакция на ионы Fe2+)
В пробирку с раствором соли Мора (NH4)2SO4·FeSO4·6H2O прилейте несколько капель раствора гексационоферрата (III) калия (красной кровяной соли). Отметьте цвет осадка. Запишите уравнение реакции, дайте название образовавшемуся соединению KFe+2[Fe+3(CN)6] (используйте справочную литературу).
Взаимодействие соли железа (III) с гексационоферратом (II) калия (качественная реакция на ионы Fe3+)
В пробирку с раствором хлорида железа (III) прилейте несколько капель раствора гексационоферрата (II) калия (желтой кровяной соли). Отметьте цвет осадка. Запишите уравнение реакции, дайте название образовавшемуся соединению KFe+3[Fe+2(CN)6] (используйте справочную литературу).
Взаимодействие соли железа (III) с роданидом калия (качественная реакция на ионы Fe3+)
В пробирку с раствором хлорида железа (III) прилейте несколько капель раствора роданида калия. Отметьте цвет раствора. Запишите уравнение реакции.
Сделайте общий вывод по работе.
Урок 2 "Пришелец из космоса". "Железо и его соединения"
Цели урока:
· в процессе исследования изучить физические и химические свойства железа и его соединений;
· развивать дальнейшие умения составлять молекулярные и ионные уравнения химических реакций;
· учить сравнивать, обобщать, анализировать и делать выводы;
· развивать познавательную деятельность через эксперимент и посредством заданий развивающего характера;
· развивать коммуникативные качества личности.
Метод обучения: проблемно-поисковый
Организационные формы: беседа, самостоятельная и практическая работа, сообщения учащихся
Средства обучения: таблицы, химическое оборудование и реактивы, медиапроектор.
Программное обеспечение: компьютерная презентация к уроку (Приложение №1)
Эпиграф к уроку:
Другого ничего в природе нет
Ни здесь, ни там, в космических глубинах:
Все от песчинок малых до планет –
Из элементов состоит единых.
С. Щипачев
I. Введение в тему. Вступительное слово учителя.
Ребята! Сегодня мы с вами отправимся в далёкое путешествие, чтобы познакомиться с Пришельцем из космоса. А какой металл считается Пришельцем? Почему его так назвали? Во время путешествия нам предстоит сделать несколько остановок по требованию.
II. Первая остановка Космическая” (появление железа на Земле). Сообщение ученика.
Знакомство человека с железом произошло в давние времена. Есть основания полагать, что образцы железа, которые держали в руках первобытные люди, были неземного происхождения. Входя в состав некоторых метеоритов - вечных странников океана Вселенной, случайно нашедших приют на нашей планете, - метеоритное железо было тем материалом, из которого человек изготовил впервые железные изделия. Железо в самородном состоянии встречается на земле главным образом в виде метеоритного, космического” железа.
- 18 октября 1916 года вблизи с. Богуславки Дальневосточного края наблюдали падение метеорита, два его осколка весили по 256 кг.
- 1920 год - Юго-Западная Африка, метеорит “Гоба” весом около 60 тонн.
- 30 июня 1908 г. упал знаменитый Тунгусский метеорит весом 50 тыс. тонн.
III. Вторая остановка. Составление визитки для железа как химического элемента” (работа в парах).
Учитель: Работая с Периодической таблицей химических элементов, составьте визитную карточку для железа по алгоритму:
Порядковый номер:
Период:
Группа:
Подгруппа:
Электронная формула:
(После работы в парах на экране появляется слайд № 1 “Визитная карточка”), учитель выслушивает ответы учащихся.
? Исходя из строения атома железа, определить его валентные электроны.
Учитель. Железо имеет 8 валентных электронов (два из них на 4s- и шесть на 3d-АО). Однако валентность 8 для железа не характерна; неустойчивы и соединения с шестивалентным железом, например производные железной кислоты H2FeO4, являющиеся сильнейшими окислителями. Обычно железо проявляет валентности равные двум и трем и соответствующие степени окисления.
? Какими свойствами обладает железо как простое вещество?
(Учитель предлагает совершить следующую остановку).
IV. Третья остановка Физические свойства”( работа в парах). Учащиеся работают с учебником, справочной литературой и записывают в тетрадь характерные физические свойства:
Цвет:
Металлический блеск:
Твердость:
Пластичность:
Теплопроводность:
Электропроводность:
Плотность:
Температура плавления:
Железо - серебристо-белый или серый металл, твердый, с высокой пластичностью, теплопроводностью и электропроводностью, плотность его равна 7,87 г/см3, тугоплавкий-1540?С. Это самый распространенный химических элементов в природе. В земной коре его массовая доля составляет 5,1%.
Учитель проверяет выполненную работу в виде беседы с классом.
? Какими ещё свойствами обладает железо?
Учитель. Да, в отличие от других металлов, железо способно намагничиваться, оно обладает ферромагнетизмом.
Демонстрация опыта: намагничивание железных опилок.
? Какова активность железа?
Учитель обращает внимание учащихся на электрохимический ряд напряжения металлов. Для того, чтобы узнать активность железа по отношению к другим веществам, мы совершаем с вами очередную остановку.
V. Четвёртая остановка. Экспериментальная. “Химические свойства железа”.
Учитель. Железо взаимодействует как с простыми, так и сложными веществами. Предлагаю вам провести эксперименты с серой, соляной кислотой, сульфатом меди, объяснить свои наблюдения и составить уравнения химических реакций.
? Чем является железо в данных уравнениях реакций? (На экране появляется второй слайд).
1. Fe + S = FeS
2. Fe + 2HCI = FeCI2 + H2
3. Fe + CuSO4 = FeSO4 + Cu
Fe0 - 2e = Fe+2 (восстановитель)
? Что вы наблюдали при проведении третьей реакции? (Железо вытеснило медь из раствора сульфата меди).
? Действует ли вода и кислород на железо?
Учитель. При обычных условиях вода не действует на железо, однако, в присутствии кислорода протекает следующая реакция: (на экране появляется слайд №3)

Fe(OH)3 - гидроксид железа (III) - основная часть ржавчины. Для протекания данной реакции необходимо одновременно присутствие воды и кислорода, в противном случае коррозия так и не наступит. Известно, что в течение многих столетий стоит знаменитая железная колонна в столице Индии Дели. Почему? (Там сухой воздух).
Учитель. Предлагаю учащимся провести опыт: реакцию обмена между сульфатом железа (II) и гидроксидом меди, записать уравнение химической реакции в молекулярном и ионном виде (на экране появляется слайд № 4).
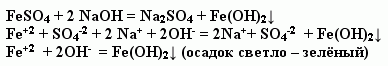
Учитель предлагает учащимся вновь вернуться к полученному осадку и посмотреть на изменение цвета.
? Как изменился цвет осадка? Что произошло?
Учитель. Соединение железа двухвалентного неустойчиво и окисляется, превращаясь в соединение железа трехвалентного бурого цвета (слайд № 5).
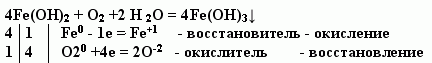
? Может вытеснять железо водород из воды?
Да, может, но только при сильном нагревании (запись на доске).
Fe + H2O = FeO +H2
Fe0 - 2e = Fe+2 - восстановитель - окисление
2H+ + 2е = Н2 - окислитель - восстановление
? Какие два оксида образует химический элемент железо? (FeO и Fe2O3)
? Какими свойствами они обладают? (Основными).
При окислении железа в высокотемпературном режиме образуется железная окалина:
3 Fe +2O2 = Fе 3O 4
Учитель. Что вы узнали во время данной остановки? Какими свойствами обладает железо как простое вещество? Сделайте вывод.
VI. Остановка № 5. Подумай!” (слайд № 6).
(Письменная работа, в результате которой учащиеся должны написать возможно протекающие реакции).
VII. Остановка № 6. Значение железа” (сообщение ученика)
Биохимики раскрывают огромную роль железа в жизни растений, животных и человека. Входя в состав гемоглобина, железо обуславливает красный цвет этого вещества, от которого, в свою очередь, зависит цвет крови. В организме взрослого человека содержится 3 г железа, из них 75% входят в состав гемоглобина, благодаря которому осуществляется важнейший биологический процесс - дыхание. Железо необходимо и для растений. Оно участвует в окислительных процессах протоплазмы, при дыхании растений и в построении хлорофилла, хотя само и не входит в его состав.
Железо издавна применяется в медицине для лечения малокровия, при истощении, упадке сил.
Железо - основа всей металлургии, машиностроения, железнодорожного транспорта, судостроения, грандиозных инженерных сооружений - от башни Эйфеля до ажура железнодорожных мостов. Все, все - начиная от швейной иглы, гвоздя, топора и кончая паутиной железных дорог, плавающими крепостями - авианосцами и линкорами - и огнедышащими домнами, где рождается само железо, - состоит из железа. Железо - это металл созидания!
YIII. Подведение итогов урока. Рефлексия.
Учитель. В завершении путешествия поделитесь своими впечатлениями. Для этого допишите предложения, посвященные сегодняшнему уроку:
Сегодня я узнал (а)______________________________________
Я удивился (лась)_______________________________________
Теперь я умею _________________________________________
Я хотел (а) бы __________________________________________
Домашнее задание
3.2 Задачи
Важную роль в процессе подготовки к экзамену по химии играют задачи. Их решение способствует неформальному усвоению теоретического курса. Они включаются в экзаменационные билеты. При этом мы будем рассматривать некоторые наиболее типовые задачи с решениями [5, 11, 12].
1.Почему применение чистого железа ограничено?
Ответ Чистое железо достаточно легко корродирует, поэтому его надо каким-то образом защищать от коррозии- либо покрывать защитным покрытием, либо применять в виде сплавов.
2. Составьте уравнения реакций железа с простыми и сложными веществами. Покажите переход электронов и поясните, что окисляется и что восстанавливается
3. Требуется скрепить железные детали. Какими заклепками следует пользоваться — медными или цинковыми, чтобы замедлить коррозию деталей? Ответ обоснуйте.
Ответ: Если скрепить железные детали медными заклепками, то процесс электрохимической коррозии железа усилится, поскольку медь — менее активный металл, чем железо. Поэтому надо пользоваться цинковыми заклепками, которые замедляют коррозию железа. При этом сами заклепки буду корродировать быстрее, чем в отсутствие железа.
4.
Вычислите
массовые доли железа в соединениях: ![]() ,
, ![]()
![]() ,
, ![]() . В каком из этих соединений
массовая доля железа наибольшая?
. В каком из этих соединений
массовая доля железа наибольшая?
5. Минерал содержит 72, 36% железа и 27, 64% кислорода. Определите формулу минерала.
6. Сколько граммов сульфата железа (II) можно получить при растворении 140г железа в разбавленной серной кислоте?
7. Сколько граммов гидроксида железа (III) можно получить при взаимодействии 120г гидроксида натрия с избытком хлорида железа (III)?
3.3 Тесты
1.Хлорид железа (II) получают реакцией:
а) ![]()
б) ![]() +
+
в)![]()
г) ![]()
2.Какова электронная конфигурация атома железа
а) ![]()
б)![]()
в)![]() +
+
г)![]()
3. С какими из указанных веществ реагирует железо
а) ![]() +
+
б)![]()
в)![]() +
+
г)![]()
4. Взаимодействие соляной кислоты с оксидом железа (II) относится к реакции:
а) разложения
б) соединения
в) замещения
г) обмена +
5. О простом веществе железо идет речь в выражении
а) железо входит в состав стали
б) железо входит в состав ржавчины
в) железо входит в состав железного купороса
г) железо притягивается магнитом +
6. Химическое равновесие
в системе ![]()
сместится в сторону продукта реакции при
а) повышении давления
б) повышении температуры
в) понижении давления
г) использовании катализатора
7.Сумма коэффициентов
перед формулами неэлектролитов в уравнении реакции ![]() равно
равно
а)2 +
б) 3
в) 4
г)5
8. Концентрированную азотную кислоту можно транспортировать в стальных цистернах так как :
а) железо не растворяется в кислотах
б) азотная кислота не действует на металлы
в) концетрированная азотная кислота не реагирует с железом +
г) азотная кислота является сильным электролитом
9. Коэффициент перед формулой восстановителя в уравнении реакции алюминия с оксидом железа (II) равен
а) 1
б)2 +
в)3
г)4
10. Химическое равновесие
в системе ![]()
не смещается при
а) повышении давления +
б) повышении температуры
в) понижении температуры
г) добавлении водорода
11. Осадок образуется при взаимодействии растворов хлорида железа (III) и
а) гидроксида натрия +
б) сульфата натрия
в) соляной кислоты
г) нитрата меди (II)
12. Формула вещества, обозначенного «Х» в схеме превращений
![]()
а) ![]()
б) ![]()
в)![]() +
+
г)![]()
13. Суммы всех коэффициентов в полном и сокращенном ионных уравнениях реакции между растворами сульфата железа (II) с гидроксидом бария равны
а) 9 и 5
б) 9 и 7
в) 7 и 5
г) 7 и 7 +
14. При нагревании 28г
железа с 32г серы образуется сульфид железа ![]() (Mr=88) массой:
(Mr=88) массой:
а) 32г
б)38г
в)44г +
г)60г
15. Растворение желез в соляной кислоте будет замедляться при:
а) увеличении концентрации кислоты
б) раздроблении железа
в) разбавлении кислоты +
г)повышении температуры
16. Химическое равновесие
в системе ![]() сместится
в сторону исходных веществ при
сместится
в сторону исходных веществ при
а) повышении давления
б) повышении температуры
в) понижении давления
г) понижении температуры +
17. При взаимодействии с хлором железо проявляет свойства
а) окислительные
б) кислотные
в) восстановительные +
г) основные
18. Сокращенное ионное
уравнение ![]() соответствует
взаимодействию:
соответствует
взаимодействию:
а) раствора соли железа (II) с раствором щелочи +
б) раствора соли железа (II) со щелочью
в) раствора соли железа (II) с нерастворимым основанием
г) нерастворимой соли железа (II) с нерастворимым основанием
19. В уравнении реакции железа с хлором с образованием хлорида железа (III) коэффициент перед формулой соли равен:
а) 1
б) 2 +
в) 3
г) 4
20. Соляная кислота может взаимодействовать со всеми веществами группы
а) железо, оксид железа (III), гидроксид меди (II) +
б) цинк, оксид кремния (IV), гидроксид меди (II)
в) медь, оксид меди (II), гидроксид меди (II)
г) сера, оксид серы (IV), оксид серы (VI)
21. При пропускании водорода над раскаленным оксидом железа (III) водород играет роль:
а) восстановителя +
б) катализатора
в) окислителя
г) и восстановителя, и окислителя
22. В уравнении реакции,
схема которой ![]() коэффициент перед формулой
восстановителя равен:
коэффициент перед формулой
восстановителя равен:
а)1
б) 2
в) 3
г) 4 +
23. В химических реакциях Fe2+выполняет роль:
а) окислителя;
б) восстановителя; +
в) окислителя или восстановителя в зависимости от условий.
24. FeCl3+NaOH![]()
а) Fe3+ +3OH-
![]() Fe(OH)3
+
Fe(OH)3
+
б) Fe2+ +2OH-
![]() Fe(OH)2
Fe(OH)2
в) Fe3+ + OH-
![]() Fe(OH)3
Fe(OH)3
25.Fe(NO3)2+K3PO4![]()
а) 2Fe3+ + 3PO42-
![]() Fe2(PO4)3
Fe2(PO4)3
б) 3Fe2+ +2
PO43- ![]() Fe3(PO4)2
+
Fe3(PO4)2
+
в) Fe2+ + PO42-
![]() Fe PO4
Fe PO4
26. Fe2O3+HCl![]()
а) Fe2O3+6H+
![]() 2Fe3+ +3H2O
+
2Fe3+ +3H2O
+
б) 2Fe3+ + O32+
+6 H+ ![]() Fe3+ + 3Н2О
Fe3+ + 3Н2О
в) Fe2O3+6H+![]() 2Fe2+ +
3Н2О
2Fe2+ +
3Н2О
27. LiOH+FeCl2![]()
а) Fe2+ +2OH-
![]() Fe(OH)2
Fe(OH)2
б) Fe3+ + 3OH-
![]() Fe(OH)3
Fe(OH)3
в) Fe2+ +OH-
![]() Fe(OH)2 +
Fe(OH)2 +
28.
| № | Дана схема реакции | № ответа | Полуреакция в электронном балансе |
|
1. 2. 3. 4. 5. |
Fe+Cl2 Li+H2 Fe+HCl Li+H2O FeO+HCl |
А) Б) Г) Д) E) |
H20 +2e- Cl20+2e- 2H++2e- 2Cl- - 2e- Fe0 -2e- Fe0 -3e- |
29. Железо не взаимодействует с…
а) соляной кислотой;
б) кислородом воздуха;
в) оксидом калия. +
30. Найдите сокращенное
ионное уравнение, соответствующее левой части молекулярного уравнения: Fe(OH)2+2HNO3![]()
а) Fe (OH)2+2H+![]() Fe 2++2H2O
Fe 2++2H2O
б) OH-+H+![]() H2O
H2O
в) Fe 2++2NO3- ![]() Fe (NO3)2 +
Fe (NO3)2 +
31. Реакцией замещения является
а)Fe + CuCl2 → FeCl2 + Cu
б)FeCl3 + Cu → CuCl2 + FeCl2
в)FeCl2 + Cl2 → FeCl3
г)FeCl2 + NH3 + H2O → Fe(OH)2 + NH4Cl +
д)Fe(OH)2 → FeO + H2O
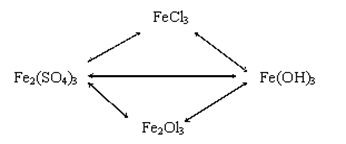
32. Составьте уравнение по схеме:
33. Массовая доля железа в пирите равна:
а) 0,549
б) 0,382
в) 0,728 +
г) 0,467
34.Число неспаренных электронов в основном состоянии атома железа равно:
а) 2
б) 4 +
в) 3
г) 1
35. С водными растворами каких веществ будет реагировать железо?
а) хлорид калия
б) нитрат кальция
в) хлороводород +
г) нитрат серебра (I) +
36. Гидроксид железа (II) можно получить взаимодействием:
а) оксида железа (II) и воды
б) хлорида железа (II) и щелочи +
в) сульфата железа (II) и гидроксида натрия +
г) гидроксида железа (III)
37. Процесс ржавления
железа может быть описан уравнением: ![]() Какие утверждения справедливы
относительно этого процесса?
Какие утверждения справедливы
относительно этого процесса?
а) кислород восстанавливается +
б) железо окисляется +
в) степень окисления железа повышается +
г) степень окисления кислорода понижается +
38. Для превращения магнетита в оксид железа (III) необходимо, чтобы магнетит прореагировал с:
а) водородом
б) кислородом +
в) оксидом углерода (II)
г) коксом
39. В каком из природных соединений железа его массовая доля наибольшая?
а) магнетит +
б) гематит +
в) пирит +
г) сидерит
40. Для железа в соединениях наиболее характерны степени окисления, равные:
а) +8
б) +3 +
в) +1
г) +2 +
41. В отличие от гидроксида железа (III) гидроксид железа (II) реагирует с:
а) соляной кислотой
б) концентрированным раствором щелочи
в) кислородом во влажном воздухе +
г) разбавленной серной кислотой
42. С водными растворами каких солей реагирует железо?
а) ![]()
б) ![]() +
+
в) ![]() +
+
г) ![]()
43. Отметьте формулы веществ, с которыми реагирует водный раствор сульфата железа (III):
а) соляная кислота
б) медь
в) гидроксид калия +
г) цинк +
44. Различить между собой
пробирки, содержащие водные растворы ![]() и
и ![]() можно с помощью:
можно с помощью:
а) лакмуса
б) нитрата серебра (I)
в) серной кислоты
г) гидроксида натрия +
45. Растворы каких веществ имеют кислую реакцию среды (pH меньше 7):
а) ![]() +
+
б) ![]()
в) ![]()
г) ![]() +
+
46. Какие из указанных металлов являются более активными, чем железо?
а) медь
б) кальций +
в) ртуть
г) калий +
47. В чем растворяется ![]() ?
?
а) вода
б) раствор гидроксида натрия
в) раствор соляной кислоты +
г) раствор хлорида натрия
48. Какие из указанных металлов являются менее активными, чем железо
а) натрий
б) олово +
в) никель +
г) барий
49. В чем растворяется ![]() ?
?
а) вода
б) раствор соляной кислоты +
в) раствор нитрата калия
г) раствор гидроксида калия разбавленный
50. С какими из указанных
веществ реагирует ![]() ?
?
а) вода
б) соляная кислота +
в) оксид натрия
г) оксид серы (IV) +
ЛИТЕРАТУРА
1. Фельдман Ф.Г., Рудзитис Г.Е. Химия. Учебник для 9 класса общеобразовательных учебных учреждений. М.: Просвещение, 1999;
2. Хомченко Г.П. Химия для поступающих в вузы. М.: Высшая школа, 1993.
3. Ахметов Н.С. Химия. Учебник для 9 класса общеобразовательных учебных учреждений М.: Просвещение, 2001;
4.Малышкина В. Занимательная химия. – Санкт-Петербург, “Тригон”, 2001;
5.Книга для чтения по неорганической химии. Сост. В.А.Крицман, М.: Просвещение, 1984;
6.Программно-методические материалы. Химия 8-11 классы. – М.: Дрофа, 2001.
7.Степин Б.Д., Аликберова Л.Ю. Книга по химии для домашнего чтения. – М.: Химия, 1995;
8. Я иду на урок Химии. Книга для учителя. – М.: “Первое сентября, 2000.
9. Исидоров В.А. Экологическая химия: Учебное пособие для вузов.
– СПб: Химиздат, 2001;
10. Кузьменко Н.Е., Еремин В.В. Химия. 2400 задач для школьников
и поступающих в вузы.- М.: Дрофа, 1999;
11. Химия: Большой справочник для школьников и поступающих в вузы/
Е. А. Алферова, Н.С. Ахметов – М.: Дрофа, 1999;
© 2009 База Рефератов