Рефераты по рекламе
Рефераты по физике
Рефераты по философии
Рефераты по финансам
Рефераты по химии
Рефераты по хозяйственному праву
Рефераты по цифровым устройствам
Рефераты по экологическому праву
Рефераты по экономико-математическому моделированию
Рефераты по экономической географии
Рефераты по экономической теории
Рефераты по этике
Рефераты по юриспруденции
Рефераты по языковедению
Рефераты по юридическим наукам
Рефераты по истории
Рефераты по компьютерным наукам
Рефераты по медицинским наукам
Рефераты по финансовым наукам
Рефераты по управленческим наукам
психология педагогика
Промышленность производство
Биология и химия
Языкознание филология
Издательское дело и полиграфия
Рефераты по краеведению и этнографии
Рефераты по религии и мифологии
Рефераты по медицине
Курсовая работа: Методы защиты от коррозии металлов и сплавов
Курсовая работа: Методы защиты от коррозии металлов и сплавов
МЕТОДЫ ЗАЩИТЫ ОТ КОРРОЗИИ МЕТАЛЛОВ И СПЛАВОВ
Основным условием противокоррозийной защиты металлов и сплавов является уменьшение скорости коррозии. Уменьшить скорость коррозии можно, используя различные методы защиты металлических конструкций от коррозии. Основными из них являются:
1 Защитные покрытия.
2 Обработка коррозионной среды с целью снижения коррозионной активности (в особенности при постоянных объемах коррозионных сред).
3 Электрохимическая защита.
4 Разработка и производство новых конструкционных материалов повышенной коррозионной устойчивости.
5 Переход в ряде конструкций от металлических к химически стойким материалам (пластические высокомолекулярные материалы, стекло, керамика и др.).
6 Рациональное конструирование и эксплуатация металлических сооружений и деталей.
1. Защитные покрытия
Защитное покрытие должно быть сплошным, равномерно распределенным по всей поверхности, непроницаемым для окружающей среды, иметь высокую адгезию (прочность сцепления) к металлу, быть твердым и износостойким. Коэффициент теплового расширения должен быть близким к коэффициенту теплового расширения металла защищаемого изделия.
Классификация защитных покрытий представлена на рис. 43

Защитные покрытия

![]() Неметаллические
Металлические
Неметаллические
Металлические
![]()
![]()
![]() покрытия
покрытия
покрытия
покрытия
Неорганические Органические Катодные Анодные
![]()
|
Неорганические эмали, оксиды металлов, соединения хрома, фосфора и др.
|
Лакокрасочные покрытия, покрытия смолами, покрытия пластмассами, покрытия полимерными пленками, резиной |
|
Рисунок 43 - Схема классификации защитных покрытий
1.1 Металлические покрытия
Нанесение защитных металлических покрытий – один из самых распространенных методов борьбы с коррозией. Эти покрытия не только защищают от коррозии, но и придают их поверхности ряд ценных физико-механических свойств: твердость, износоустойчивость, электропроводность, паяемость, отражательную способность, обеспечивают изделиям декоративную отделку и т.д.
По способу защитного действия металлические покрытия делят на катодные и анодные.
Катодные покрытия имеют более положительный, а анодные - более электроотрицательный электродные потенциалы по сравнению с потенциалом металла, на который они нанесены. Так, например, медь, никель, серебро, золото, осажденные на сталь, являются катодными покрытиями, а цинк и кадмий по отношению к этой же стали – анодными покрытиями.
Необходимо отметить, что вид покрытия зависит не только от природы металлов, но и от состава коррозионной среды. Олово по отношению к железу в растворах неорганических кислот и солей играет роль катодного покрытия, а в ряде органических кислот (пищевых консервах) служит анодом. В обычных условиях катодные покрытия защищают металл изделия механически, изолируя его от окружающей среды. Основное требование к катодным покрытиям – беспористость. В противном случае при погружении изделия в электролит или при конденсации на его поверхности тонкой пленки влаги обнаженные (в порах или трещинах) участки основного металла становятся анодами, а поверхность покрытия катодом. В местах несплошностей начнется коррозия основного металла, которая может распространяться под покрытие (рис. 44 а).
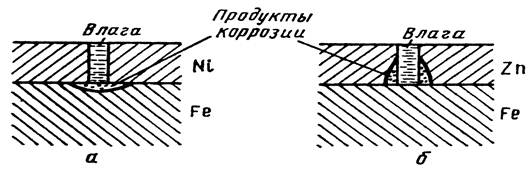
Рисунок 11 Схема коррозии железа с пористым катодным (а) и анодным (б) покрытием
Анодные покрытия защищают металл изделия не только механически, но главным образом электрохимически. В образовавшемся гальваническом элементе металл покрытия становится анодом и подвергается коррозии, а обнаженные (в порах) участки основного металла выполняют роль катодов и не разрушаются, пока сохраняется электрический контакт покрытия с защищаемым металлом и через систему проходит достаточный ток (рис.4 б). Поэтому степень пористости анодных покрытий в отличие от катодных не играет существенной роли.
В отдельных случаях электрохимическая защита может иметь место при нанесении катодных покрытий. Это происходит, если металл покрытия по отношению к изделию является эффективным катодом, а основной металл склонен к пассивации. Возникающая анодная поляризация пассивирует незащищенные (в порах) участки основного металла и затрудняет их разрушение. Такой вид анодной электрохимической защиты проявляется для медных покрытий на сталях 12Х13 и 12Х18Н9Т в растворах серной кислоты.
Основной метод нанесения защитных металлических покрытий – гальванический. Применяют также термодиффузионный и механотермический методы, металлизацию распылением и погружением в расплав.Разберем каждый из методов более подробно.
1.2 Гальванические покрытия.
Гальванический метод осаждения защитных металлических покрытий получил очень широкое распространение в промышленности. По сравнению с другими способами нанесения металлопокрытий он имеет ряд серьезных преимуществ: высокую экономичность (защита металла от коррозии достигается весьма тонкими покрытиями), возможность получения покрытий одного и того же металла с различными механическими свойствами, легкую управляемость процесса (регулирование толщины и свойств металлических осадков путем изменения состава электролита и режима электролиза), возможность получения сплавов разнообразного состава без применения высоких температур, хорошее сцепление с основным металлом и др.
Недостаток гальванического метода – неравномерность толщины покрытия на изделиях сложного профиля.
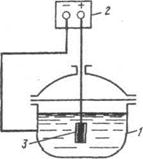
Электрохимическое осаждение металлов проводят в гальванической ванне постоянного тока (рис 45). Покрываемое металлом изделие завешивают на катод. В качестве анодов используют пластины из осаждаемого металла (растворимые аноды) или из материала, нерастворимого в электролите (нерастворимые аноды).
Обязательный компонент электролита – ион металла, осаждающийся на катоде. В состав электролита могут также входить вещества, повышающие его электропроводность, регулирующие протекание анодного процесса, обеспечивающие постоянство рН, поверхностно-активные вещества, повышающие поляризацию катодного процесса, блескообразующие и выравнивающие добавки и др.
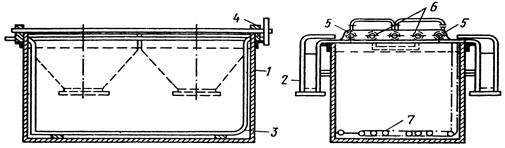
Рисунок 5 Гальваническая ванна для электроосаждения металлов:
1 – корпус; 2 вентиляционный кожух; 3 – змеевик для обогрева; 4 – изоляторы; 5 – анодные штанги; 6 – катодные штанги; 7 – барботер для перемешивания сжатым воздухом
В зависимости от того, в каком виде ион разряжающегося металла находится в растворе, все электролиты делятся на комплексные и простые. Разряд комплексных ионов на катоде происходит при более высоком перенапряжении, чем разряд простых ионов. Поэтому осадки, полученные из комплексных электролитов, более мелкозернисты и равномерны по толщине. Однако у этих электролитов ниже выход металла по току и более низкие рабочие плотности тока, т.е. по производительности они уступают простым электролитам, в которых ион металла находится в виде простых гидратированных ионов.
Распределение тока по поверхности изделия в гальванической ванне никогда не бывает равномерным. Это приводит к разной скорости осаждения, а следовательно, и толщине покрытия на отдельных участках катода. Особенно сильный разброс по толщине наблюдается на изделиях сложного профиля, что отрицательно сказывается на защитных свойствах покрытия. Равномерность толщины осаждаемого покрытия улучшается с увеличением электропроводности электролита, ростом поляризации с ростом плотности тока, уменьшением выхода металла по току при повышении плотности тока, увеличении расстояния между катодом и анодом.
Способность гальванической ванны давать равномерные по толщине покрытия на рельефной поверхности называется рассеивающей способностью. Наибольшей рассеивающей способностью обладают комплексные электролиты.
Для защиты изделий от коррозии используют гальваническое осаждение многих металлов: цинка, кадмия, никеля, хрома, олова, свинца, золота, серебра и др. Применяют также электролитические сплавы, например Cu – Zn, Cu – Sn, Sn – Bi и многослойные покрытия.
Наиболее эффективно (электрохимически и механически) защищают черные металлы от коррозии анодные покрытия цинком и кадмием.
Цинковые покрытия применяются для защиты от коррозии деталей машин, трубопроводов, стальных листов. Цинк – дешевый и доступный металл. Он защищает основное изделие механическим и электрохимическим способами, так как при наличии пор или оголенных мест происходит разрушение цинка, а стальная основа не корродирует.
Покрытия из цинка занимают доминирующее положение. С помощью цинка защищают от коррозии примерно 20 % всех стальных деталей, и около 50% производимого в мире цинка расходуется на гальванические покрытия.
В последние годы получили развитие работы по созданию защитных гальванических покрытий из сплавов на основе цинка: Zn – Ni (8 – 12% Ni), Zn – Fe, Zn – Co (0,6 – 0,8% Co). При этом удается повысить коррозионную стойкость покрытия в 2-3 раза.
Цинкование проводят в кислых, цианидных и цинкатных электролитах. Осаждение цинка происходит с высоким выходом по току. Цинковые покрытия отличаются высокой степенью чистоты, химической стойкостью и хорошими механическими свойствами.
Применение цианидных электролитов обеспечивает получение более мелкозернистых покрытий. Их используют для обработки деталей сложной формы. Однако эти электролиты экологически опасны. В некоторых случаях цианидные электролиты заменяют на щелочные цинкатные.
Все большее распространение получают цинковые комбинированные электрохимические покрытия (КЭП). Из сульфатного электролита получают КЭП с включениями корунда до 0,4 0,5 масс. %. Из цинкатного электролита с порошком карбонильного никеля получают КЭП с содержанием никеля 6 – 12 масс. %. На основе цинка получают также покрытия с частицами полимеров – капрона и полиамида, содержание которых в КЭП 0,9 – 3,1 масс. %. Эти покрытия в 1,5 раза более стойки к воздействию кислот, чем чистые цинковые покрытия.
Кадмий имеет более близкий потенциал к железу, чем цинк. Характер защиты кадмием зависит от коррозионной среды. Во влажной атмосфере в присутствии хлор-ионов потенциал кадмия становится электроотрицательнее потенциала железа, и кадмий электрохимически защищает металл от коррозии.
Необходимо учитывать высокую токсичность и дефицитность кадмия. Поэтому его применяют только для защиты особо важных деталей.
Для цинкования и кадмирования предложены электролиты, в которых металлы находятся в виде простых солей или в виде комплексных соединений. Наибольшее применение получили сульфатные электролиты. Их состав, г/л:
| Цинкование | Кадмирование |
|
Zn SO4 – 200 – 250 |
Cd SO4 – 40 – 60 |
|
Na2 SO4 – 50 – 100 |
(NH4)2SO4 – 240 – 250 |
|
Al2 (SO4)3 – 20 – 30 |
Препарат ОС-20 – 0,7 – 1,2 |
| Декстрин – 8 – 10 | Диспергатор НФ – 50 – 100 |
|
рН = 3,5 |
Уротропин – 15 – 20 |
Катодная плотность тока для цинкования 100 – 400 А/м2. Температура электролита для обоих процессов – 15 – 30 ºС.
Очень распространены никелевые покрытия. Их широко применяют для защиты изделий от коррозии и для декоративной отделки в машиностроении, приборостроении, автомобилестроительной, медицинской, электронной промышленности, при изготовлении предметов бытового потребления. Никелевые покрытия весьма стойки в атмосфере, растворах щелочей и некоторых органических кислот, что обусловлено сильно выраженной способностью никеля к пассивации в этих средах.
Никель в паре с железом является катодом, так как имеет более электроположительный потенциал, чем железо. Никель может защищать сталь только механическим путем, следовательно, покрытие не должно иметь пор и должно иметь большую толщину – 20 25 мкм. Существуют несколько разновидностей никелевых покрытий.
Никелирование матовое – нанесение на поверхность металлических деталей матового слоя никеля. Основным компонентом электролитов для получения матовых осадков никеля является сульфат никеля. В раствор вводят также сульфат натрия или магния для получения пластичных и полируемых покрытий, а также борную кислоту для поддержания устойчивого значения рН.
Блестящее никелирование используют для защитно-декоративной отделки поверхности. Блестящий никель можно наносить на детали со сложным профилем, он обладает пониженной коррозионной стойкостью по сравнению с матовыми покрытиями.
Никелирование черное – электролитическое нанесение на поверхность металлических изделий слоя никеля черного цвета. Такое покрытие используют как с защитно-декоративной целью, так и для уменьшения коэффициента отражения света. Оно нашло применение в оптической промышленности и в некоторых отраслях машиностроения. У черного никеля низкие показатели коррозионной стойкости, пластичности и прочности сцепления с поверхностью. Поэтому применяют предварительное оловянирование или осаждение матового никеля. Если применить предварительное цинкование, а затем осадить черный никель, то покрытия приобретают такую же коррозионную стойкость, как если бы они были покрыты только цинком. Часто черный никель наносят на изделия из меди или латуни.
Применяют также химический способ нанесения никеля на поверхность металлических изделий. Химически восстановленный никель отличается повышенной коррозионной стойкостью и твердостью. Он позволяет получать равномерные по толщине осадки, отличающиеся высокими декоративными свойствами и малой пористостью.
Усовершенствование процессов никелирования идет по пути создания новых электролитов и сплавов на основе никеля. Разработаны новые метансульфоновые растворы, из которых получают пластичные никелевые покрытия с низкими внутренними напряжениями.
Многослойные в два-три слоя никелевые покрытия обладают большей коррозионной стойкостью, чем однослойные. Первый слой никеля осаждают из простого никелевого электролита, а 2-й слой из электролита, содержащего серу, в составе органических добавок. Потенциал никеля, содержащего серу имеет более отрицательное значение, чем потенциал никеля без включений серы. Поэтому второй слой электрохимически защищает от коррозии первый слой никеля. Таким образом обеспечивается более высокая защита основного изделия.
Используют также двухслойное покрытие, называемое «сил-никель». Оно состоит из первого блестящего слоя никеля. Второй слой получают из электролита, содержащего в виде суспензии каолин. В ходе электролиза каолин осаждается вместе с никелем и включается в осадок.
Покрытия из сплавов Ni – W используются при изготовлении пуансонов штампов для производства телевизионных трубок. Совершенствуются процессы соосаждения Ni с фторопластом и MoS2. Введение в матрицу покрытия алмазных и других неметаллических составляющих позволяет существенно повысить твердость и износостойкость никелевых покрытий.
Использование многослойных никелевых покрытий обеспечивает значительную экономию никеля и повышает их эксплуатационные свойства.
Хромовые покрытия широко применяют для защиты от коррозии и механического износа различных машин и аппаратов.
Хромовые покрытия бывают защитно-декоративные и функциональные. Хром по отношению к стали является катодом, и при их контакте разрушаться будет сталь. Поэтому хромовые покрытия на стали должны быть сплошными и беспористыми.
Стальные изделия могут быть защищены от коррозии в атмосферных условиях однослойным хромовым покрытием толщиной не менее 40 мкм.
Для деталей из меди и медных сплавов осаждают хром по никелевому подслою. Детали из цинковых, алюминиевых, магниевых сплавов покрывают хромом после нанесения многослойного покрытия.
Основными компонентами электролитов для хромирования являются оксид хрома (VI) CrO3 и серная кислота. В водном растворе соединения Cr (VI) образуют смесь, состоящую из кислот H2Cr2O7 и H2CrO4. В растворе эти кислоты находятся в динамическом равновесии:
2H2 Cr O4 Û H2 Cr2 O7 + H2O
При электролизе на катоде одновременно происходит восстановление Cr+2 до Cr+3 и до металлического хрома, а также разряд ионов водорода. Выход по току хрома не превышает 15 – 25%. Хромирование – очень сложный процесс. Хром выделяется на катоде только при очень высоких плотностях тока (1000 – 3000 А/м2). Причем для каждой температуры имеется минимум плотности тока, ниже которого хром не осаждается.
Изменяя режим электролиза, можно получить блестящие, матовые (серые) или «молочные» осадки хрома. Блестящие осадки имеют наиболее высокую твердость, хорошее сцепление с основным металлом и наименьшую хрупкость. Матово-серые осадки отличаются высокой хрупкостью. Покрытия «молочным» хромом имеют высокую твердость, пластичность, значительно меньшую пористость и более высокую защитную способность.
Стальные детали приборов и машин, работающих в жестких условиях эксплуатации , покрывают двумя слоями хрома: нижний - молочный и верхний – блестящий. Это обеспечивает хорошую защиту от коррозии и высокую износостойкость при необходимых декоративных качествах.
Хромирование черное применяется для защитно-декоративной отделки деталей, поверхность которых наряду с коррозионной стойкостью должна иметь низкий коэффициент отражения света. По сравнению с другими покрытиями черного цвета черное хромовое покрытие отличается повышенной коррозионной стойкостью. Наносят черный хром по подслою молочного или блестящего хрома или никеля. Черные хромовые покрытия состоят на 75% из металлического хрома и на 25% из оксидов хрома.
Традиционные процессы получения хромовых покрытий из растворов, содержащих соединения Cr (VI), экологически опасны. ПДК для Cr (VI) равно 0,02 мг/л, а для Cr (III) – 0,07 мг/л. В связи с этим отработанные гальваностоки проходят сложную систему очистки. Первоначально соединения Cr(VI) восстанавливают до Cr(III). Если процесс восстановления проводят химическим путем, то применяют гидросульфит натрия – Na HS O3. Для полного восстановления соединений Cr (VI) требуется 5-7-кратный избыток гидросульфита и рН = 2 - 2,5. В процессе очистки часть Na HSO3 разлагается с выделением SO2, что приводит к дополнительному загрязнению атмосферы. Заключительная стадия очистки состоит в подщелачивании раствора до рН = 8,0-8,5 и осаждении Сг (ОН)3 вместе с другими примесями в осадок.
С целью улучшения экологической ситуации очень привлекательно выглядит идея получения осадков хрома из электролитов, содержащих соединения Сr (III). На этом пути возникают трудности, связанные с низким рН гидратообразования Сr(ОН)з, инертностью аквакомплексов Сr(Н2О)63+, образованием прочных внутриорбитальных комплексов и сложной конструкцией электролизера.
Разработанные электролиты на основе соединений Сr(III) не позволяли получить толстые слои. При достижении толщины в несколько микрон выделение хрома прекращается. Введение в раствор слабых лигандов, таких, как муравьиная или малоновая кислоты, а также ряда добавок позволяет получать толстые осадки хрома (до 100-200 мкм). Использование новых электролитов дало возможность проводить осаждение хрома с выходами по току до 25-45 % и скоростью 0,8-1,6 мкм/мин вне зависимости от времени.
В процессе электролиза растворов, содержащих ионы Сr3+, соединения Сr (VI) оказывают вредное влияние. Это требует усложнения конструкции электролизера и разделения диафрагмой или мембраной анодного и катодного пространства, так как шестивалентные ионы хрома (Сr6+) в основном образуются в результате химического взаимодействия с озоном, выделяющимся на аноде. Применение новых оксидных материалов, имеющих высокое перенапряжение для реакции образования соединений Сr (VI), позволило резко снизить выход по току Сrб+ и избежать конструктивного усложнения электролизера.
Таким образом, открываются перспективы для промышленного освоения новых передовых технологий нанесения защитных хромовых покрытий.
Оловянные покрытия применяют главным образом
для защиты от коррозии в растворах органических кислот и солей, содержащихся в
пищевых продуктах, а также от атмосферной коррозии в приборостроении, где
наряду с защитными свойствами необходимо обеспечить
паяемость изделия.
Олово в контакте со сталью является катодом, так как его потенциал имеет более положительное значение по отношению к железу. Однако в среде органических кислот олово образует комплексные соединения, и потенциал его становится более электроотрицательным.
В этих средах олово выступает как анод.
Около 50% добываемого олова расходуется на изготовление белой жести. С целью повышения коррозионной устойчивости производят оплавление оловянных покрытий. Блестящее оловянирование – это нанесение на поверхность металлических изделий блестящего слоя олова. По пористости и коррозионной стойкости они не отличаются от матовых покрытий, но обладают повышенной твердостью.
Для оловянирования применяют кислые и щелочные электролиты. Кислые электролиты просты по составу и работают при комнатной температуре. Они применяются для покрытия деталей простой конфигурации. Состав кислого электролита для покрытия оловом, г/л: Sn SO4 — 20-25; H2SO4 — 50-100; препарат ОС-20 2-5. Температура 15-30°С, плотность тока— 100-200 А/м2.
Для покрытия оловом сложных деталей применяют щелочной электролит состава, г/л: Na2Sn(OH)6 — 45-90; NaOHсвoб — 7-17; CH3COONa — 15. Температура 60-80 °С, плотность тока — 50-200 А/м2.
Свинец устойчив в среде серной кислоты и ее соединений. Свинец, как и олово, не может защищать стальные изделия электрохимически. Поэтому применяют свинцовые беспористые покрытия большой толщины (до 300 мкм), которые механически защищают детали из черных металлов в средах, содержащих серную и хромовые кислоты и их соли. Необходимо учитывать высокую токсичность свинца.
Для покрытия изделий свинцом в промышленности применяют борфтористоводородные или фенолсульфоновые электролиты. Осадки хорошего качества получают только в присутствии органических добавок. Состав электролитов, г/л:
| Борфтористоводородный | Фенолсульфоновый |
|
Pb (BF4)2 125-200 |
Рb(НОС6Н4SОз)2 170-180 |
|
HBF4 — 40-600 |
НО Сб Н4 S0з Н своб —20-25 |
| Клей столярный — 0,5-1,0 | Клей столярный — 0,4-0,5 |
Электролиз проводят при температуре 15-30 °С и плотности тока 50-200 А/м2
1.3 Термодиффузионный метод покрытия
Термодиффузионный метод был разработан в 1938 году Н.А. Изгарышевым и Э.С. Саркисовым и получил практическое применение. Сущность метода состоит в поверхностном насыщении основного металла атомами легирующего компонента в результате диффузии его при высоких температурах. Тем самым удается значительно снизить расход легирующего металла.
Для создания термодиффузионного покрытия должны существовать следующие необходимые условия:
- возможность образования твердого раствора основного металла с металлом покрытия;
- атомный радиус металла покрытия не должен превышать атомный радиус основного металла, что обеспечивает свободу перемещения атомов вглубь кристаллической решетки.
Термодиффузионные покрытия на железе могут создавать металлы: Сu, Аu, Zn, Ti, Al, Si, Cr, Mo и т.д. Из них наибольшее применение в промышленности нашли покрытия:
- алюминием термоалитирование;
- хромом термохромирование;
- кремнием термосилицирование.
Термодиффузионные покрытия рассмотрены ранее (см. часть 1, гл. I, п. 8).
Плакирование — термомеханический способ. Плакирование является наиболее совершенным методом защиты малостойких металлов сплавами или металлами, обладающими повышенной коррозионной стойкостью.
Способ плакирования заключается в том, что на матрицу основного металла накладывают с обеих сторон листы другого металла, затем весь пакет подвергают горячей прокатке. В результате термодиффузии на границе раздела металлов получают прочное многослойное изделие.
Для плакирования применяют металлы и сплавы, обладающие хорошей свариваемостью: углеродистые и кислотостойкие стали, дюралюмины, сплавы меди.
В качестве защитного покрытия для плакирования используют алюминий, тантал, молибден, титан, никель, нержавеющие стали.
Толщина плакирующего слоя колеблется от 3 до 40 % от толщины защищаемого металла. Плакированную сталь можно подвергать всем видам механической обработки, в том числе штамповке и сварке.
Металлургическая промышленность выпускает углеродистую сталь в виде листов марок Ст. З, 10, 15К, 20К и др., плакированную хромистыми, хромоникелевыми и другими высоколегированными сталями (08Х17Т, 08X13, 10Х17Н13М2Т, 15X25T, 12Х18Н10Т и др.) различной толщины. Известны также сплавы, плакированные медью, серебром, алюминием. В электрохимической промышленности нашли широкое применение бианоды - плакированные электроды, основу которых составляет титан или тантал, а защитный слой состоит из платины, родия, иридия.
Метод плакирования позволяет экономить дорогостоящие металлы или высоколегированные сплавы и находит широкое применение в промышленности.
1.4 Горячий метод, или метод погружения в расплавленный металл
Это старейший и наиболее простой способ нанесения металла на стальные листы, проволоку и готовые изделия. «Горячие» покрытия образуются при погружении защищаемого металла в расплав металла, используемого для покрытия. В качестве последних применяют металлы, имеющие невысокую температуру плавления: цинк (tпл= 419°С), олово (tпл = 232 °С), свинец (tпл = 327 °С), алюминий (tпл = 658°С).
Перед нанесением на металл покрытия его обрабатывают флюсом, состоящим из 52-56% хлорида аммония, 5-6% глицерина и остальное — хлорид покрываемого металла. Флюс защищает расплав от окисления и, кроме того, удаляет с поверхности оксидные и солевые пленки. К числу недостатков этого способа относятся сравнительно большой расход наносимого металла, неравномерность покрытия по толщине и невозможность нанесения металла на резьбу, в узкие отверстия и т.д.
Горячее лужение используют в пищевой промышленности. Горячее цинкование применяют для защиты готовых изделий от коррозии в атмосфере и в воде.
В химическом машиностроении используют нанесение на железо или сталь алюминия. Алюминиевые покрытия получают в ваннах с расплавленным алюминием, нагретым до 780-800 °С, погружая детали на 40-50 мин.
Большое применение нашел способ горячего свинцевания. Горячие свинцовые покрытия применяют для защиты мешалок, кранов, различной арматуры. При толщине покрытия в несколько миллиметров на железе получают плотный беспористый слой свинца.
Для защиты особо ответственных аппаратов или при работе с очень агрессивными средами применяют гомогенное свинцевание. По этому способу свинец наносится на предварительно луженую поверхность защищаемой конструкции в виде капель расплава, которые, смачивая деталь и растекаясь по поверхности, образуют гомогенное покрытие. Например, емкости, покрытые методом гомогенного свинцевания, применяются для хранения и транспортировки брома.
1.5 Металлизация напылением
Сущность метода состоит в нанесении расплавленного металла на поверхность защищаемого изделия с помощью струи сжатого воздуха или инертного газа. Частицы расплавленного металла, двигаясь с большой скоростью, ударяются о поверхность основного металла и сцепляются с ней, образуя металлическое покрытие. Металл поступает в распылитель в виде проволоки и расплавляется либо в газовом пламени, либо в электрической дуге, создающейся между двумя электродами. Проволока подается специальным механизмом со скоростью до 2,5 м/мин.
Покрытия наносят с целью защиты изделий от коррозионного воздействия среды, для восстановления изношенных трущихся поверхностей, для придания изделиям жаростойкости. Металлизацией можно покрывать большие сложной формы конструкции в собранном виде. На рис. 46 приведена схема устройства электрометаллизатора проволочного типа. Концы проволок, по которым проходит электрический ток, выходя из наконечника (4), встречаются, и возникает вольтовая дуга, под действием которой концы проволок расплавляются. Струя сжатого воздуха через сопло (5) распыляет расплавленный металл.
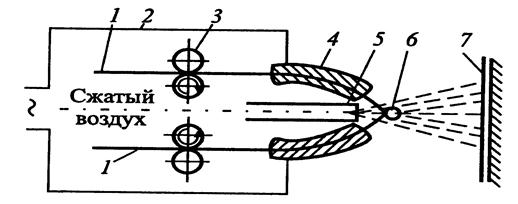
Рисунок Схема устройства электрометаллизатора:
1 проволока; 2 — корпус аппарата; 3 — механизм для протягивания проволоки; 4 наконечник; 5 — воздушное сопло; 6 — электрическая дуга; 7 — металлизируемая деталь.
Вместо двух проволок можно взять три и подавать на них ток от трехфазного источника тока. В этом случае образуется сочетание электрических дуг, горящих между концами различных проволок. Такой металлизационный аппарат применяют обычно для получения псевдосплавов (искусственных сплавов железа с медью, цинком, алюминием и т.д.). Полученные таким образом псевдосплавы обладают очень высокими антифрикционными свойствами.
При газовой металлизации происходит более мелкое и равномерное распыление металла. При электрической металлизации из-за невозможности одинакового оплавления концов проволоки в напыленном слое обнаруживают частицы различных размеров — от 10 мкм до 100 мкм. Такая неоднородность частиц по размерам ухудшает физико-механические свойства металлизированных покрытий.
Основной металл детали в процессе металлизации нагревается весьма незначительно, поэтому он не претерпевает структурных изменений, и его усталостная прочность не понижается.
Получаемое покрытие имеет чешуйчатую структуру и высокую пористость. При металлизации расходуется большое количество металла на угар и распыление, покрытие имеет пористую структуру, неравномерную толщину и низкую адгезию к металлу. Толщина получаемого слоя обычно равна 0,5-0,7 мкм.
Метод напыления применяется в промышленности для защиты крупногабаритных конструкций в собранном виде, например, газгольдеров, резервуаров и т.д. В химическом машиностроении он не нашел широкого применения вследствие недостатков, указанных выше. Известно только применение алюминиевых покрытий, полученных подобным способом, для защиты от коррозии оборудования заводов, перерабатывающих сернистые нефти, вулканизационных котлов и подобных аппаратов.
1.2 Неметаллические покрытия
1.2.1 Неорганические покрытия
Большинство металлов окисляется кислородом воздyxa с образованием поверхностных оксидных пленок. Однако эти пленки в силу незначительной толщины не обеспечивают надежной защиты от коррозии. Особенно слабы в этом отношении естественные пленки на железе.
Между тем в результате определенной химической или электрохимической обработки можно создать на поверхности металла искусственные пленки, которые обладали бы значительно более высокой коррозионной стойкостью, чем основной металл, и защищали бы его от разрушения.
Существуют различные методы получения таких неметаллических пленок, отличающихся химическим составом. Наиболее распространены оксидные и фосфатные пленки, хотя по защитным свойствам они уступают металлическим покрытиям. Процесс изготовления оксидных покрытий на металле получил название оксидирования, а фосфатных — фосфатирования.
Оксидирование. Основное назначение этого процесса — защита черных и цветных металлов от атмосферной коррозии.
Современный метод оксидирования — химическая и электрохимическая обработка деталей в щелочных растворах.
Электрохимическое оксидирование ведут в растворе 4% едкого натра при 65—120°С и анодной плотности тока от 2,5 до 10 А/дм2. Продолжительность анодной обработки не превышает 60 минут.
Качественное покрытие состоит из магнитной окиси железа, получающейся в результате последовательных превращений:
Fe → Na2 Fe 02 → Na2 Fe2 04 → Fe3 O4
Оксидирование черных металлов носит также название «воронения». Его осуществляют в растворе состава, г/л: Na OH — 600-700; Na NO2 — 200-250; Na NO3 — 50-100. Температура 135-145 °С, время 30-90 мин. В процессе происходит растворение железа с образованием соединений Na2FeO2 и Na2Fe204, из которых образуется поверхностная пленка оксида железа
Na2 Fe 02 + Na2 Fe2 04 + 2H2O = Fe3 O4 + 4 Na OH
Оксидная пленка на малоуглеродистой стали имеет глубокий черный цвет, а на высокоуглеродистых сталях — черный с сероватым оттенком. Для повышения антикоррозионных свойств оксидированное изделие погружают на 2-3 мин в горячий 2-3% раствор мыла, а затем на 5-10 мин - в минеральное трансформаторное или машинное масло при температуре 105-120 °С. После этой операции поверхность покрытия становится блестящей, с равномерной черной окраской. Возможно оксидирование и магниевых сплавов — в хромово-кислых электролитах с последующим нанесением лакокрасочных покрытий. Толщина оксидных пленок составляет 0,8-1,5 мкм.
Противокоррозионные свойства поверхностной пленки оксидов невысоки, поэтому область применения этого метода ограничена. Основное назначение его — декоративная отделка. Почти все стрелковое оружие и ряд точных приборов подвергают воронению, в результате чего изделия приобретают красивый черный цвет. Воронение используют и в том случае, когда необходимо сохранить исходные размеры изделия, так как оксидная пленка составляет всего 1,0-1,5 микрона.
Анодирование. Особенно широко применяется оксидирование алюминия и его сплавов. Это наиболее простой и надежный метод защиты их от коррозионного разрушения.
Процесс образования оксидных пленок на поверхности алюминия называют анодированием.
В обычных условиях на поверхности алюминия присутствует тонкая пленка оксидов Al2O3 или Al2O3 · nН2О, которая не может защитить его от коррозии. Под воздействием окружающей среды алюминий покрывается слоем рыхлых белых продуктов коррозии. Процесс искусственного образования толстых оксидных пленок может быть проведен химическим и электрохимическим способами.
Пленки, образующиеся при анодной обработке алюминия, обладают достаточной толщиной и рядом ценных свойств. Они защищают металл от коррозии и являются хорошим подслоем под лакокрасочные покрытия. Анодные пленки на алюминии обладают большим сопротивлением к истиранию, имеют высокое омическое сопротивление и хорошо окрашиваются, что позволяет придать изделиям из анодированного алюминия красивый вид. Для анодного окисления используют два типа электролитов.
В растворах слабых кислот (борная, винная, лимонная) и их солей оксидная пленка не растворяется. В этом случае получают беспористые, плотные, не проводящие электрический ток покрытия толщиной до 1 мкм. Такие пленки используют в качестве электроизоляционных покрытий в производстве конденсаторов.
Электролиты второго типа содержат растворы серной, хромовой и щавелевой кислот, в которых происходит частичное растворение оксидной пленки алюминия. В этих электролитах получают пористые пленки толщиной от 1 до 50 мкм.
На практике анодирование алюминия и его сплавов проводят в растворах серной кислоты концентрацией 180-200 г/л, хромового ангидрида (3 %) и щавелевой кислоты (3-10%) с плотностью тока 80-200 А/м2, при напряжении до 24В в течение 15-60 мин. Катоды выполняются из свинца или стали марки 12Х18Н9Т.
Для повышения защитных свойств изделие после оксидирования обрабатывают паром или горячей водой и далее в горячих растворах хроматов и бихроматов. При обработке паром в порах пленки образуется гидроксид алюминия, а в хромовых растворах - более стойкие соединения типа (АlО)2СrO4.
Оксид образуется на поверхности алюминия в результате анодного окисления
2А1 + ЗН2О = А12О3 + 6Н+ + 6 е
Он состоит из двух слоев: плотного барьерного слоя толщиной 0,01-0,1 мкм, расположенного непосредственно на поверхности металла, и внешнего пористого слоя толщиной до 200-400 мкм.
Химическое оксидирование алюминия и его сплавов осуществляют в щелочных хромистых растворах состава, г/л: Na2 Cr O4 — 15; Na OH — 2,5 и Na2CO3 — 50 при температуре 90-95 °С в течение 5-10 мин. Образуются пленки толщиной 3-4 мкм с невысокими механическими и диэлектрическими свойствами. Процесс простой, быстрый и не требует специального оборудования.
1.2.2 Фосфатирование
Технология процесса фосфатирования проста. Фосфатирование применяют для черных и цветных металлов, и оно состоит в обработке металлических деталей (например стальных) в горячем растворе фосфорно-кислых солей некоторых металлов, главным образом марганца, железа, цинка. При этом на поверхности изделия образуется пористая пленка, состоящая из труднорастворимых фосфатов этих металлов. Благодаря большой пористости пленка хорошо удерживает масло, краску и служит отличным грунтом под лакокрасочное покрытие. Сама фосфатная пленка не обладает высокими антикоррозионными свойствами и используется в качестве защитной в сочетании с лакокрасочными покрытиями или после пропитки ее маслом. В этом случае она надежно защищает сталь от коррозии. Иногда применяют обработку фосфатированного изделия в 7—9% растворе бихромата натрия, который заполняет поры и пассивирует нефосфатированные участки поверхности металла.
Обычно фосфатирование проводят при температуре 96—98° С погружением стальных изделий в раствор, содержащий 20—35 г/л препарата «Мажеф». В его состав входят фосфаты марганца и железа —Мn(Н2РО4)2, МпНРO4, Fe(H2PO4)2. Используют также раствор на основе дигидрофосфата цинка Zn(H2P04)2. Продолжительность фосфатирования 0,5—2 ч.
Основан метод на свойствах солей фосфорной кислоты. Фосфорная кислота Н3РО4 — может образовывать три вида солей:
1) однозамещенные - дигидрофосфаты Ме (Н2РО4)2;
2) двухзамещенные- гидрофосфаты Ме Н РО4;
3) трехзамещенные - фосфаты Ме3 (РО4)2 (где Me — двухвалентный металл).
В воде растворяются только фосфаты аммония и щелочных металлов. Двух- и трехзамещенные фосфаты железа, марганца и цинка малорастворимы. Следовательно, если создать условия для их образования, то они будут оставаться на поверхности металла.
При взаимодействии металла с фосфорной кислотой первоначально образуются дигидрофосфаты:
Me + 2Н3РО4 = Ме (Н2РО)2 + Н2
.
При снижении концентрации фосфорной кислоты получают вторичные и третичные соли:
Ме (Н2РО4)2 Û Ме НРО4 + Н3РО4;
3 Ме (Н2 РО4)2 Û Ме3 (РО4)2 + 4Н3РО4
В образовании фосфатной пленки участвуют продукты взаимодействия фосфорной кислоты с металлом и вещества, входящие в состав раствора для фосфатирования.
Предполагается, что образованию фосфатной пленки предшествуют реакции ионизации железа на анодных участках:
Fc Û Fe2+ + 2е
и выделение водорода на катодных участках
2Н+ + 2е Û Н2 ↑
Железо, переходящее в раствор, связывает фосфорную кислоту, и равновесие реакций смещается вправо. Выпадающие в осадок ди- и трифосфаты кристаллизуются на поверхности стального изделия, образуя плотную кристаллическую пленку.
Фосфатирование заканчивается после того, как вся поверхность покроется сплошной пленкой и выделение водорода прекратится. Фосфатирование используют для изделий, которые эксплуатируют в морской воде, в тропических районах. Недостатком фосфатных пленок являются низкая прочность и эластичность. Они имеют короткий срок эксплуатации.
1.2.3 Пассивирование
Для защиты от коррозии применяют метод пассивирования — обработка металла в растворах хроматов или нитратов.
Для пассивирования оцинкованных изделий применяют раствор: 8-10 мл/л H2SO4 и Na2Cr207·2H20 — 200 г/л. Время обработки 5-30 с. От времени обработки зависит окраска пленки. При выдержке 5 с цвет пленки радужный с зеленоватым оттенком, а масса пленки составляет 0,9-1,2 г/м2. При дальнейшем увеличении времени цвет меняется от желтого до коричневого.
Для пассивирования алюминия используют раствор бихромата калия (200 г/л) и 2 мл/л НF.
Пассивация меди в хроматных растворах дает особенно хорошие результаты при защите изделий, соприкасающихся с парами SO2 и растворами нейтральных солей. Стальные детали можно обрабатывать в 60-90% растворе нитрита натрия. В результате они не ржавеют в течение двух лет.
1.2.1 Эмали
Эмаль представляет собой стекловидную массу, получаемую сплавлением шихты (песок, мел, глина, полевой пшат и др.) и плавней (бура, сода, поташ, фтористые соли и др.). Кроме стеклообразующих веществ, в шихту вводят оксиды хрома, титана, цинка, повышающие жаростойкость, сцепляемость с металлом и придающие эмали нужную окраску.
Высокая химическая стойкость эмалей обусловлена присутствием буры и кремнезема; термостойкость обеспечивается близостью температурных коэффициентов линейного расширения покрытия и металла.
Наиболее жаростойкие эмали (так называемые керамические) выдерживают температуру 1100 ºС, а в отдельных случаях до 1400 ºС.
Эмалевые покрытия стойки к минеральным и органическим кислотам, солям, газовым средам, но разрушаются горячими растворами концентрированных щелочей, плавиковой кислоты и рядом фтористых соединений.
Эмалевую суспензию наносят на очищенную поверхность изделия погружением в расплав или пульверизацией из специального пистолета, после чего обжигают до спекания в пламенной или муфельной печи при температуре 880— 1050 ºС
1.2.2 Органические покрытия
Лакокрасочные покрытия. Защита металлов лакокрасочными покрытиями — наиболее старый и один из самых распространенных способов защиты от коррозии.
Основными достоинствами лакокрасочных покрытий
являются:
1) сравнительная дешевизна;
2) относительная простота нанесения;
3) легкость восстановления разрушенного покрытия;
4) сочетаемость с другими способами защиты, например протекторной защитой, фосфатными и оксиднымипокрытиями;
5) возможность получения покрытий любого цвета, обладающих наряду с защитными свойствами красивым внешним видом.
При соответствующем подборе материалов и способа нанесения эти покрытия обеспечивают достаточно надежную защиту металлических конструкций от коррозии в атмосфере и ряде коррозионных сред (окраска речных и морских судов, водонапорных баков и др.)
К недостаткам лакокрасочных покрытий следует отнести малую термостойкость (предельная температура наиболее термостойких красок 150 – 200 ºС), сравнительно невысокую механическую прочность, недостаточную стойкость в водной среде.
Ежегодно более 80 % металлоизделий, используемых в народном хозяйстве, подвергают окрашиванию. В 1999 г производство лакокрасочных материалов достигло 26,7 млн. т. Это свидетельствует об огромных масштабах средств, вовлеченных в сферу производства этого вида противокоррозионной защиты.
Эффективность применения лакокрасочных покрытий целесообразна при условии долговечности эксплуатации не более 10 лет и скорости коррозии металла до 0,05 мм/год. Если требуется повышение долговечности или скорость коррозии металла составляет 0,5-1,0 мм/год, то следует применять комбинированные покрытия. Например, цинковые плюс лакокрасочное покрытие. Такое покрытие позволяет увеличить срок защиты до 30 лет.
Защитные действия лакокрасочного покрытия заключаются в создании на поверхности металлического изделия сплошной пленки, которая препятствует агрессивному воздействию окружающей среды и предохраняет металл от разрушения.
Компонентами лакокрасочных материалов служат пленкообразующие вещества, растворители, пластификаторы, пигменты, наполнители, катализаторы (сиккативы).
Лаки — это коллоидные растворы высыхающих масел или смол в органических растворителях. Защитное твердое покрытие образуется вследствие испарения растворителя или полимеризации масла или смолы при нагревании или под действием катализатора.
Краски представляют собой суспензию минеральных пигментов в пленкообразователе.
Эмали — это раствор лака, в который введены измельченные пигменты.
Пленкообразователи — это природные масла, естественные или искусственные смолы. Масла по своему составу представляют собой сложные эфиры, т.е. являются продуктом взаимодействия кислот и спиртов. В основу классификации масел положена их способность к высыханию.
Наиболее распространенный масляный пленкообразователь — олифа. Натуральную олифу получают из высыхающих растительных масел, обработанных при 300 °С с целью частичной полимеризации. На воздухе олифа окисляется и полимеризуется до твердого состояния.
Растворители пленкообразующих веществ придают лакокрасочным покрытиям такую вязкость, при которой они легко наносятся на поверхность. В дальнейшем растворители испаряются. Растворителями могут быть: спирты, ацетон, бензин, скипидар, толуол, ксилол, этилацетат и др.
Пластификаторы или смягчители — это вещества, повышающие эластичность пленок после высыхания. К ним относятся касторовое масло, каучуки, дибутилфталат, трикрезилфосфат, эфиры адипиновой кислоты.
Количество пластификаторов, вводимых в смесь, составляет 20-75 % от массы пленкообразователя.
Краски и пигменты вводят в состав лакокрасочных композиций для придания им определенного цвета. Краски растворяются в растворителях, а пигменты находятся в них в нерастворимом мелкодисперсном состоянии. Размер частиц от 0,5 до 5 мкм. В качестве пигментов используют охру, сурик свинцовый, хром свинцовый, цинковые белила, порошки металлов. Пигменты повышают твердость, атмосферную и химическую стойкость, износостойкость и т.д.
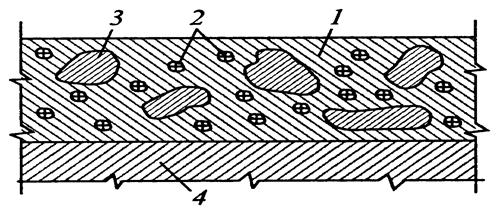
Рисунок Строение лакокрасочной пленки:
1 — пленкообразователь; 2 — наполнитель; 3 — пигмент; 4 — металл
Наполнители — это инертные вещества, которые вводят в лаки и краски для снижения расхода пигментов, а также для улучшения антикоррозионных свойств пленки. К ним относятся мел, тальк, каолин, асбестовая пыль и др.
Наполнители образуют прочную основу всей пленки. Частицы наполнителя распределяются в пленке между частицами пигмента и заполняют имеющиеся в ней промежутки. Благодаря этому пленка приобретает повышенную влагостойкость и антикоррозионные свойства. Схема строения лакокрасочной пленки представлена на рис.
Сиккативы или катализаторы представляют собой магниевые и кобальтовые соли жирных органических кислот. Их вводят в состав композиций для ускорения высыхания масляных пленок.
Успешная противокоррозионная защита лакокрасочными материалами в значительной степени зависит от соблюдения технологии получения покрытий. Основными факторами, влияющими на срок службы покрытия, являются:
1) способ подготовки поверхности;
2) методы нанесения и отверждения лакокрасочного покрытия;
3) толщина комплексного покрытия.
Для оценки влияния подготовки поверхности можно привести такой пример. Срок службы покрытия эмалью МЛ-12 (3 слоя), нанесенной по грунтовке ГФ-12 при пескоструйной обработке поверхности — 7 лет, при абразивной обработке 9 лет, при обезжиривании — 3 года, при фосфатировании с активатором — 12 лет. Активатор способствует формированию на поверхности малопористого мелкокристаллического фосфатного слоя с хорошей адгезией к металлу. Размер кристаллов 5-20 мкм.
Метод нанесения также оказывает влияние на срок службы покрытия. Так, срок службы покрытия алкидной эмалью ПОМ 15 (желтой) при нанесении в электрополе — 12 лет, пневмораспылением — 11 лет, безвоздушным распылением — 10 лет, струйным обливом — 9 лет, окунанием — 8 лет. Разницу в сроках службы покрытий объясняют различной структурой сформированных покрытий. Более мелкие и плотноупакованные структуры образуются при нанесении покрытий методом электростатического распыления.
Существуют противоречивые мнения по вопросу выбора толщины защитного лакокрасочного покрытия. По некоторым данным защитные свойства покрытия пропорциональны его толщине, по другим — повышение толщины не всегда приводит к увеличению его долговечности. Поэтому в каждом отдельном случае подбирается оптимальная толщина лакокрасочного покрытия.
Выбор лакокрасочного покрытия определяется условиями его эксплуатации. Для защиты аппаратов от воздействия кислот, щелочей, растворителей и агрессивных газов готовят лакокрасочные покрытия на основе фенолоформальдегидных, полихлорвиниловых, эпоксидных и фторорганических полимеров.
Лакокрасочные покрытия на основе эпоксидных соединений устойчивы в растворах Na OH (до 25%) при нагревании до 125 °С, в соляной (до 25%), серной (до 70%), фосфорной и азотной кислотах. Они эластичны, влаго- и атмосферостойкие в средах, содержащих CI2, HC1, хлороформ. Обладают высокими электроизоляционными и механическими свойствами.
Лаки и краски на основе полихлорвинила устойчивы к азотной, соляной, серной, уксусной и другим кислотам, щелочам и маслам. Они хорошо зарекомендовали себя в атмосферах, содержащих SO2, SO3, N2O3, NH3, HC1. Их используют для защиты гальванических ванн, аппаратов химводоочистки и др.
Полиуретановые лаки и краски применяют для защиты изделий из магниевых и алюминиевых сплавов. Они стойки в атмосфере нефтепродуктов.
Термостойкие покрытия получают на основе кремнийорганических соединений. Они могут длительно работать при температуре до 300°С, кратковременно выдерживают 500-800°С. Такие краски и эмали используют для окрашивания вентиляционных и сушильных установок, теплообменников и др.
Таблица - Распределение основных видов лакокрасочных покрытий
| Тип лакокрасочного материала | США | Европа | Япония |
| Общий объем производства, млн т | |||
| 6,4 | 7,9 | 2,0 | |
| Доля в общем объеме, % | |||
| ВСО | 2,7 | 15,0 | 1,4 |
| Водные | 11 | 11 | 11 |
| Порошковые | 5,2 | 12,3 | 3,6 |
| Органоразбавляемые | 55 | 55 | 80 |
Требования по экологии создают самые большие сложности при разработке прогрессивного ассортимента лакокрасочных материалов. По данным зарубежных фирм газовые выбросы, включающие растворители, составляют 100-185 г/м2 окрашиваемой поверхности. В 1991 г. на автомобильных производствах Европы этот показатель составлял 90 г/м2. В 1993 г. он снизился до 50 г/м2. Этому способствовало создание новых прогрессивных лакокрасочных материалов, отвечающих современным экологическим требованиям: с высоким сухим остатком (ВСО), водоразбавляемые и порошковые. В табл. показана общая тенденция к переходу на использование экологически благоприятных лакокрасочных материалов в трех основных регионах мира.
Материалы с высоким сухим остатком (ВСО) позволяют сократить на 30% потребление органических растворителей, снизить в среднем на 20-30 % расход лакокрасочных материалов, а также увеличить в 1,5-2 раза срок службы покрытия. В странах СНГ эти материалы находятся на стадии промышленного внедрения: полиэфир-меламиновая эмаль ПЭ-1282 (содержание нелетучих соединений — 65%, режим сушки — 30 минут при 130°С); эпоксиперхлорвиниловая эмаль ЭП-2154 (соответственно — 50 % и 3-5 часов при 20°С); эпоксидная грунт-эмаль ЭП-5227.
Водоразбавляемые лакокрасочные материалы занимают одно из ведущих мест в ассортименте продукции, отвечающей современным экологическим требованиям. Водные материалы применяются в основном при окрашивании изделий методом электроосаждения. Для этой цели используются водоразбавляемые лакокрасочные материалы на основе пленкообразователей-электролитов. Для электроосаждения используют грунтовки В-КЧ-0207, В-КФ-093, ВЭП-0190, эмали В-ФЛ-11990, МС-278, В-ЭП-2100.
Порошковые краски — новый вид современных лакокрасочных материалов. Их применение позволяет практически исключить опасность загрязнения окружающей среды, снизить пожаро- и взрывобезопасность при работе. В настоящее время ведутся работы, направленные на усовершенствование и удешевление этого вида покрытий. Новым классом современных лакокрасочных материалов являются модификаторы ржавчины.
Эффективность грунтовок-модификаторов определяется не только природой пленкообразователя, но и наличием специальных добавок, обеспечивающих пропитку ржавчины и максимальную стабилизацию продуктов коррозии. Промышленность выпускает грунтовки-модификаторы на основе водоразбавляемых пленкообразователей (ВА-ВА-0112, ВД-ВА-01 ГИСИ, ВД-К4-0184, ВД-К4-0251) и эпоксидные модификаторы (ЭП-0180, ЭП-0199 и ЭП-0191).
Одним из направлений повышения защитных свойств покрытий является направленная модификация серийных лакокрасочных материалов. В качестве модификаторов могут быть использованы различные поверхностно-активные вещества, выпускаемые промышленностью. Защитные свойства таких покрытий обусловлены образованием на поверхности комплексов, обеспечивающих пассивность металла.
Замедлить протекание анодного коррозионного процесса можно и введением в лакокрасочную композицию ингибиторов коррозии. К ним относятся хроматы, фосфаты металлов, азотсодержащие и силаксановые соединения. Эффект действия таких соединений связан с растворением ингибитора в диффундирующей воде из внешней среды и последующей адсорбцией его ионов или молекул на активных центрах металла.
Покрытие смолами и пластмассами
Пластмассы и смолы обладают высокой коррозионной стойкостью во многих агрессивных средах, в том числе в воде и ряде кислот и щелочей. Поэтому покрытия из этих материалов применяют для защиты металла от коррозии. Их наносят послойно в жидком состоянии (нагретом или растворенном) пламенным напылением или футеровкой листовым материалом.
Чаще других используют фенол-формальдегидные, эпоксидные, кремнийорганические смолы, асфальтобитумные покрытия.
Лаки на основе фенол-формальдегидных смол, известные под общим названием бакелитовых, стойки по отношению к большинству агрессивных сред, за исключением окислителей, щелочей и некоторых органических соединений. Их достаточно широко используют в химической промышленности. Лак готовят растворением резольной смолы в спирте. Обычно наносят 4—5 слоев лака, причем каждый слой сушат при температуре до 160—170° С. Недостаток бакелитового лака хрупкость.
Значительный интерес представляют лаки и композиции на основе эпоксидных смол, которые успешно применяют для защиты от коррозии емкостей, трубопроводов, цистерн и различных деталей химической аппаратуры.
Эпоксидные смолы — продукты поликонденсации многоатомных фенолов и соединений с эпоксигидрогруппой (например, эпихлоргидрином). Они стойки к щелочам, ряду растворителей (бензин, ацетон), нестойки к сильным окислителям. Эпоксидные смолы имеют хорошую адгезию с поверхностью металла. Высокой химической и термической стойкостью обладают кремнийорганические (силиконовые) смолы. Это органические соединения, в цепях которых кислород частично замещен кремнием. Силиконовая пленка, нанесенная на какой-либо материал, делает его поверхность водоотталкивающей. Лаки, приготовленные на основе кремнийорганических соединений, могут длительное время подвергаться действию температуры свыше 200°С, не изменяя внешнего вида и не становясь хрупкими. Особенно ценны в этом отношении фенилселиконы. Смешивая их с оксидами титана, можно получить покрытие, стойкое к нагреву до 600°С. Силиконовые покрытия характеризуются высокими диэлектрическими свойствами.
Для защиты металлических сооружений от подземной коррозии широко применяют битумно-пековые композиции. Их высокая химическая стойкость связана с присутствием в составе высокомолекулярных соединений, с трудом вступающих во взаимодействие с большинством агрессивных сред.
Футеровка стальной аппаратуры листами пластмасс достаточно хорошо защищает от коррозии в кислотах, щелочах и других агрессивных жидкостях. Наиболее стойким пластиком, не разрушающимся даже в растворах царской водки, плавиковой кислоты, органических растворителях, является фторопласт (тефлон). Однако его прочность относительно невелика. В качестве футеровочного материала используют также фаолит, винипласт, полиизобутилен, полиэтилен и др.
1.2.3 Гуммирование
Защита от коррозии химических аппаратов, трубопроводов, емкостей для перевозки и хранения химических продуктов резиной или эбонитом называется гуммированием. Аппараты, подвергающиеся сотрясениям, ударам, резким колебаниям температур, гуммируются мягкими резинами, содержащими от 2 до 4% серы, а аппараты, работающие при постоянной температуре и не подвергающиеся механическим воздействиям, - твердыми резинами (эбонитом). Применяют и комбинированные футеровки из резины и эбонита.
Нанесение покрытий производится путем облицовки поверхности изделий сырой резиновой смесью, которую прикатывают валиками, а затем вулканизируют. Для гуммирования чаще всего применяются резины и эбониты, получаемые на основе натурального, бутадиен – стирольного, бутадиен – нитрильного, бутил – каучука, хлоропреновых и фторсодержащих каучуков (см. часть 4, гл. V, п. 1.2). Такие покрытия устойчивы к хлороводородной, фтороводородной, уксусной, лимонной кислотам любой концентрации до температуры 65 ºС, к щелочам, нейтральным растворам солей, к 50% серной и 75% фосфорной кислотам, но они разрушаются сильными окислителями (азотной, концентрированной серной кислотами).
Покрытия смазками и пастами. Защитные смазки и пасты имеют ряд преимуществ перед другими покрытиями. Они легко наносятся на поверхность изделий, легко удаляются с нее и являются недорогими. Применяют эти покрытия для предохранения металлических изделий при хранении в закрытых помещениях и на открытых площадках, а некоторые смазки предохраняют изделия и во влажной атмосфере при наличии в ней CO2, SO2 и других газов.
Механизм защитного действия смазок состоит в создании на поверхности изделия тонкого защитного слоя, препятствующего проникновению агрессивной среды к поверхности металла.
Жидкие смазки получают на основе минеральных масел (авиационного, трансформаторного, машинного и других) с введением в их состав других добавок (парафин, мыла жирных кислот, нитрата натрия и др.) Например, смазка К-17 содержит девять компонентов, каждый из которых выполняет определенные функции
Защитные пасты получают из суспензий минерального воска (церезина), парафина, каучука, полиизобутилена в уайт-спирите. Их наносят на изделия тампоном, распылением. Для предохранения поверхности изделия от плесени в состав паст вводят фунгициды.
2. Обрабока коррозионной среды
В промышленных условиях эксплуатации в ряде случаев уменьшение потерь от коррозии может быть достигнуто при помощи изменения состава агрессивной среды. Используют два приема:
1) удаление из агрессивной среды веществ, вызывающих коррозию металлов;
2)введение в агрессивную среду специальных веществ, которые вызывают значительное снижение скорости коррозионного процесса. Такие вещества называются замедлителями или ингибиторами коррозии.
2.1 Снижение агрессивности коррозионной среды
Значительное изменение состава коррозионной среды может быть достигнуто одним из перечисленных способов:
а) удалением кислорода при помощи деаэрации раствора, насыщения его азотом или добавления в него поглотителей кислорода;
б) удалением кислот путем нейтрализации раствора гашеной известью или едким натром;
в) удалением солей из воды, идущей на питание паровых котлов, путем обработки ее ионообменными смолами;
г) вакуумированием.
В случае металлов, пассивирующихся в данной среде, присутствие в ней кислорода или других окислителей способствует процессу пассивации и ведет к торможению коррозии. Во всех остальных случаях окислители стимулируют коррозию металлов. Железо в аэрированных водных растворах корродирует с кислородной деполяризацией:
4Fe + 6Н2О + ЗО2 = 4Fe(OH)3.
Для снижения концентрации растворенного кислорода добавляют гидразин или сульфит натрия. Между гидразином и растворенным кислородом идет реакция
N2H4 + О2 = N2 + 2Н2О
Избыток гидразина разлагается на аммиак и азот
3N2H4 = N2 + 4NH3
Присутствие в воде аммиака ведет к увеличению щелочности и поэтому имеет положительный эффект.
Применение сульфита натрия менее эффективно, чем гидразина, т.к. увеличивает содержание солей в воде:
Na2SO3 + 1/2O2 = Na2SO4
.
Обработка водных растворов гашеной известью широко применяется в промышленности. Таким образом регулируют рН растворов, а также снижают содержание в них солей. При подщелачивании растворов образуются гидроксиды металлов, которые имеют более низкую растворимость, чем соответствующие соли. Часть гидроксидов выпадает в осадок, и содержание ионов металлов в растворе снижается.
Для глубокой очистки воды с целью предотвращения образования накипи в паровых котлах проводят ионообменную обработку. Как правило, применяют серию ионообменных аппаратов. Первоначально используют катионообменные смолы и воду очищают от катионов металла. На последующих стадиях проводят анионообменную очистку и освобождаются от анионов сильных и слабых кислот.
2.2 Ингибиторная защита
Ингибиторами коррозии (ИК) называют химические соединения, которые, присутствуя в коррозионной системе в достаточной концентрации, уменьшают скорость коррозии без значительного изменения концентрации любого коррозионного реагента. Ингибиторами коррозии могут быть и композиции химических соединений. Содержание ингибиторов в коррозионной среде должно быть небольшим.
Защиту ингибиторами применяют в системах с постоянным или мало обновляемым объемом коррозионной среды, например, в резервуарах, цистернах, паровых котлах, системах охлаждения, некоторых химических аппаратах, травильных ваннах для снятия окалины, а также при хранении и транспортировке металлических изделий.
Эффективность ингибиторов оценивается степенью защиты Z, %, и коэффициентом торможения γ (ингибиторный эффект) и определяется по формулам
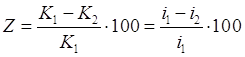 ,
,
где К1 и К2 [г/(м2·ч)] — скорость растворения металла в среде без ингибитора и с ингибитором соответственно; i1 и i2 [А/см] — плотность тока коррозии металла в среде без ингибитора и с ингибитором соответственно. При полной защите коэффициент Z равен 100%. Коэффициент торможения показывает, во сколько раз уменьшается скорость коррозии в результате действия ингибитора
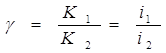 ;
;
Z и γ увязаны между собой:
![]()
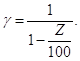
Ингибиторы подразделяются:
а) по механизму своего действия — на катодные, анодные и смешанные;
б) по химической природе — на неорганические, органические и летучие;
в) по сфере своего влияния — в кислой, щелочной и нейтральной среде.
Действие ингибиторов обусловлено изменением состояния поверхности металла вследствие адсорбции ингибитора или образования с катионами металла труднорастворимых соединений. Защитные слои, создаваемые ингибиторами, всегда тоньше наносимых покрытий.
Ингибиторы могут действовать двумя путями: уменьшать площадь активной поверхности или изменять энергию активации коррозионного процесса.
В результате адсорбции ингибитора происходит изменение структуры двойного электрического слоя. Экранирование части поверхности (Θ) сплошной пленкой ингибитора исключает ее из коррозионного процесса, который протекает на поверхности, равной (1 — Θ).
Катодные и анодные ингибиторы замедляют соответствующие электродные реакции, смешенные ингибиторы изменяют скорость обеих реакций. Адсорбция и формирование на металле защитных слоев обусловлены зарядом частиц ингибитора и способностью образовывать с поверхностью химические связи.
Катодные ингибиторы замедляют катодные реакции или активное растворение металла. Для предотвращения локальной коррозии более эффективны анионные ингибиторы. Часто для лучшей защиты металлов используют композиции ингибиторов с различными добавками.
Неорганические ингибиторы. Способностью замедлять коррозию металлов в агрессивных средах обладают многие неорганические вещества. Ингибирующее действие этих соединений обуславливается присутствием в них катионов (Са2+, Zn2+, Ni2+, As3+, Bi3+, Sb3+) или анионов (Cr2O42-, Cr2O72-, NO2-, SiO32-, РO43-).
Неорганические катодные ингибиторы уменьшают скорость коррозии вследствие снижения эффективности катодного процесса или сокращения площади катодов.
Снижение эффективности катодного процесса может быть достигнуто: а) при коррозии с кислородной деполяризацией — уменьшением содержания кислорода в жидкой коррозионной среде; б) при коррозии с водородной деполяризацией повышением перенапряжения реакции выделения водорода.
Уменьшение содержания растворенного в коррозионной среде кислорода тормозит реакцию его восстановления, а следовательно, и скорость коррозии.
Перенапряжение водорода может быть повышено при введении в коррозионную среду солей некоторых тяжелых металлов — As Cl3, Bi2(SO4)3. Происходит контактное осаждение этих металлов, что затрудняет реакцию выделения водорода и тем самым - процесс коррозии, так как он протекает с водородной деполяризацией. На рис. 48 показано влияние небольшой добавки As2O3 (0.045% в пересчете на мышьяк) на скорость коррозии углеродистой стали в серной кислоте.
Сокращение площади катодов достигается добавлением экранирующих катодных ингибиторов, которые образуют на микрокатодах нерастворимые соединения, отлагающиеся в виде изолирующего защитного слоя. Для железа в водной среде такими соединениями могут быть Zn SO4, Zn CI2, а чаще Са(НСО3)2.
Бикарбонат кальция Са(НСО3)2 — самый дешевый катодный экранирующий ингибитор, применяемый для защиты стали в системах водоснабжения. Бикарбонат кальция в подщелоченной среде образует нерастворимые соединения СаСО3, осаждающиеся на поверхности, изолируя ее от электролита. Этим объясняется меньшая коррозия стали в жесткой воде по сравнению с умягченной.
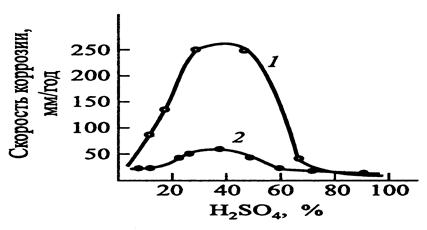
Рисунок - Зависимость скорости коррозии стали в растворах H2SO4:
1 – H2SO4; 2 – H2SO4 + As3+ (0,045%)
Катодные ингибиторы по защитному действию менее эффективны, чем анодные. Однако они совершенно безопасны, так как не вызывают усиления коррозии при их недостаточном содержании.
Анодные неорганические ингибиторы образуют на поверхности металла тонкие (~ 0,01 мкм) пленки, которые тормозят переход металла в раствор. К группе анодных замедлителей коррозии относятся химические соединения пленкообразователи и окислители, часто называемые пассиваторами.
Катодно-анодные неорганические ингибиторы, например KJ, КВг в растворах кислот, тормозят в равной степени анодный и катодный процессы за счет образования на поверхности металла хемосорбционного слоя.
Пленкообразующие ингибиторы защищают металл, создавая на его поверхности фазовые или адсорбционные пленки. В их число входят некоторые соединения со щелочными свойствами: фосфаты; полифосфаты; силикаты; бораты и др.
Их ингибирующее действие проявляется только при наличии растворенного кислорода, который и играет роль пассиватора. Не являясь окислителями, эти вещества лишь способствуют адсорбции кислорода на поверхности металла. Кроме того, они тормозят анодный процесс растворения из-за образования защитных пленок, представляющих собой труднорастворимые продукты взаимодействия ингибитора с ионами переходящего в раствор металла. Так, например, фосфаты, адсорбируясь на поверхности стали, образуют с ионами железа экранирующие пленки, состоящие из смеси γ·Fe2О3 и FePO4·2H2O. Для большего защитного эффекта фосфаты часто используются в смеси с полифосфатами.
Чаще всего в качестве пассиваторов используют неорганические окислители: хроматы, нитриты, молибдаты, вольфраматы. Легко восстанавливаясь на катодных поверхностях, они ведут себя как деполяризаторы, вызывая появление на анодных участках плотностей тока, превышающих величины, необходимые для их пассивации. При этом стационарный потенциал облагораживается на несколько десятых вольта, а скорость анодного перехода в раствор ионов корродирующего металла резко снижается.
Пассиваторы тормозят анодную реакцию растворения металла благодаря образованию на его поверхности оксидов
Me + nН2О → Ме Оn + 2nН+ + 2nе
Эта реакция может протекать только на металлах, склонных к пассивации.
Анодные ингибиторы коррозии относятся к категории опасных, так как при определенных условиях они из замедлителей коррозии превращаются в ее стимуляторы. Это чаще всего происходит, когда коррозионный процесс протекает с катодным контролем, и по тем или иным причинам не обеспечивается пассивация анодных участков. В данном случае сильные окислители, являющиеся хорошими деполяризаторами, легко восcтанавливаются на катодных участках и увеличивают скорость коррозии. Для того чтобы этого не произошло, плотность коррозионного тока должна быть выше той, при которой достигается полная пассивация анодных участков. Поэтому концентрация ингибитора (пассиватора) не должна быть ниже определенной величины, иначе пассивация может не наступить или будет неполной.
Неполная пассивация также очень опасна, так как приводит к сокращению анодной поверхности, увеличению скорости и глубины разрушения металла на локализованных участках, т.е. появлению точечной коррозии.
Минимальная концентрация Cr O42-, NO22-, Mo O42-, используемых в качестве ингибиторов коррозии стали, приблизительно равна 10-4 —10-3 моль/л. При повышении температуры среды или наличии в ней активаторов, например хлор-ионов, необходимо увеличение концентрации ингибитора.
Анодные замедлители неокислительного типа (фосфаты, силикаты и др.), добавленные в незначительном количестве, также вызывают более глубокую местную коррозию из-за сильного увеличения соотношения катодной площади к анодной.
Таким образом, для обеспечения эффективной защиты необходимо поддерживать концентрацию анодного ингибитора выше предельного значения во всех участках защищаемого изделия (например, в резьбовых соединениях, щелях и других труднодоступных местах).
Анодные ингибиторы очень чувствительны и к рН среды.
Применение анодных ингибиторов разнообразно.
Хроматы и бихроматы натрия и калия используются как ингибиторы коррозии железа, оцинкованной стали, меди, латуни и алюминия в промышленных водных системах. В случае железа действие хроматов описывают реакциями:
2Fe + 2Na2Cr04 + 2Н2О = Сг2 О3 + Fe2O3 + 4Na OH,
6 Fe3 O4 + 2 Na2 Cr04 + 2H2O = Сг2 О3 + 9 Fe2 O3 + 4 Na OH
Оксидная пленка состоит из 25 % Сг2 О3 и 75 % Fe2O3.
Нитриты применяются в качестве ингибиторов коррозии многих металлов (кроме цинка и меди) при рН более 5. Они дешевы и эффективны в случае присутствия ржавчины.
Защитное действие нитритов состоит в образовании поверхностной оксидной пленки по уравнению
2 Fe + Na NO2 + 2H2O = Fe2 O3 + Na OH + NH3
.
Силикаты относятся к ингибиторам смешанного действия, уменьшая скорости как катодной, так и анодной реакций.
Общая формула силикатов — xSi O2·Me2O. Действие силикатов (рис. 49) состоит в нейтрализации растворенного в воде углекислого газа и в образовании защитной пленки на поверхности металла.
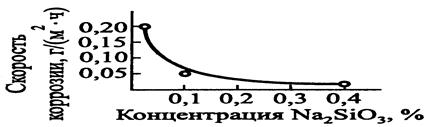
Рисунок - Зависимость скорости коррозии стали в нейтральных водных растворах от концентрации Na2 Si O3
Пленка не имеет постоянного состава. По структуре она напоминает гель кремниевой кислоты, в которой адсорбируются соединения железа и соли жесткости. Ее толщина обычно равна ≈ 0,002 мм.
Полифосфаты растворимые в воде соединения метафосфатов общей формулы (Ме Р О3)n. Защитное действие полифосфатов состоит в образовании непроницаемой защитной пленки на поверхности металла. В водных растворах происходит медленный гидролиз полифосфатов, в результате образуются ортофосфаты:
![]() ,
,
![]() .
.
В присутствии Са2+ и Fe3+ на поверхности образуется непроницаемая защитная пленка:
![]() ,
,
![]()
Наибольшее распространение в промышленности получил гексаметафосфат натрия. Фосфаты и полифосфаты находят применение в качестве замедлителей коррозии стали в воде и холодильных рассолах. Большой эффект достигается при совместном использовании фосфатов и хроматов.
2.2.1 Органические ингибиторы.
Многие органические соединения способны замедлить коррозию металла. Органические соединения — это ингибиторы смешанного действия, т.е. они воздействуют на скорость как катодной, так и анодной реакций. Значительное влияние на развитие теории ингибирующего действия специальных добавок оказали исследования А.Н. Фрумкина и его сотрудников. Современные представления электрохимической кинетики позволяют в ряде случаев предвидеть направление течения той или иной реакции при введении в электролит специальных добавок. Удалось объяснить основные закономерности, наблюдающиеся при использовании в качестве ингибиторов галоидных ионов, органических катионов и соединений молекулярного типа. Экспериментальные данные показали, что многие химические соединения адсорбируются на поверхности металла в соответствии с изотермами Ленгмюра или Темкина.
Органические ингибиторы адсорбируются только на поверхности металла. Продукты коррозии их не адсорбируют. Поэтому эти ингибиторы применяют при кислотном травлении металлов для очистки последних от ржавчины, окалины, накипи. Органическими ингибиторами коррозии чаще всего бывают алифатические и ароматические соединения, имеющие в своем составе атомы азота, серы и кислорода.
Амины применяют как ингибиторы коррозии железа в кислотах и водных средах.
Тиолы (меркаптаны), а также органические сульфиды и дисульфиды проявляют более сильное ингибирующее действие по сравнению с аминами. Основные представители этого класса—тиомочевина, бензотриазол, алифатические меркаптаны, дибензилсульфоксид.
Органические кислоты и их соли применяют как ингибиторы коррозии железа в кислотах, маслах и электролитах, а также как ингибиторы процесса наводороживания. Наличие в органических кислотах амино- и гидроксильных групп улучшает их защитные свойства. Среди этой группы особенно выделяют бензоат натрия.
Спирты, особенно многоосновные, — эффективные ингибиторы коррозии. В водных системах охлаждения—этиленгликоль НОСН2-СН2ОН, в морской и речной воде — глюконат натрия NaOOC(CHO-Н)4СН2ОН.
Необычайно широко применение ингибиторов в промышленности. В щелочных средах ингибиторы используются при обработке амфотерных металлов, защите выпарного оборудования, в моющих составах, для уменьшения саморазряда щелочных источников тока.
В последние годы появились новые смесевые ингибиторы для защиты стальной арматуры в железобетоне. Эти соединения — лигносульфонаты, танины, аминоспирты — способны образовывать с катионами железа труднорастворимые комплексы. Среди них особое внимание заслуживают таннины, благодаря их положительному влиянию на бетон и способности взаимодействовать с прокорродировавшей сталью. Новый класс ингибиторов — это мигрирующие ингибиторы. Они обладают способностью диффундировать через слой бетона и адсорбироваться на поверхности стальной арматуры, замедляя ее коррозию. Впервые мигрирующие ингибиторы — MCI 2000 и 2200 - были применены американской фирмой Cortec Corporation. В настоящее время появились отечественные разработки — ингибитор ИФХАН-16.
Из ингибиторов для нейтральных сред следует выделить группу ингибиторов для систем охлаждения и водоснабжения. Видное место здесь занимают полифосфаты, поликарбоксильные аминокислоты, так называемые комплексоны — ЭДТА, НТА и др.; и их фосфорсодержащие аналоги — ОЭДФ, НТФ, ФБТК. Комплексоны защищают металлы только в жестких водах, где они образуют соединения с катионами Са2+ и Mg2+.
В мягких водах хорошие результаты получены с солями высших карбоксилатов, на основе которых созданы ингибиторы ИФХАН-31 и -34. Они надежно защищают охлаждающие системы, состоящие из различных конструкционных материалов (Fe, Сu, Al, Zn и их сплавы).
Летучие ингибиторы являются современным средством защиты от атмосферной коррозии металлических полуфабрикатов и готовых изделий на время их хранения и транспортировки. Принцип действия летучих ингибиторов коррозии заключается в образовании паров, которые диффундируют через слой воздуха к поверхности металла и защищают ее.
Летучие ингибиторы коррозии раньше использовались преимущественно для защиты военной техники и энергетического оборудования. В последние годы к известным летучим ингибиторам НДА, КЦА, Г-2, ИФХАН-1, ВНХ-Л-20, ИФХАН-100, ВНХЛ-49 добавился ряд новых — ИФХАН-8А, -112, -118 и ВНХ-ЛФ-408. Установлена способность лучших летучих ингибиторов защищать металл от коррозии длительное время (более 3 месяцев) даже после удаления их из упаковочного пространства — эффект последействия.
На практике получили применение пассивирующие растворы ИФ-ХАН-39А и ИФХАН-33-ЛГ, которые применяют для защиты оксидированной и фосфатированной стали взамен их промасливания. Они пропитывают пористые покрытия и после сушки придают ему антикоррозионную стойкость. В последние годы видное место заняли ингибированные восковые составы. Объединяя в себе полезные качества тонкопленочных покрытий и масел, они формируют на поверхности металлов тонкие пластичные пленки. Наличие в них ингибиторов в совокупности с гидрофобностью воска обеспечивает сильный эффект антикоррозионного последействия. В настоящее время ведущую роль в практике противокоррозионной защиты играют пленкообразующие ингибированные нефтяные составы. Широкую известность получили Мовиль, Мовитин, ИФХАН-29А, НГ-216, Оремин, ИФХАН-ЗОА и -30Т.
Коррозионная активность нефти колеблется в очень широких пределах. Это обусловлено различным содержанием в ней коррозионноактивных примесей и сероводорода. В нефти может содержаться также неэмульгированная вода и вода в виде устойчивой эмульсии. Концентрация солей в воде может достигать 10 %. Опасность коррозии оборудования сохраняется на всех стадиях — при добыче, транспортировке, хранении и переработке нефти. Поэтому одни и те же типы ингибиторов используются как на стадии добычи, так и на стадии переработки нефти. Ингибиторы, которые добавляют в нефть, адсорбируются на поверхности металла полярной группой таким образом, что углеводородная цепь оказывается на внешней стороне образовавшейся пленки, вызывая гидрофобизацию поверхности. К ней присоединяется масло или другие углеводороды, благодаря чему на поверхности металла возникает двойная пленка, препятствующая протеканию коррозии. Хорошими защитными свойствами обладают соединения, в молекулу которых входят кислород и длинная углеводородная цепь с более чем десятью атомами углерода. Широкое применение в нефтедобыче получила технология рассредоточенного ингибирования, суть которого заключается в приближении точек его подачи к наиболее коррозионно-опасным участкам. Кроме отечественного ингибитора Олазол-Т2П, применяют импортные продукты Корексит-6350 (Налко-Эксен), ИСА-148 (Серво).
Проблема внутренней коррозии газопроводов является одной из важнейших проблем в газовой промышленности. Почти все месторождения содержат в составе газа большое количество СO2 (до 20 об. %), а в некоторых случаях и сероводород (до 25 об.%). Защита ингибиторами внутренней поверхности трубопроводов является одним из действенных методов противокоррозионной защиты.
Ингибитор коррозии - антивспениватель ИФХАНГАЗ-1 получил широкое применение в газовой промышленности. В результате взаимодействия ингибитора с сероводородом на поверхности металла возникает прочное соединение, которое затрудняет протекание электрохимических реакций.
Совместно с французской фирмой СЕКА разработаны ингибиторы коррозии серии СЕКАНГАЗ (Секангаз 9, 9Б и 10)
Их основу составляют производные жирных аминов. Эти вещества представляют собой полярные молекулы, адсорбирующиеся на поверхности металла. Жирная липофильная цепочка удерживает масляный слой, который препятствует контакту воды с металлом. Совместно с немецкими фирмами БАСФ и ХЕХСТ созданы ингибиторы Сепакор 5478 и Додиген 4482-1. Ингибитор Сепакор 5478 рекомендован для непрерывной закачки в пласт. Расход ингибитора составляет 14 л на 1 млн м3 газа. Ингибитор подается в скважину в виде 16% раствора в метаноле. В результате испытаний показано, что общая скорость коррозии составила 0,005 мм/год, а степень защиты от охрупчивания достигла 98 %. Аналогичные результаты получены и для ингибитора Додиген 481. Его термостабильность равна 200°С, и он рекомендован для технологий, предусматривающих как непрерывную, так и периодическую закачку в скважины и наземные трубопроводы.
3. Электрохимическая защита
Скорость электрохимической коррозии можно значительно уменьшить, если металлическую конструкцию подвергнуть поляризации. Этот метод получил название электрохимической защиты, В зависимости от вида поляризации различают катодную и анодную защиту.
На рис. 50 приведена схема, поясняющая снижение скорости растворения металла при различных способах его электрохимической защиты.
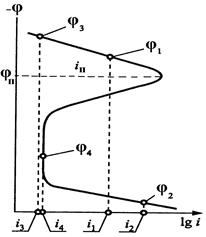
Рисунок Способы снижения скорости растворения металлов при электрохимической защите
Электрохимическую защиту применяют в том случае, если потенциал свободной коррозии φкор конструкционного материала располагается в области активного растворения φ1 или перепассивации φ2, то есть материал растворяется с высокой скоростью.
При катодной защите снижение скорости растворения металла происходит вследствие смещения потенциала в область значений, отрицательнее φкор. Например, если потенциал свободной коррозии φ1 металла располагается в области активного растворения (скорость растворения i1), то сдвиг потенциала в отрицательную сторону до значения φ3 приводит к снижению скорости растворения до величины i3, оказывающейся ниже i1. Аналогичное снижение скорости растворения металла происходит и в случае, когда потенциал свободной коррозии φ2 металла располагается в области перепассивации. При смещении потенциала в отрицательную сторону до величины φ4 скорость растворения снижается до i4. Различие заключается в том, что в первом случае снижение скорости растворения металла достигнуто без изменения характера его растворения — металл остался в активном состоянии. Во втором случае скорость растворения снизилась вследствие перехода металла из активного в пассивное состояние.
При анодной защите потенциал защищаемой конструкции смещают в
область положительнее φкор. При этом происходит переход металла
из активного в пассивное состояние. Так, если потенциал свободной коррозии
φ1 металла располагается в активной области
и соответствующая ему скорость растворения равна i1, то при его смещении в
положительную сторону до значения φ4 скорость растворения
снижается до величины i4.
3.1 Катодная защита
Катодная защита — наиболее распространенный вид электрохимической защиты. Она применяется в тех случаях, когда металл не склонен к пассивации, то есть имеет протяжненную область активного растворения, узкую пассивную область, высокие значения тока пассивации (iп) и потенциала пассивации (φп).
Катодную поляризацию можно осуществлять путем присоединения защищаемой конструкции к отрицательному полюсу внешнего источника тока или к металлу, имеющему более электроотрицательный электродный потенциал. В последнем случае нет надобности во внешнем источнике тока, так как образуется гальванический элемент с тем же направлением тока, т. е. защищаемая деталь становится катодом, а более электроотрицательный металл, называемый протектором, — анодом.
Катодная защита внешним током. Катодную защиту с использованием поляризации от внешнего источника тока применяют для защиты оборудования из углеродистых, низко- и высоколегированных и высокохромистых сталей, олова, цинка, медных и медно-никелевых сплавов, алюминия и его сплавов, свинца, титана и его сплавов. Как правило, это подземные сооружения (трубопроводы и кабели различных назначений, фундаменты, буровое оборудование), оборудование, эксплуатируемое в контакте с морской водой (корпуса судов, металлические части береговых сооружений, морских буровых платформ), внутренние поверхности аппаратов и резервуаров химической промышленности. Часто катодную защиту применяют одновременно с нанесением защитных покрытий. Уменьшение скорости саморастворения металла при его внешней поляризации называют защитным эффектом.
Основным критерием катодной защиты является защитный потенциал. Защитным потенциалом называется потенциал, при котором скорость растворения металла принимает предельно низкое значение, допустимое для данных условий эксплуатации. Характеристикой катодной защиты является величина защитного эффекта Z, %:
![]() ,
,
где K0 [г/(м2·ч)] скорость коррозии металла без защиты, К1 [г/(м2·ч)] скорость коррозии металла в условиях электрохимической защиты. Коэффициент защитного действия К3 [г/А] определяют по формуле
К3 = (Dm0 - Dmi)/iK,
где Dmo и Dmi — потери массы металла соответственно без катодной защиты и при ее применении, г/м2; iк [А/м2] плотность катодного тока.
Схема катодной защиты представлена на рис. 51. Отрицательный полюс внешнего источника тока 4 присоединен к защищаемой металлической конструкции 1, а положительный полюс – к вспомогательному электроду 2, работающему как анод. В процессе защиты анод активно разрушается и подлежит периодическому восстановлению.
|
|
| Рисунок - Схема катодной защиты внешним током | Рисунок - Схема катодной защиты плавильного котла: 1 — котел; 2 — источник тока; 3 —анод |
В качестве материала анода применяют чугун, сталь, уголь, графит, металлический лом (старые трубы, рельсы и др.). Так как эффективное сопротивление прохождению электрического тока оказывает только тот слой почвы, который находится в непосредственной близости от анода, то его обычно помещают в так называемую засыпку 3— толстый слой кокса, в который добавляют 3—4 части (по массе) гипса и 1 часть поваренной соли. Засыпка имеет высокую электропроводность, благодаря чему снижается переходное сопротивление почва—анод.
Источниками внешнего тока при катодной защите служат станции катодной защиты, обязательными элементами которых являются: преобразователь (выпрямитель), вырабатывающий ток; токоподвод к защищаемой конструкции, электрод сравнения, анодные заземлители, анодный кабель.
Станции катодной защиты бывают регулируемые и нерегулируемые. Нерегулируемые станции катодной защиты применяются в том случае, когда изменения сопротивления в цепи тока практически отсутствуют. Указанные станции работают в режиме поддержания постоянного потенциала или тока и применяются для защиты резервуаров, хранилищ, высоковольтных кабелей в стальной броне, трубопроводов и др.
Регулируемые станции катодной защиты применяются при наличии в системе блуждающих токов (близость электрифицированного транспорта), периодических изменений сопротивления растеканию тока (сезонные колебания температуры и влажности грунтов), технологических колебаний (изменение уровня раствора и скорости течения жидкости). Регулируемым параметром может служить ток или потенциал. Частота расположения станций катодной защиты по длине защищаемого объекта определяется электропроводностью эксплуатационной среды. Чем она выше, тем на большем расстоянии друг от друга будут располагаться катодные станции.
Для защиты сооружений в воде аноды устанавливают на дне рек, озер, морей. В этом случае засыпка не требуется.
Катодную защиту заводской аппаратуры (холодильников, теплообменников, конденсаторов и др.), подвергающейся воздействию агрессивной среды, осуществляют путем подсоединения к отрицательному полюсу внешнего источника тока и погружения анода в эту среду.
Катодную защиту внешним током применяют как дополнительное средство к изоляционному покрытию. При этом изоляционное покрытие может иметь повреждения. Защитный ток протекает в основном по обнаженным участкам металла, которые и нуждаются в защите.
Применяют катодную защиту внешним током и к конструкциям, имеющим значительные повреждения, что позволяет приостановить дальнейшее распространение коррозии.
Использование катодной защиты сопряжено с опасностью так называемой перезащиты. В этом случае вследствие слишком сильного смещения потенциала защищаемой конструкции в отрицательную сторону может резко возрасти скорость выделения водорода. Результатом этого является водородное охрупчивание или коррозионное растрескивание материалов и разрушение защитных покрытий.
Катодная защита внешним током нецелесообразна в условиях атмосферной коррозии, в парообразной среде, в органических растворителях, так как в этом случае коррозионная среда не обладает достаточной электропроводностью.
Протекторная защита. Протекторная защита является разновидностью катодной защиты. Схема протекторной защиты трубопровода показана на рис. 53. К защищаемой конструкции 2 присоединяют более электроотрицательный металл протектор 3, который, растворяясь в окружающей среде, защищает от разрушения основную конструкцию.
После полного растворения протектора или потери контакта его с защищаемой конструкцией протектор необходимо заменить.
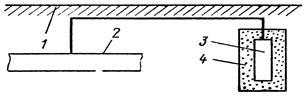
Рисунок - Схема протекторной защиты трубопровода
Протектор работает эффективно, если переходное сопротивление между ним и окружающей средой невелико. В процессе работы протектор, например цинковый, может покрываться слоем нерастворимых продуктов коррозии, которые изолируют его от окружающей среды и резко увеличивают переходное сопротивление. Для борьбы с этим протектор помещают в наполнитель 4 — смесь солей, которая создает вокруг него определенную среду, облегчающую растворение продуктов коррозии и повышающую эффективность и стабильность работы протектора в грунте 1.
Действие протектора ограничивается определенным расстоянием. Максимально возможное удаление протектора от защищаемой конструкции называется радиусом действия протектора. Он зависит от ряда факторов, важнейшими из которых являются электропроводность среды, разность потенциалов между протектором и защищаемой конструкцией, поляризационные характеристики. С увеличением электропроводности среды защитное действие протектора распространяется на большее расстояние. Так, радиус действия цинкового протектора при защите стали в дистиллированной воде равен 0,1 см, морской воде 4 м, в 3% растворе Na Cl – 6 м
Протекторную защиту по сравнению с катодной защитой внешним током целесообразно использовать в тех случаях, когда получение энергии извне связано с трудностями или если сооружение специальных электролиний экономически невыгодно.
В настоящее время протекторную защиту применяют для борьбы с коррозией металлических конструкций в морской и речной воде, грунте и других нейтральных средах. Использование протекторной защиты в кислых средах ограничивается высокой скоростью саморастворения протектора.---
В качестве протекторов можно применять металлы: Al, Fe, Mg, Zn. Однако использовать чистые металлы в качестве протекторов не всегда целесообразно. Так, например, чистый цинк растворяется неравномерно из-за крупнозернистой дендритной структуры, поверхность чистого алюминия покрывается плотной оксидной пленкой, магний имеет высокую скорость собственной коррозии. Для придания протекторам требуемых эксплуатационных свойств в их состав вводят легирующие элементы.
В состав цинковых протекторов вводят Cd (0,025-0,15%) и А1 (0,1-0,5%). Содержание таких примесей, как Fe, Cu, Pb, стараются поддерживать на уровне не более 0,001-0,005 %. В состав алюминиевых протекторов вводят добавки, предотвращающие образование оксидных слоев на их поверхности — Zn (до 8 %), Mg (до 5 %), а также Cd, In, Gl, Hg, Tl, Mn, Si (от сотых до десятых долей процента), способствующие требуемому изменению параметров решетки. Магниевые протекторные сплавы в качестве легирующих добавок содержат Al (5-7 %) и Zn (2-5 %); содержание таких примесей, как Fe, Ni, Cu, Pb, Si поддерживают на уровне десятых или сотых долей процента. Железо в качестве протекторного материала используют либо в чистом виде (Fe-армко), либо в виде углеродистых сталей.
Цинковые протекторы применяют для защиты оборудования, эксплуатирующегося в морской воде (морских судов, трубопроводов, прибрежных сооружений). Применение их в слабосоленой, пресной воде и грунтах ограничено вследствие образования на их поверхности слоев гидроксида Zn(OH)2 или оксида цинка Zn O.
Алюминиевые протекторы применяют для защиты сооружений, эксплуатирующихся в проточной морской воде, а также для защиты портовых сооружений и конструкций, располагающихся в прибрежном шельфе.
Магниевые протекторы преимущественно применяют для защиты небольших сооружений в слабоэлектропроводных средах, где эффективность действия алюминиевых и цинковых протекторов низка, — грунтах, пресных или слабосоленых водах. Однако из-за высокой скорости собственного растворения и склонности к образованию на поверхности труднорастворимых соединений область эксплуатации магниевых протекторов ограничивается средами с рН = 9,5 – 10,5. При защите магниевыми протекторами закрытых систем, например резервуаров, необходимо учитывать возможность образования гремучего газа вследствие выделения водорода в катодной реакции, протекающей на поверхности магниевого сплава. Использование магниевых протекторов сопряжено также с опасностью развития водородного охрупчивания и коррозионного растрескивания оборудования.
Как и в случае катодной защиты внешним током, эффективность протекторной защиты возрастает при ее совместном использовании с защитными покрытиями. Так, нанесение битумного покрытия на трубопроводы значительно улучшает распределение защитного тока, уменьшает число анодов и увеличивает протяженность участка трубопровода, защищаемого с помощью одного протектора. Если одним магниевым анодом можно обеспечить защиту непокрытого трубопровода длиной всего 30 м, то защита покрытого битумом трубопровода действует на длину до 8 км.
3.2 Анодная защита
Анодную защиту применяют при эксплуатации оборудования в хорошо электропроводных средах и изготовленного из легко пассивирующихся материалов – углеродистых, низколегированных нержавеющих сталей, титана, высоколегированных сплавов на основе железа. Анодная защита перспективна в случае оборудования, изготовленного из разнородных пассивирующихся материалов, например нержавеющих сталей различного состава, сварных соединений.
Анодная защита осуществляется присоединением защищаемой металлической конструкции к положительному полюсу внешнего источника постоянного тока или к металлу с более положительным потенциалом (катодный протектор).
При этом потенциал защищаемого металла смещается в положительную сторону до достижения устойчивого пассивного состояния (рис. 50).
В результате происходит не только существенное (в тысячи раз) снижение скорости коррозии металла, но и предотвращение попадания продуктов его растворения в производимый продукт.
Катоды, используемые при анодной защите от внешнего источника тока, должны иметь высокую устойчивость в коррозионной среде. Выбор материала катода определяется характеристиками среды. Используют такие материалы, как Pt, Ta, Pb, Ni, платинированную латунь, высоколегированные нержавеющие стали и др. Схема расположения катодов проектируется индивидуально для каждого конкретного случая защиты.
В качестве катодного проектора можно использовать такие материалы, как углерод, диоксид марганца, магнетит, диоксид свинца, имеющие весьма положительный потенциал.
Анодная защита от внешнего источника основана на пропускании тока через защищаемый объект и на смещении потенциала коррозии в сторону более положительных значений.
Установка для анодной защиты состоит из объекта защиты, катода, электрода сравнения и источника электрического тока.
Основным условием возможности применения анодной защиты является наличие протяженной области устойчивой пассивности металла при плотности тока растворения металла не более (1,5— 6,0)·10-1А/м2.
Основным критерием, характеризующим состояние поверхности металла, является электродный потенциал. Обычно возможность применения анодной защиты для конкретного металла или сплава определяют методом снятия анодных поляризационных кривых. При этом получают следующие данные:
а) потенциал коррозии металла в исследуемом растворе;
б) протяженность области устойчивой пассивности;
в) плотность тока в области устойчивой пассивности.
Эффективность защиты определяют как отношение скорости коррозии без защиты к скорости коррозии под защитой.
Как правило, параметры анодной защиты, полученные в лабораторных и производственных условиях, хорошо согласуются между собой. В зависимости от конкретных условий эксплуатации область защитных потенциалов при анодной защите лежит на 0,3-1,5В положительнее потенциала свободной коррозии, а скорость растворения металлов при этом может уменьшиться в тысячи раз.
Существенным ограничением применения анодной защиты является вероятность возникновения локальных видов коррозии в области пассивного состояния металла. Для предотвращения этого явления на основании предварительных исследований рекомендуют такое значение защитного потенциала, при котором локальные виды коррозии не возникают или в раствор вводят ингибирующие добавки. Например, анодная защита стали 12X18Н10Т в растворах хлоридов в присутствии ионов N03- предотвращает образование питтингов и снижает скорость растворения стали в 2000 раз. В ряде случаев вследствие повышенной опасности возникновения локальных коррозионных процессов применение анодной защиты неэффективно. Резкий рост тока пассивации металлов с увеличением температуры агрессивных сред ограничивает применение анодной защиты в условиях повышенных температур.
При стационарном режиме работы установки величина тока поляризации, требуемого для поддержания устойчивого пассивного состояния, постоянно меняется вследствие изменения эксплуатационных параметров коррозионной среды (температуры, химического состава, условий перемешивания, скорости движения раствора и др.). Поддерживать потенциал металлоконструкции в заданных границах можно путем постоянной или периодической поляризации. В случае периодической поляризации включение и выключение тока производят либо при достижении определенного значения потенциала, либо при его отклонении на определенную величину. В обоих случаях параметры анодной защиты определяют опытным способом в лабораторных условиях.
Для успешного применения анодной защиты объект должен отвечать следующим требованиям:
а) материал аппарата должен пассивироваться в технологической среде;
б) конструкция аппарата не должна иметь заклепок, количество щелей и воздушных карманов должно быть минимальным, сварка должна быть качественной;
в) катод и электрод сравнения в защищаемом устройстве должны постоянно находиться в растворе.
В химической промышленности для анодной защиты наиболее пригодны аппараты цилиндрической формы, а также теплообменники. В настоящее время анодная защита нержавеющих сталей применяется для мерников, сборников, цистерн, хранилищ в производстве серной кислоты, минеральных удобрений, аммиачных растворов. Описаны случаи применения анодной защиты теплообменной аппаратуры в производствах серной кислоты и искусственного волокна, а также ванн для химического никелирования.
Метод анодной защиты имеет относительно ограниченное применение, так как пассивация эффективна в основном в окислительных средах при отсутствии активных депассивирующих ионов, например ионов хлора для железа и нержавеющих сталей. Кроме того, анодная защита потенциально опасна: в случае перерыва подачи тока возможно активирование металла и его интенсивное анодное растворение. Поэтому анодная защита требует наличия тщательной системы контроля.
В отличие от катодной защиты скорость коррозии при анодной защите никогда не уменьшается до нуля, хотя может быть и очень небольшой. Зато защитная плотность тока здесь значительно ниже, а потребление электроэнергии невелико.
Другое достоинство анодной защиты — высокая рассеивающая способность, т.е. возможность защиты на более отдаленном от катода расстоянии и в электрически экранированных участках.
3.3 Кислородная защита
Кислородная защита является разновидностью электрохимической защиты, при которой смещение потенциала защищаемой металлоконструкции в положительную сторону осуществляется путем насыщения коррозионной среды кислородом. В результате этого скорость катодного процесса настолько возрастает, что становится возможным перевод стали из активного в пассивное состояние.

Рисунок- Зависимость скорости коррозии низколегированной стали в воде при температуре 300 °С от концентрации кислорода в воде
Поскольку величина критического тока пассивации сплавов Fe-Cr, к которым относятся и стали, существенно зависит от содержания в них хрома, ее эффективность возрастает с увеличением концентрации хрома в сплаве. Кислородная защита применяется при коррозии теплоэнергетического оборудования, эксплуатирующегося в воде при высоких параметрах (высокие температура и давление). На рис. представлена зависимость скорости коррозии низколегированной стали от концентрации кислорода в высокотемпературной воде. Как видно, увеличение концентрации растворенного в воде кислорода приводит к первоначальному росту скорости коррозии, последующему се снижению и дальнейшей стационарности. Низкие стационарные скорости растворения стали (в 10—30 раз ниже имеющих место без защиты) достигаются при содержании кислорода в воде ~ 1,8 г/л. Кислородная защита металлов нашла применение в атомной энергетике.
4. Разработка и производство новых конструкционных материалов повышенной коррозионной устойчивости
Улучшение антикоррозионных свойств самих металлических материалов осуществляется:
1) устранением из металлов и сплавов примесей, ускоряющих коррозионные процессы;
2) легированием.
Чистые металлы и сплавы, то есть металлические конструкционные материалы, практически беспримесные, строго отвечают заданному поведению. Поскольку в них нет отклонений от стехиометрии в составе и структуре, то нет отклонений и в поведении.
Для наиболее ответственных конструкций и аппаратов налажен промышленный выпуск металлов и сплавов, обладающих высокой чистотой и применяемых в ракетостроении, ядерной технике и т.д.
Примеси в металлах и сплавах образуют дефекты в кристаллах. Из-за дефектов запас энергии реальных кристаллов выше, чем идеальных, что обуславливает более реакционную способность первых.
В условиях газовой коррозии примеси влияют не только на жаропрочность, но и жаростойкость. Технические стали делятся на стали обыкновенного качества и качественные. Качественные стали имеют узкие пределы по содержанию примесей (серы, фосфора, неметаллических включений и др.) по количеству и макро- и микроструктуры. Например, наличие в стали серы приводит к тому, что при 1000 – 1200 ºС в местах ее скопления возникают надрывы и трещины. Растворенный в стали или меди водород делает металл более хрупким. Фосфор, образуя фосфиды железа (легкоплавкие эвтектики), оказывает вредное влияние на свойства стали.
При электрохимической коррозии металлов и сплавов наличие примесей приводит к образованию микрогальванических элементов с основным металлом и увеличению скорости коррозии. При значительном накоплении примесей может протекать и контактная коррозия. Поэтому повышение чистоты конструкционных материалов ведет к снижению коррозионных потерь.
Легирование металлов и сплавов повышает их коррозионную стойкость. Сильно повышается коррозионная стойкость железа при введении более 12% хрома, марганца в магниевые сплавы, никеля в железные сплавы, меди в никелевые сплавы и т.д.
Для жаростойких сплавов на основе железа основными легирующими компонентами являются хром, кремний и алюминий.
Под действием высоких температур кремний, алюминий и хром образуют тугоплавкие оксиды. Так, температура плавления Al2O3 и Cr2O3 составляет 2320 и 2500 ºС соответственно. При легировании стали хромом, алюминием и кремнием на поверхности образуются окалиностойкие пленки (Cr Fe)2O3, (Al Fe)2O3 или (Si Fe)2O3. Железо на воздухе легко окисляется при 500ºС и выше. Для низкохромистой стали с содержанием 5-8% хрома окалиностойкость (жаростойкость) повышается до 700 – 750 ºС; введение в сталь 15-18% хрома повышает жаростойкость до 950 – 1000 ºС, а при 25% хрома – до 1100 ºС.
Как метод защиты от электрохимической коррозии из трех контролирующих факторов коррозии по Н.Д.Томашову – анодного и катодного торможения и омического сопротивления легирование в основном воздействует на первые два фактора.
Эффективность катодного и анодного процессов можно понизить:
а) повышением термодинамической устойчивости сплава, вводя в сплав (твердый раствор) значительное количество (по правилу Таммана) более благородного компонента (легирование стали никелем, никеля медью, меди золотом и др.);
б) повышение способности перехода анодной фазы в пассивное состояние (создание хромистых сталей, легирование никеля хромом, то есть получение нихромов и никонелей);
в) введением в очень небольшом количестве активных катодов, способствующих катодному процессу (с кислородной деполяризацией), самопассивированию металла (легирование хромистых и хромоникелевых сплавов малым количеством платины для повышения устойчивости к атмосферной коррозии, сырого чугуна медью для повышения устойчивости к азотной кислоте и т.д.);
г) если для неокислительных сред повышать перенапряжение выделения водорода (легирование стали мышьяком, сурьмой или висмутом, цинка кадмием и т.д.).
При кислотной коррозии в восстановительных средах, когда отсутствует возможность пассивирования, весьма полезны методы а) и г). В окислительных средах применимы все методы снижения активности анодного процесса, кроме г).
Принципы легирования и создания сплавов повышенной коррозионной стойкости более подробно рассматривались в предыдущих главах.
5. Переход в ряде конструкций от металлических к химически стойким неметаллическим материалам
Дополнительным резервом для организации противокоррозионной защиты являются неметаллические материалы. Из стекла, керамики, ситаллов, винипласта, фаолита, графита и других неметаллических материалов могут быть изготовлены отдельные аппараты или детали к ним. Их отличительной особенностью является высокая коррозионная стойкость во многих агрессивных средах. Подробно неметаллические материалы рассмотрены в главе V, часть 4
6. Рациональное конструирование и эксплуатация металлических сооружений и деталей
При проектировании химического производства, как правило, уделяют основное внимание анализу характера агрессивной среды и условиям протекания процесса. Руководствуясь этими данными, выбирают материал, обладающий достаточным химическим сопротивлением. Однако конструкционный материал ,наиболее стойкий в данной коррозионной среде, далеко не во всех случаях позволяет предотвращать опасность быстрого коррозионного разрушения. Поэтому столь же пристального внимания заслуживает рациональное конструирование отдельных узлов и аппаратов. Неудачное конструирование во многих случаях может явиться причиной образования застойных зон, зазоров, концентрации напряжений и других явлений, способствующих возникновению и протеканию коррозии.
Вместе с тем уже на стадии проектирования можно предусмотреть такие конструктивные решения отдельных узлов аппарата, которые значительно снизят или устранят возможность возникновения процесса коррозии.
При конструировании оборудования следует обращать внимание на характер обработки поверхности металла, контакт соединительных элементов из различных материалов, режим распределения потоков теплоносителя, наличие щелей и зазоров, возможность образования застойных зон.
Гладкая поверхность металла имеет меньше дефектов в виде царапин, неровностей и т.д. На шероховатой поверхности легче скапливаются грязь, пыль и другие вещества. Это особенно характерно для производства удобрений, солей. Металлическое оборудование и конструкции с шероховатой поверхностью в этом случае покрываются различными веществами. Если эти вещества гигроскопичны, то они прилипают к поверхности металла, создаются местные очаги с высокой концентрацией электролита, что способствует усилению коррозии.
Если в конструируемом аппарате есть детали, выполненные из различных металлических материалов, то возникает опасность появления контактной коррозии. В этом случае еще на стадии проектирования обязательно должны быть приняты меры по предотвращению или ослаблению этого явления. Обычно применяют один из двух возможных приемов.
Контактирующие детали из разнородных металлов изготавливают с различной величиной поверхности. При этом деталь с наименьшей поверхностью должна быть выполнена из более благородного металла (втулки вентилей, поршневые кольца насосов и т.д.).
Если такой способ оказывается невозможным, то детали из разных материалов изолируют друг от друга. Особое внимание при этом следует уделить свойствам прокладочного материала. Он должен быть инертным по отношению к рабочей среде, иметь высокую износостойкость. Некоторые изоляционные материалы (войлок, асбест, древесина) могут впитывать и удерживать влагу и, таким образом, быть очагами усиления коррозии. Некоторые полимерные материалы, подвергаясь со временем старению, при соприкосновении с водой могут выделять коррозионноактивные агенты, ускоряющие разрушение металлов. Поэтому изоляционные материалы часто пропитывают дегтем или битумом, а применяемые полимерные материалы подвергают специальным исследованиям с целью определения опасности выделения агрессивных агентов.
Многие процессы протекают при повышенных температурах. Поверхность металла, соприкасающаяся с теплоносителями, подвергается дополнительному коррозионному воздействию. Чем выше температура, тем интенсивнее происходит разрушение металла. Например, теплообменники являются одним из наименее стойких видов оборудования. В 92% случаев причиной отказа в работе теплообменников является коррозия теплоотдающих поверхностей.
При проектировании аппаратов следует предусмотреть равномерное распределение теплового потока, исключить возможность локального перегрева. Во многих промышленных аппаратах, в которых протекают высокотемпературные процессы, такие меры предусмотрены. Например, в производстве аммиака между катализаторной коробкой, в которой осуществляется реакция при температуре 350-420 ºС, и корпусом аппарата предусмотрен канал, внутри которого циркулируется холодный газ. Таким конструктивным приемом предохраняют стенки аппарата от перегрева.
Если в химическом процессе используют реакторы с рубашкой, то внутри реактора должна быть установлена мешалка для обеспечения равномерного перемещения жидкости мимо теплопередающей поверхности.
Змеевики, кипятильники и другое оборудование для нагрева технологических сред должны быть погружены в жидкость.
Для теплообменного оборудования наиболее распространенными являются локальные виды коррозии, такие, как питтинговая, щелевая, межкристаллитная.
При проектировании конструкций должны быть обозначены места и способы сварки. При сварке металлов в зоне шва и околошовной зоне создаются большие растягивающие напряжения. В зонах, расположенных вдоль шва, где металл нагревается выше критических температур, меняется структура металла. Это может привести к растрескиванию металла.
При конструировании сварных узлов и деталей следует предусмотреть ряд мер: избегать скопления швов, исключить точечную сварку, при которой особенно велика концентрация напряжений, применять местный отжиг и т.д.
Скопление влаги в различных элементах конструкции способствует развитию коррозии. Поэтому при создании различных конструкций предусматривают возможность проветривания полостей, наличие дренажных отверстий и др. Очень опасными в коррозионном отношении зонами в аппаратуре являются зазоры и щели. В них может происходить концентрирование рабочего раствора, нарушается аэрация, что неизбежно приведет к развитию местной коррозии. С этой точки зрения опасны прерывистые, сварные швы, в которых вследствие неплотного прилегания материала друг к другу образуются щели и зазоры, являющиеся причиной возникновения щелевой коррозии.
Образование застойных зон жидкости в аппаратах и трубопроводах сильно увеличивает возможность возникновения коррозии за счет образования микропара неравномерной аэрации. Этому способствует и отложение различных осадков в застойной зоне. На изделии не должно быть различных углублений, канавок и пазов, в которых может скапливаться влага. Элементы конструкции должны быть по возможности обтекаемыми, это облегчает испарение влаги.
В рационально сконструированных узлах устранена возможность скапливания влаги и продуктов коррозии, предусмотрена возможность удаления осадка.
Существуют и другие требования к конструированию, обеспечивающие создание изделий, в наименьшей степени подверженных опасности развития коррозии. К ним относятся: требования к общей компоновке и расположению элементов, учет возможности нанесения и возобновления различных покрытий в процессе эксплуатации и при ремонте, учет особенностей эксплуатации изделий и др.
© 2009 База Рефератов