
Рефераты по рекламе
Рефераты по физике
Рефераты по философии
Рефераты по финансам
Рефераты по химии
Рефераты по хозяйственному праву
Рефераты по цифровым устройствам
Рефераты по экологическому праву
Рефераты по экономико-математическому моделированию
Рефераты по экономической географии
Рефераты по экономической теории
Рефераты по этике
Рефераты по юриспруденции
Рефераты по языковедению
Рефераты по юридическим наукам
Рефераты по истории
Рефераты по компьютерным наукам
Рефераты по медицинским наукам
Рефераты по финансовым наукам
Рефераты по управленческим наукам
психология педагогика
Промышленность производство
Биология и химия
Языкознание филология
Издательское дело и полиграфия
Рефераты по краеведению и этнографии
Рефераты по религии и мифологии
Рефераты по медицине
Реферат: Ароматичні вуглеводні сполуки
Реферат: Ароматичні вуглеводні сполуки
Ароматичні вуглеводні сполуки
ВСТУП
Назва ароматичні сполуки виникла на початку 19-го ст., коли були вперше відкриті сполуки цього типу при їх виділенні із рослинних смол і бальзамів, що мали дуже приємні запахи. І хоч пізніше виявилось, що в основної більшості ароматичних сполук, навпаки, запахи неприємні, однак назва збереглася.
Ароматичні вуглеводні (арени) – це циклічн сполуки бензенового ряду, що мають специфічну властивість – ароматичність, яка зумовлює спільні ознаки в їх будові та реакційній здатності.
Структурним родоначальником аренів бензен.
1 АРОМАТИЧНІСТЬ. БУДОВА МОЛЕКУЛИ БЕНЗЕНУ
Поняття ароматичність об¢єдну сукупність певних ознак, які визначаються за правилом Хюккеля:
Ароматичною називається замкнута система, що має плоский циклічний s–скелет і 4n+2 узагальнених p–електрони, де n = =1,2,3,…
Структура молекули бензену С6Н6 ідеально відповідає правилу ароматичності Хюккеля, оскільки в ній всі шість атомів С перебувають у стані sp2-гібридизації. Внаслідок цього осі трьох sp2-гібридизованих одноелектронних орбіталей знаходяться на одній площині під кутом 1200, а вісь четвертої, негібридизованої, рz-орбіталі розміщується перпендикулярно до них (рис. 13б). Кожний атом карбону утворює за рахунок гібридизованих орбіталей три s-зв¢язки: два – із сусідніми атомами карбону, а третій – при перекриванні зі сферичною s-орбіталлю атома гідрогену (рис. 13а). Отже, усі s-зв¢язки в молекулі С6Н6 копланарні, тобто лежать на одній площині. Таким чином, шість атомів С без напруження замикаються за допомогою s-зв¢язків у правильний шестикутник – так званий s-скелет молекули.
Шість негібридизованих рz-орбіталей, як розміщуються перпендикулярно до s-скелета і паралельно одна до одної, взаємно перекриваються, утворюючи єдину делокалізовану p-електронну хмару, тобто виникає колове спряження (рис.3в). Найбільша електронна густина в цій спряженій системі розміщується над і під площиною s-скелета молекули і охоплює всі шість атомів С у циклі. Завдяки коловому спряженню вс зв¢язки між атомами карбону вирівнюються, вони мають однакову довжину (0,139нм), яка є проміжною між довжиною подвійного зв¢язку в алкенах (0,133нм) і одинарного в алканах (0,154нм). Вирівнювання зв¢язків С–С у бензені графічно зображується правильним колом всередині правильного шестикутника
Колове спряження та вирівнювання довжини зв¢язків приводить до того, що зв¢язки у бензені не можуть вважатися одинарними чи подвійними. На основі точних фізико-хімічних методів дослідження встановлено, що насправді кратність зв¢язків С–С у молекулі бензену становить 1,67.
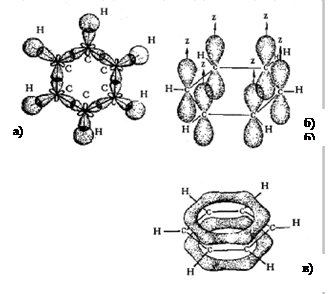
Рисунок 3 – Будова молекули бензену: а) s-скелет молекули; б) розташування негібридизованих pz-орбіталей перпендикулярно до площини σ-зв’язків; в) утворення колового спряження
Колове спряження дає виграш в енергії 150,7 кДж/моль. Нагадаємо, що енергетичний виграш за рахунок утворення спряжено системи називається енергією спряження, або енергією делокалізації, і дорівню енергії, яку необхідно витратити для руйнування ароматичної системи.
Електронна будова і ароматичність бензену зумовлює його властивості, у тому числі високу термічну стійкість (він не розкладається навіть при нагріванні до 9000С), відсутність схильності до реакцій приєднання (незважаючи на велику ненасиченість), оскільки реакц приєднання супроводжуються порушенням ароматичності, а це енергетично невигідно.
2. КЛАСИФІКАЦІЯ. НОМЕНКЛАТУРА
За кількістю бензенових кілець арени поділяються на дві групи.
1Моноядерні арени – це бензен та його гомологи, в яких один чи декілька атомів гідрогену заміщені на аліфатичн бокові ланцюги (насичені чи ненасичені). Назви моноядерних аренів утворюються від родоначальної структури – бензену (стара назва бензену, яка трапляється досить часто, – бензол) із зазначенням природи замісників та їх положення. Для багатьох гомологів бензену вживають тривіальні назви, які набули настільки широкого розповсюдження, що їх було введено у правила номенклатури IUPAC. Якщо бензенове кільце містить два радикали, то залежно від їх взаємного розташування використовуються додаткові префікси: орто- (1,2-положення), мета- (1,3-положення) і пара- (1,4-положення). Приклади моноядерних аренів:
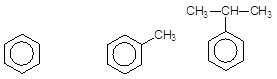
Бензен Толуол Кумол
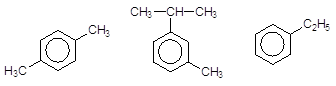
n-Ксилол м-Цимол Етилбензен
(1,4-диметилбензен) (3-ізопропілметилбензен)
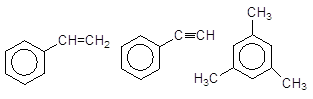 Стирен Фенілацетилен Мезитилен
Стирен Фенілацетилен Мезитилен
Дуже часто для називання складних сполук необхідно знати назви ароматичних радикалів – арилів, які умовно позначаються спільним символом Ar:
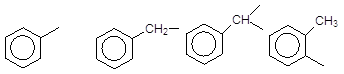
(С6Н5-) (С6Н5-СН2-) (С6Н5-СН=) (о-СH3-С6Н4-)
Феніл Бензил Бензиліден о-Толіл
2Поліядерні арени, які складаються з декількох бензенових ядер. Вони, у свою чергу, поділяються на конденсовані та неконденсовані, або ізольовані.
Назви неконденсованих (ізольованих) поліаренів утворюються згідно із замісниковим і радикально-функціональним способами IUPAC:
![]()
Дифеніл Дифенілметан м-Фенілтолуол
Для конденсованих поліядерних аренів вживаються такі назви:
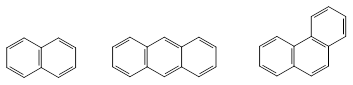
Нафталін Антрацен Фенантрен
У монозаміщених похідних нафталіну однотипні атоми карбону позначаються грецькими буквами a і b, у дизаміщених – цифрами від 1 до 8, при цьому атоми С, спільні для обох циклів, не нумеруються. В неконденсованих поліядерних аренах одне кільце нумерується цифрами без штрихів, а всі інші – із штрихами, наприклад:
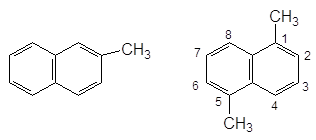
b-Метилнафталін 1,5-Диметилнафталін
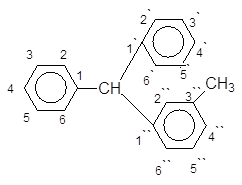
3¢¢ - Метилтрифенілметан
ІЗОМЕРІЯ МОНОЯДЕРНИХ АРЕНІВ
Ізомерія монозаміщених моноядерних аренів зумовлена будовою замісника, наприклад:
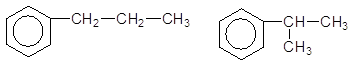
Пропілбензен Ізопропілбензен
У ди- і багатозаміщених гомологів бензену виникає ще один вид ізомерії, зумовлений різним положенням замісників:
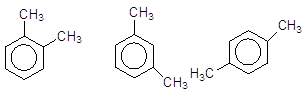
орто-Ксилол мета-Ксилол nара-Ксилол
ФІЗИЧНІ ВЛАСТИВОСТІ
Моноядерні арени – безбарвні леткі рідини з густинами 0,8-0,9г/мл, нерозчинні у воді, але добре розчинні у малополярних розчинниках.
Самі вони також є добрими розчинниками. Температури кипіння гомологів бензену зростають із підвищенням молекулярно маси: кожна нова метиленова група –СН2– збільшує температуру кипіння у середньому на 20-300. Всі арени мають характерні запахи, деякі (толуол) виявляють помітну наркотичну дію.
Бензен і більшість конденсованих поліаренів належать до високотоксичних речовин. Вдихання їх парів викликає головний біль, а при високих концентраціях – отруєння. Пари бензену вражають слизисту оболонку ока. А рідкий бензен може проникати через шкіру. Для нього характерна кумулятивність, тобто виявлення токсичної дії при поступовому накопиченні в організмі.
Поліядерні арени – білі тверді речовини, майже без запаху, слизькі на дотик, нерозчинні у воді.
ХІМІЧНІ ВЛАСТИВОСТІ БЕНЗЕНУ
Незважаючи на велику ненасиченість аренів, для них не характерні реакції приєднання. Більш того, ненасиченість бензену не відкривається за допомогою звичайних якісних реакцій: він не знебарвлює н бромну воду, ні розчин KMnO4.
Хімічні властивості аренів зумовлюються у першу чергу наявністю спряженої системи і високою енергією делокалізації, тому бензен і його гомологи вступають переважно в такі реакції, при яких зберігається їх ароматичність.
І Реакції електрофільного заміщення SE
Механізм реакцій електрофільного заміщення за участю аренів складається з декількох послідовних стадій.
1 Генерування електрофільної частинки у відповідних умовах під впливом каталізатора, який сприяє спочатку поляризації, а потім і розриву зв¢язків у молекулі реагенту:
Поляризація
молекули d+ d– Розрив зв¢язку
Е – А –––––––––––––à E A –––––––––––––––à E+ + A-.
Каталізатор
2 Утворення p-комплексу. Початкова атака електрофілом Е+ p-електронної хмари бензенового кільця проходить швидко і без порушення ароматичності системи:
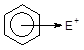
![]() Швидко
Швидко
+ Е+ ––––––––––à
ß–––––––––
p-Комплекс
3 Утворення s-комплексу повільна стадія, під час якої електрофіл Е+ утворює s-зв¢язок з одним із атомів карбону за рахунок двох p-електронів, які вилучаються із спряженої системи. При цьому атом карбону переходить із sp2- у sp3-гібридизований стан, ароматичність системи порушується, тому що у кільц залишаються тільки чотири p-електрони, які розподіляються на п¢ять sp2-гібридизованих атомів карбону. Молекула перетворюється в s-комплекс карбкатіон, точніше – аренонієвий катіон:
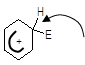
![]() Повільно
Повільно
–––––––à sp3-Гібридизований атом карбону
p-Комплекс s-Комплекс (аренонієвий катіон)
4 Повернення ароматичності. Оскільки втрата ароматичності енергетично невигідна, система прагне повернути її найпростішим шляхом, а саме – відщепленням протону Н+ від s-комплексу. Внаслідок цього два електрони, що утворювали зв¢язок С-Н, приєднуються до тих чотирьох p-електронів, які залишалися в s-комплексі. Тому замкнута шестиелектронна система поновлюється і молекула переходить в ароматичний стан:
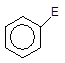
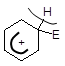 Швидко
Швидко
–––––––––à + H+.
s-Комплекс Продукт Протон
5 Утворення побічного продукту. Відщеплений протон взаємодіє з негативно зарядженим аніоном А-, що утворився при розриві зв¢язків у молекулі реагенту на перший стадії:
Н+ + А- –––––––à HA.
Побічний продукт
У загальному вигляді механізм реакції електрофільного заміщення в аренах можна зобразити схемою
 + Е+ Û –––à
+ Е+ Û –––à
Субстрат Електрофіл p-Комплекс
 –H+
–H+
–––> –––––––>
s-Комплекс Продукт
Розглянемо найважливіші реакц електрофільного заміщення SE.
1 Галогенування бензену проходить тільки за
наявності каталізаторів – так званих кислот Льюїса (речовин, здатних зв¢язувати
вільну електронну пару): AlCl3, FeCl3, AlBr3, FeBr3, SnCl4, TiCl4, BF3.
Практичного значення набули реакції хлорування та бромування, тому що реакція з
хімічно активним F2 проходить деструктивно, а з І2 – дає надзвичайно малий
вихід завдяки низькій реакційній здатності йоду.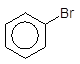

80оC
+ Br2 –––––à + HBr,
AlВr3
Бромбензен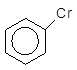
![]()
25оC
+ Cl2 ––––––––à + HCl.
AlCl3
2 Нітрування. Бензен реагує дуже повільно навіть з концентрованою HNO3 при нагріванні, але при дії на нього нітрувальною сумішшю (суміш концентрованих HNO3 i H2SO4) досить легко перетворюється на нітропохідні.
Електрофільною частинкою є нітроїл-катіон NO2+, який утворюється під впливом сірчаної кислоти:
HO-NO2(к) + 2H2SO4 (к) Û 2HSO4- + H3O+ + NO2+,
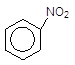
![]() 50оС
50оС
+ HO-NO2(к) --------à + H2O.
H2SO4 (к)
Бензен Нітробензен
3 Сульфування. Бензен сульфується при звичайній
температурі олеумом (розчин SO3 у 100% H2SO4) або чадною сірчаною кислотою, яка дає SO3 внаслідок встановлення рівноваги:
2H2SO4 Û SO3 + H3O+ + HSO4-.
Отже, електрофільним реагентом сульфур(ІV) оксид, оскільки за рахунок трьох електронегативних атомів оксигену, які відтягують на себе електронну густину зв¢язків S=О, на атомі сульфуру виникає великий дефіцит електронної густини і достатньо значний частковий позитивний заряд (3d+). Реакція сульфування належить до оборотних процесів: при оброблюванні продукту перегрітою водяною парою проходить зворотна реакція – десульфування:
![]()
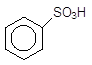 SO3×H2SO4, 250C
SO3×H2SO4, 250C
––––––––––––––––à
ß––––––––––––––––.
H2O, 1500C (-H2SO4)
Бензен Бензенсульфонова кислота
4 Алкілування – реакція Фріделя-Крафтса введення алкільної групи у бензенове кільце за наявності каталізаторів (кислот Льюїса) з утворенням гомологів бензену. Як алкілувальний реагент використовують галогеналкани СnH2n+1Hal, спирти CnH2n+1OH, алкени CnH2n, наприклад:
 |
|||||
 |
|||||
80о
+ CH3Cl ––––––à + HCl.
AlCl3
Бензен Толуол
Каталізатор ініціює утворення електрофілу за схемою
СН3Cl + AlCl3 à CH3+ + [AlCl4]-.
Реакції з алкенами і спиртами каталізуються найчастіше кислотами
![]()
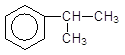 0оC
0оC
+ СH3-CH====CH2 à,
HF
Ізопропілбензен (кумол)
![]()
![]()
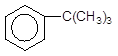 OH 60оC
OH 60оC
![]() + СH3-C-CH3 –––––––––à.
+ СH3-C-CH3 –––––––––à.
OH H3PO4 Трет-бутилбензен
![]() 5 Ацилювання – заміщення атома гідрогену в бензеновому кільці на
ацильну групу RCO. Ацилювальним реагентом є галогенангідриди чи ангідриди
карбонових кислот; при цьому одержують змішані ароматично-аліфатичні кетони.
5 Ацилювання – заміщення атома гідрогену в бензеновому кільці на
ацильну групу RCO. Ацилювальним реагентом є галогенангідриди чи ангідриди
карбонових кислот; при цьому одержують змішані ароматично-аліфатичні кетони.
O 80оC
![]()
![]()
![]() +
СН3-С --------à +
HCl
+
СН3-С --------à +
HCl
Cl AlCl3
Бензен Хлорацетил Ацетофенон
![]() O
O
![]()
![]() CH3-C 80оC.
CH3-C 80оC.
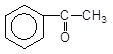
![]()
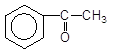 + O
--------à +
CH3COOH
+ O
--------à +
CH3COOH
![]() CH3-C AlCl3
CH3-C AlCl3
О
Бензен Ангідрид оцтової кислоти Ацетофенон
ІІ Реакції приєднання АЕ
Реакціі приєднання для ароматичних вуглеводнів не характерні, оскільки вони супроводжуються порушенням ароматичності і вимагають великої витрати енергії. Тому ці реакції проводяться в дуже жорстких умовах:
1 Гідрування (відновлення)
200оC, 50 Атм
+ 3Н2 ––––––––––––à .
Ni
Бензен Циклогексан
Гідрування використовується для одержання циклогексану, який є, по-перше, добрим розчинником, а по-друге, – вихідною речовиною при добуванні адипінової кислоти, а з неї – капролактаму.
Реакція оборотна: при 3000С і нормальному тиску проходить зворотний процес.
2 Хлорування при інтенсивному ультрафіолетовому опромінюванні:
![]() УФ
УФ
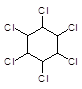 + 3Cl2
à
+ 3Cl2
à
Гексахлорциклогексан (гексахлоран)
Гексахлоран – сильна харчова, контактна дихальна отрута, застосовується як інсектицид: смертельна доза для мух становить усього 10-12 г.
ІІІ Реакції окиснення
Відмінною рисою ароматичних вуглеводнів
х стійкість по відношенню навіть до сильних окисників. У звичайних умовах на
них не діють ні концентровані кислоти, ні хромова суміш, ні розчин KMnO4. Однак
у жорстких умовах вони піддаються окисненню:
О О
![]()
![]()
![]()
![]() 500оC НС С НС С О
500оC НС С НС С О
+ О2 ––––––à О––––à О
V2O5 НС С НС С
Бензен -2СО2 О О
-2Н2О
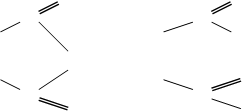
Малеїновий ангідрид Малеїнова кислота
Малеїновий ангідрид і малеїнова кислота використовуються у виробництві поліестерних смол, склопластику і лакофарбових матеріалів.
У живих організмах бензен під дією ферментів окиснюється до дуже шкідливої сполуки – муконової кислоти:

+ 2О2 –––––––à HOOC-CH=CH-CH=CH-COOH.
Бензен Фермент Муконова кислота
ВПЛИВ ЗАМІСНИКІВ НА РЕАКЦІЙНУ ЗДАТНІСТЬ АРОМАТИЧНИХ ВУГЛЕВОДНІВ
Найважливішим чинником, що визначає хімічн властивості речовин, є розподілення електронної густини в молекулах, яке залежить від взаємного впливу атомів і атомних груп. Якщо молекула містить тільки s-зв¢язки, взаємний вплив здійснюється через індуктивні ефекти, а в спряжених системах виявляється дія мезомерного ефекту.
Мезомерний ефект, або ефект спряження – це зміщення електронів, які утворюють p-зв¢язки спряженої системи, а також неподілених електронних пар атомів електронегативних елементів (0, S, N), що містяться у ланцюгу.
Замісники можуть виявляти позитивний мезомерний ефект (+М), якщо зміщують p-електронну густину від себе, негативний мезомерний ефект (-М), якщо зміщення електронної густини відбувається у протилежному напрямку.
Одна і та сама група атомів може виявляти одночасно два електронних ефекти: мезомерний і індуктивний. Обидва ефекти можуть як збігатися, так і не збігатися за напрямком свого впливу. Наприклад, аміногрупа NH2 виявляє негативний індуктивний ефект (–І), тобто зміщу електронну густину σ-зв’язку на себе, і в той же час – позитивний мезомерний (+М), завдяки якому π-електронна густина спряженої системи зміщується від аміногрупи. Найчастіше вплив мезомерного ефекту перебільшує дію ндуктивного.
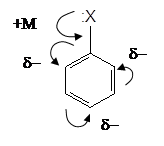
Молекула бензену – ця спряжена система з рівномірним і симетричним розподіленням шестиелектронної p-електронно хмари. Однак наявність у бензеновому кільці замісника призводить до певного перерозподілу електронної густини і, як наслідок, до зміни реакційної здатност сполуки. Тобто замісник виявляє орієнтуючу (спрямовуючу) дію при введенні у кільце ще одного, нового замісника.
За характером орієнтуючої дії замісники поділяються на два типи.
Замісники І роду (елек–тронодонорні), як підвищують електронну густину бензенового кільця (особливо в о- і n-положеннях) збільшують швидкість реакцій електрофільного заміщення SE. Такі замісники називаються активуючими.
До них належать атоми і атомні групи з позитивним мезомерним (+М) чи індуктивним (+І) ефектом (табл. 2).
Оскільки електроно–донорний замісник утворює з кільцем загальну спряжену систему, то відбувається перерозподіл електронної густини таким чином, що найбільша її частина зосереджується в о- n-положеннях на атомах С – з цієї причини їх часто називають орто- і параорієнтантами. За рахунок виникнення часткових негативних зарядів (d-) ці атоми карбону стають центрами електрофільної атаки. До того ж полярність зв¢язків С-Н в о- і n-положеннях збільшується, тому зростає рухливість атомів Н, що полегшує їх заміщення.
Серед замісників І роду окреме місце займають галогени, які хоч і виявляють о- і n-орієнтуючу дію, але на відміну від інших електронодонорних замісників ускладнюють вступ нового замісника сповільнюють швидкість реакції SE порівняно із бензеном. Така особливість галогенів поснюється тим, що їх негативний індуктивний ефект за абсолютною величиною перебільшує позитивний мезомерний ефект | -I| > |+M|.
Подвійний о- і n-орієнтуючий вплив електронодонорних замісників приводить до утворення внаслідок реакцій SE суміш зомерів, наприклад:
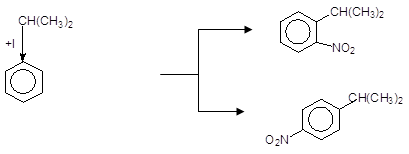 +Н2О
+Н2О
+ HO-NO2 о-Нітрокумол
+ H2O
Кумол
n-Нітрокумол
Замісники ІІ роду (електроноакцепторні) це метаорієнтанти, які знижують електронну густину бензенового кільця зменшують швидкість реакцій електрофільного заміщення. Їх називають дезактивуючими замісниками (табл. 2).
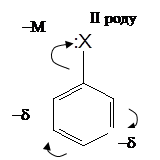
Замісниками ІІ роду є атоми і атомні групи, які відтягують p-електронну хмару бензенового кільця на себе завдяки негативному мезомерному (-М) чи негативному індукційному (-І) ефекту. Тому електронна густина на бензеновому кільці зменшується і внаслідок її перерозподілу лишається дуже незначний за величиною частковий негативний заряд (d-) на атомах карбону в мета-положеннях. Отже, замісники ІІ роду зменшують реакційну здатність кільця в реакціях SE, однак напрямлюють нові електрофільні групи у мета-положення, хоч реакції SE проходять дуже повільно.
Таблиця 2 – Вплив замісників на реакційну здатність та напрямок реакцій електрофільного заміщення в ароматичному кільці
| Замісник | Тип електрон–ного ефекту | Вплив на реакційну здатність* | Переважна орієнтуюча дія |
| Замісники І роду | |||
| -NH2, -NHR, -NR2, OH- | +M >> -I | + + + | o-, n- |
| -O– | +M, +I | + + + | o-,n- |
| -NHCOCH3, -OCH3, (-OR) | +M > -I | + + | o-, n- |
| -CH3, -CnH2n+1 | +I | + | o-, n- |
| -C6H5, -CH=CH2, -CºCH | +M > -I | + | o-, n- |
| -F, -Cl, -Br, -I | +M < -I | - | o-, n- |
| Замісники ІІ роду | |||
|
-CN, -CH=O, -COR, -COOH, -COOR, -SO3H |
-I, -M | - - | м- |
| -NR3+, -CF3, -CCl3 | -I | - - - | м- |
| -NO2, -N2+ | -I, -M | - - - | |
|
* Активують сильно ( + + +), помірно ( + +) , слабо (+); дезактивують сильно ( - - -), помірно ( - - ), слабо ( - ). |
|||
Наприклад, швидкість реакції нітрування нітробензену в 10000 разів менша, ніж швидкість нітрування самого бензену:
![]()
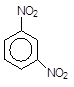 t0
t0
+ HO-NO2 ------à + H2O.
H2SO4
Нітробензен 1,3-Динітробензен
Правила орієнтації дозволяють передбачити переважний напрямок перебігу реакції, однак вони рідко виконуються з абсолютною точністю. У продуктах реакції можуть одночасно міститися о-, n- і м-ізомери, але їх відносна кількість буде різною. Наприклад, при нітруванні толуолу продукти утворюються у таких масових співвідношеннях: n–нітротолуол (38%), о–нітротолуол (58%), м–нітротолуол (4%).
Відносна реакційна здатність, що зумовлюється впливом замісника, може змінюватися у широкому діапазоні. Вона визначається природою самого замісника, характером реагенту і умовами реакції. Наприклад, швидкість бромування, хлорування і нітрування толуолу відповідно у 600; 300 і 30 разів більша, ніж швидкість цих реакцій з бензеном.
Правила орієнтації в аренах з двома замісниками
У тому випадку, коли ароматична сполука містить декілька різних за природою замісників, їх узагальнений орієнтуючий вплив буває відмінним від індивідуальної дії кожного окремого замісника.
Узгоджена орієнтація виявляється, якщо обидва замісники напрямлюють вступ нової електрофільної частинки однаково, тобто до одного і того атома карбону, наприклад (на схемі стрілками показан місця можливого вступу третього замісника):
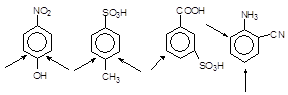
1 2 3 4
1. n-Нітрофенол
2. n-Метилбензен-сульфонова кислота
3. м-Сульфо-бензойна кислота
4. о-Аміно-бензнітрил
Неузгоджена орієнтація буває тоді, коли орієнтуюча дія одного замісника не збігається за напрямком із впливом іншого замісника. В цьому випадку також можна передбачити напрямок реакції, керуючись такими правилами.
1 Якщо бензенове кільце містить одночасно активуючі і дезактивуючі замісники, які конкурують між собою, то орієнтація вступу нового електрофільного реагенту визначається активуючим замісником, наприклад:
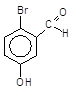
![]() ––––> +
HBr
––––> +
HBr
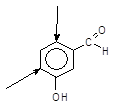
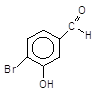 + Br2––––– 2–Бром–5–гідрокситбензальдегид
+ Br2––––– 2–Бром–5–гідрокситбензальдегид
AlBr3
––––> + HBr
3–Гідроксибензальдегід
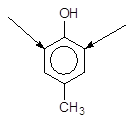 2 Якщо бензенове кільце містить сильну і слабку активуючі групи (обидва
замісники І роду), то напрямок вступу нового електрофільного реагенту
визначається сильнішим замісником (табл.2), наприклад:
2 Якщо бензенове кільце містить сильну і слабку активуючі групи (обидва
замісники І роду), то напрямок вступу нового електрофільного реагенту
визначається сильнішим замісником (табл.2), наприклад:
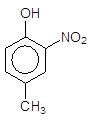
+HO-NO2----à + H2O
4-Метилфенол (n-крезол) 4-Метил-2-нітрофенол
3 Якщо два замісники перебувають у мета-положеннях один відносно другого, то новий замісник майже не вступає у кільце між ними, навіть якщо це випливає із узгодженої орієнтації. Наприклад, масові співвідношення продуктів нітрування ароматичної сполуки із узгодженим впливом замісників дані у дужках:
![]()
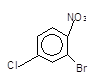 –––––––>
–––––––>
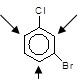
(H2SO4) 2–Бром–4–хлорнітро–
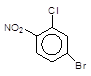 + HO–NO2
> бензен (62%)
+ HO–NO2
> бензен (62%)
–H2O
3–Бромхлорбензен –––––––>
4–Бром–2–хлорнітро–
бензен (37%)
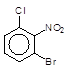
––––––––>
2–Бром–6–хлорнітробензен (1%)
ХІМІЧНІ ОСОБЛИВОСТІ ГОМОЛОГІВ БЕНЗЕНУ
В основному для гомологів бензену характерн такі самі властивості, що і для самого бензену. Однак наявність вуглеводневого радикала, яка сприяє перерозподілу електронної густини, накладає свою специфіку на швидкість і напрямок проходження реакцій.
І Реакції електрофільного заміщення в алкілбензенах
Внаслідок реакцій електрофільного заміщення за участю гомологів бензену утворюється суміш продуктів, як було показано на прикладі мононітрування толуолу в параграфі ІІІ.6. Оскільки алкільний радикал СН3 належить до замісників І роду, тобто є орто- і пара-орієнтаном, то утворюється суміш головним чином о- і n-нітротолуолів.
Однак активуюча дія метильного радикала, який полегшує реакції SE, приводить до того, що нітрування в більш жорстких умовах дає тризаміщену нітросполуку:
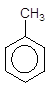 140о
140о
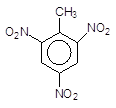 +
3HO-NO2 ––––à + 3H2O.
+
3HO-NO2 ––––à + 3H2O.
олеум
Толуол 2,4,6-Тринітротолуол (тротил)
Реакційна здатність аренів з двома чи з трьома насиченими радикалами ще більше зростає, особливо якщо вони мають узгоджену орієнтацію. Так, мезителен легко нітрується навіть при від¢ємних температурах:
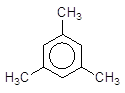 |
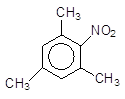 |
||
-10оC
+ HO-NO2(розв.) à + Н2О.
CH3COOH
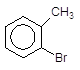 Мезитилен 2,4,6-Триметилнітробензен
Мезитилен 2,4,6-Триметилнітробензен
Аналогічно до мононітрування толуолу проходять реакції SE з іншими реагентами, наприклад, бромування:
![]()
![]() ––à + HBr,
––à + HBr,
о-Бромтолуол
+ Br2 ––––à
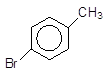 FeBr3
FeBr3
Толуол –––à + HBr.
n-Бромтолуол
Алкілувальні реагенти діють менш селективно порівняно з іншими електрофілами. Так, метилювання толуолу при 00С дає о- n-ксилоли, а при підвищеній температурі – мета-ізомер. Цікаво, що нагрівання о- n-ксилолів спричиняє їх ізомеризацію:
ІІ Реакції у бокових ланцюгах
Поряд з реакціями SE для алкілбензенів характерні реакції галогенування за механізмом SR, які проводять у відповідних умовах. Заміщення атомів Н у боковому ланцюгу на галоген проходить селективно, особливо при бромуванні: переважно заміщується бензильний атом Н, тобто гідроген, безпосередньо сполучений з атомом карбону, найближчим до ароматичного ядра. Така селективність пояснюється впливом бензенового кільця на міцність зв¢язку С-Н у бензильному положенні і невеликою енергією зв¢язку (314кДж/моль). З цієї причини швидкість радикального бромування толуолу у 3 рази більша, ніж бромування ізобутану (нагадуємо, що при третинному карбон енергія зв¢язку С-Н дорівнює 376кДж/моль) і аж у 108 разів більша, ніж бромування метану. Хлор як більш реакційно активний реагент,виявляє не таку повну селективність (масове співвідношення між ізомерними продуктами наведене у дужках):
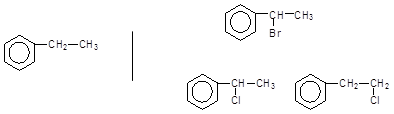 Br2, УФ + HBr
Br2, УФ + HBr
–––––>
–––––– Cl2, hn
Етилбензен ––––>
1–Феніл–1– 2–Феніл–1–
хлорбензен хлорбензен
(90%) (10%)
Арени з насиченими боковими ланцюгами піддаються дегідруванню (реакції елімінування Е) при одержанні стирену, який використовують для виробництва синтетичних каучуків:
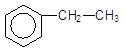 500оC
500оC
––––––à + H2.
Al2O3/Cr2O3
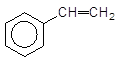 Етилбензен
Стирен (стирол)
Етилбензен
Стирен (стирол)
Гомологи бензену з ненасиченими боковими ланцюгами дуже важко вступають у реакції SE в ароматичному кільці, якщо кратний зв¢язок знаходиться при бензильному атомі карбону (тобто замісники належать до дезактивуючих м-орієнтантів, які сповільнюють реакцію).
Однак у той самий час вуглеводням з ненасиченим боковим ланцюгом притаманні всі реакції, характерні для сполук з подвійними і потрійними зв¢язками, наприклад, знебарвлення бромної води, а для похідних фенілацетилену – якісна реакція на крайній потрійний зв¢язок:
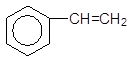 |
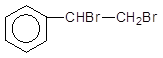 |
||
+ Br2 –––––à ,
Стирен Н2О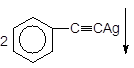 1,2-Дибромфенілетан
1,2-Дибромфенілетан
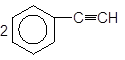
+ Ag2O ––à + H2O.
NH4OH
Фенілацетилен Фенілацетиленід аргентуму(І)
ІІІ Окиснення
На відміну від бензену його гомологи значно легше окиснюються навіть лужним розчином KMnO4, за винятком алкілбензенів з третинним бензильним атомом карбону. Для трет-алкілбензенів необхідно створювати більш жорсткі умови, наприклад, кип¢ятіння з концентрованим сірчанокислим розчином KMnO4. Продуктом окиснення завжди бува бензойна кислота – незалежно від довжини і розгалуженості бокового ланцюга.
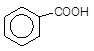
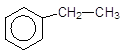 [O]
[O]
–––––––à + CO2,
KMnO4, KOH
Етилбензен Бензойна кислота
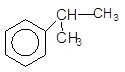
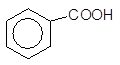 [O]
[O]
––––––––à + 2 CO2,
KMnO4, KOH
Кумол
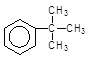 |
|||
[O]
––––––––––––––––––à ,
KMnO4, KOH
Трет-Бутилбензен
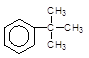 |
|||
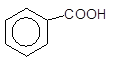 |
|||
[O], t0
––––––––––––––––à + 3 CO2.
KMnO4, H2SO4(конц.)
Полізаміщені гомологи бензену при окисненн дають багатоосновні кислоти:
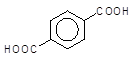
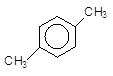 [O]
[O]
–––––––––à ,
KMnO4, KOH
n-Ксилол Бензен-1,4-дикарбонова (терефталева) кислота
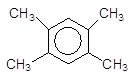
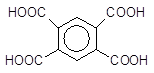 [O]
[O]
–––––––––––à .
KMnO4, KOH
Дурол (1,2,4,5-тетраметил–бензен) Бензен-1,2,4,5- тетракарбонова (піромелітова) кислота
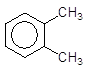
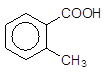 Можна
здійснити і селективне окиснення тільки одного алкільного радикала при дії на
дизаміщений арен гарячою розведеною азотною кислотою
Можна
здійснити і селективне окиснення тільки одного алкільного радикала при дії на
дизаміщений арен гарячою розведеною азотною кислотою
[O]
–––––––––à ,
HNO3 (розв.)
о-Ксилол о-Толуїлова кислота
[O]
–––––––à .
HNO3 (розв.)
n-Цимол n-Толуїлова кислота

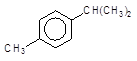 Реакції окиснення використовують для ідентифікації аренів (одержуючи
певну кислоту, за її будовою встановлюють взаємне розміщення бокових ланцюгів у
вихідному алкілбензені) і для промислового добування важливих продуктів.
Наприклад, терефталеву кислоту піддають сополімеризації з багатоатомним
спиртом, внаслідок чого утворюються важливі поліестери.
Реакції окиснення використовують для ідентифікації аренів (одержуючи
певну кислоту, за її будовою встановлюють взаємне розміщення бокових ланцюгів у
вихідному алкілбензені) і для промислового добування важливих продуктів.
Наприклад, терефталеву кислоту піддають сополімеризації з багатоатомним
спиртом, внаслідок чого утворюються важливі поліестери.
ВЛАСТИВОСТІ ПОЛІЯДЕРНИХ АРЕНІВ
Ароматичні вуглеводні з неконденсованими
ядрами вступають у реакції електрофільного заміщення значно легше, ніж бензен,
подібно до толуолу. Причому утворюються переважно продукти n-заміщення: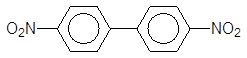
![]()
+ 2HO-NO2 ––––––à + H2O.
Дифеніл H2SO4 4,4¢-Динітридифеніл
Ди- і трифенілметани, крім того, піддаються реакціям радикального заміщення та окиснення за sp3-гібридизованим атомом карбону, наприклад:
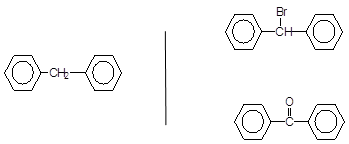 Br2, УФ
Br2, УФ
–––––> + HBr
Бромдифенілметан
Дифенілметан [O]
––––––>
CrO3, t0 Бензофенон
Конденсовані поліарени виявляють ще більшу схильність до реакцій електрофільного заміщення, які проходять в основному за a-положенням.
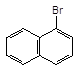 +Br2, 400C
+Br2, 400C
![]() ––––––––––> +
HBr
––––––––––> +
HBr
CH3COOH 1–Бромнафталін
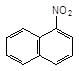
![]() HO–NO2
HO–NO2
––––––––––> +H2O
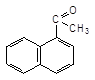 H2SO4 1–Нітронафталін
H2SO4 1–Нітронафталін
CH3COCl
––––––––––––> + HCl
AlCl3 1–Ацетонафтон
Сульфування нафталіну залежно від температури може давати різні продукти, один з яких здатний ізомеризуватися в нший за певних умов:
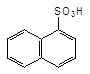 HO–SO3H,
80оC
HO–SO3H,
80оC
![]() ––––––––––>
+H2O
––––––––––>
+H2O
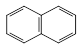
![]()
![]() Нафталін–1–сульфонова
кислота
Нафталін–1–сульфонова
кислота
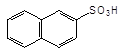 HO–SO3H, 160оC
HO–SO3H, 160оC
––––––––––>
Нафталін–2–сульфонова кислота
Якщо нафталін вже містить один замісник, то орієнтація вступу другого замісника підлягає певним правилам, схематично як можна зобразити так:
І роду І роду
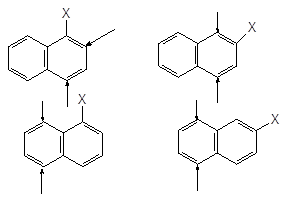
ІІ роду ІІ роду
Реакції, що супроводжуються порушенням ароматичності, для нафталіну проходять легше, ніж для бензену. Він може відновлюватися навіть воднем у момент виділення, наприклад, внаслідок взаємод Na із спиртом.
Окиснюється нафталін також значно легше порівняно з бензеном і може давати різні продукти залежно від умов
У заміщених похідних нафталіну окисненню піддається кільце з підвищеною електронною густиною:
І роду [O]
––––––––––à.
Фталева кислота
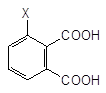 ІІ роду
ІІ роду
[O]
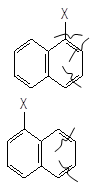 ––––––––à
––––––––à
Заміщена фталева кислота
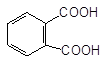 Антрацен і фенантрен характеризуються ще більшою реакційною здатністю,
ніж нафталін. У реакціях SE переважно утворюються продукти заміщення у
положенні 9:
Антрацен і фенантрен характеризуються ще більшою реакційною здатністю,
ніж нафталін. У реакціях SE переважно утворюються продукти заміщення у
положенні 9:
Br2
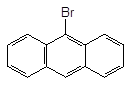
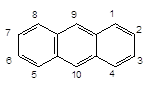 ––––––à + HBr,
––––––à + HBr,
FeBr3
Антрацен 9-Бромантрацен
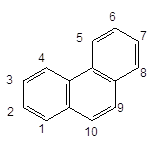 |
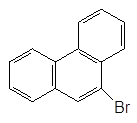 |
||
+ Br2 –––à + HBr.
Фенантрен 9-Бромфенантрен
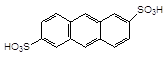
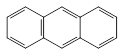
Нітрування, алкілування, ацилювання триядерних конденсованих аренів також проходить в положенні 9, а сульфування залежно від концентрації H2SO4 може давати a,a¢(1,8)- чи b,b¢(2,6)-продукти:
 HO-SO3H
(розв.)
HO-SO3H
(розв.)
![]() ––––––––––––à + H2O,
––––––––––––à + H2O,
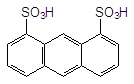 Aнтрацен-2.6-дисульфонова
кислота
Aнтрацен-2.6-дисульфонова
кислота
HO-SO3H (конц.)
–––––––––––––à + H2O.
Антрацен-1,8-дисульфонова кислота
Ці поліарени легко відновлюються до дигідропохідних і легко окиснюються до відповідних хінонів. Наприклад, антрацен при відновленні воднем (Na+C2H5OH) дає 9,10-дигідроантрацен, а при окисненн хромовою сумішшю – антрахінон-9,10. Аналогічні продукти утворює і фінанентрен.
Антрахінон і фенантренхінон є сировиною для добування багатьох барвників (алізарину, індатренового синього та ін.) та лікарських препаратів.
ОДЕРЖАННЯ АРЕНІВ
Більшість аренів мають важливе практичне значення, тому їх виробляють у великій кількості багатьма способами.
1 Фракційне розділення кам¢яновугільно смоли. Із 1т вугілля внаслідок коксування одержують близько 55кг кам¢яновугільно смоли, з якої виділяють приблизно 0,9кг бензену, 2,3кг нафталіну, 200г толуолу, 45г ксилолів, а також невеликі кількості a- і b-метилнафталінів, антрацену, фенантрену, дифенілу. Оскільки коксування вугілля – це багатотоннажне виробництво, виділення аренів із смоли досягає великих об¢ємів.
2 Ароматизація насичених вуглеводнів нафти, під час якої проходять процеси циклізації, дегідрування, ізомеризації:
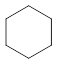
Дегідрування шестичленних циклоалканів проводять при каталітичному риформінгу – нагріванні нафтових фракцій до 5000С під тиском 17-50 Атм на алюмокобальтовому чи паладійплатиновому каталізаторі:

 tо,
P, kat
tо,
P, kat
––––––––à + 3H2.
3 Тримеризація алкінів – реакція Зелінського-Казанського:
650оC
 3СНºСН ––––––––––––à,
3СНºСН ––––––––––––à,
Cакт
Ацетилен Бензен
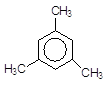 650оC
650оC
3СН3-СºСН ––––––––à.
Cакт
4 Лужне плавлення солей – реакція Дюма:
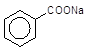
 t0
t0
+ NaOH ––––à + Na2CO3.
Бензоат натрію Плавл. Бензен
5 Відновлення фенолів при їх перегонці з
цинковим порошком![]()
![]()
![]()
tо
+ Zn –––––––à + ZnO.
Фенол Бензен
6 Гідроліз бензенсульфонових кислот гострою парою
tо
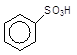
 + H2О ---------à + H2SO4.
+ H2О ---------à + H2SO4.
Бензенсульфонова кислота Бензен
7 Гідродезметилювання – новий спосіб одержання бензену із толуолу, впроваджений у виробництво останнім часом, оскільки потреба у бензені вища, ніж у толуолі.
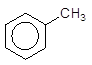 |
|||
 |
|||
750о
+ H2 ––––––––à + CН4.
Толуол Со, Мо Бензин
8 Одержання гомологів бензену включає й нші способи, крім перелічених:
- із галогенопохідних за Вюрцом-Фіттігом:
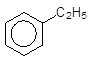
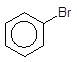 + 2Na
+ C2H5Br –––––à + 2NaBr;
+ 2Na
+ C2H5Br –––––à + 2NaBr;
Бромбензен Етилбензен
- алкілування за Фріделем-Крафтсом:
![]()
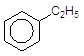 tо
tо
+ С2Н5Br –––––––à + HBr;
Бензен FeBr3 Етилбензен
відновлення кетонів за Клеменсеном
![]()
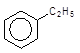 + 2Zn
+ 4HCl –à + 2ZnCl2;
+ 2Zn
+ 4HCl –à + 2ZnCl2;
Ацетофенон Етилбензен
9 Одержання поліаренів
1) Спосіб Бертло – пропускання парів бензену через розжарену залізну трубку:
![]()
tо
![]() 2 ––––––––––à + Н2;
2 ––––––––––à + Н2;
Бензен Fe Дифеніл
Спосіб Ульмана – нагрівання йодбензену з міддю:
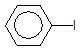 |
|||
2 + Cu ––––––à + CuI2;
Йодбензен Дифеніл
Реакція Вюрца-Фіттіга:
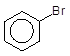 |
|||
2 + 2Na -------à + 2NaBr;
Бромбензен Дифеніл
Одержання арилметанів за Фріделем-Крафтсом:
![]()
![]() tо
tо
2 + CH2Cl2 –––à + 2HCl;
Дихлорметан AlCl3 Дифенілметан
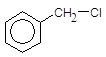
![]()
![]() tо
tо
+ ––à + HCl;
Бензилхлорид AlCl3
Бензен Дифенілметан![]()

80о
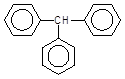 3 + CНCl3 –––à +
HCl;
3 + CНCl3 –––à +
HCl;
AlCl3
Хлороформ Трифенілметан
Відновлення бензофенону:
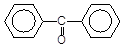
[H]
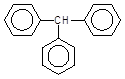 –––à + Н2О.
–––à + Н2О.
Дифенілметан Бензофенон
ВИКОРИСТАННЯ АРЕНІВ
Бензен використовується для одержання фенолу, стирену, аніліну, галогенопохідних аренів, а також для синтезу барвників, поверхнево-активних речовин, фармацевтичних препаратів, поліестерів (лаки, смоли) тощо.
Толуол застосовується у виробництв вибухових речовин (тротил), бензойного альдегіду, фенолу, бензилхлориду, який напівпродуктом в анілобарвниковій, парфюмерній, харчовій та інших галузях господарства.
Етилбензен іде на синтез стирену, з якого одержують полістирен (завдяки його високим електроізолювальним якостям з нього виготовляють електро- і радіовироби, труби, крани, посуд, пінопласти) бутадієнстиреновий каучук – для виробництва автомобільних покришок, камер, ебоніту.
Кумол витрачається у великих кількостях для синтезу фенолу і ацетону.
Ксилол у суміші (о-, n- і м-ізомери) використовують як розчинник і як компонент моторного палива (підвищує октанове число до 120 та більше); n-ксилол є основою виробництва синтетичного волокна лавсану (терилен).
Антрацен використовують у виробництв антрахінонових барвників.
© 2009 База Рефератов